Ammoniumchlorid In Wasser Reaktionsgleichung
Habt ihr euch jemals gefragt, was passiert, wenn man Ammoniumchlorid in Wasser kippt? Klingt erstmal nach einem Rezept für eine Chemie-Katastrophe, ist es aber gar nicht! Eher wie ein kleiner, faszinierender Tanz der Moleküle. Stellt euch vor, die Moleküle sind wie kleine, hyperaktive Tänzer, die wild durcheinander wirbeln.
Also, was genau passiert da? Die kurze Antwort (und haltet euch fest, jetzt kommt's): Die Reaktionsgleichung lautet:
NH4Cl (s) + H2O (l) ⇌ NH4+ (aq) + Cl- (aq)
Puh, das sieht erstmal nach einer Sprache aus, die nur von weißen Kitteln verstanden wird. Aber keine Panik! Wir übersetzen das mal ins Deutsche (oder besser gesagt, ins "Normalo-Deutsch").
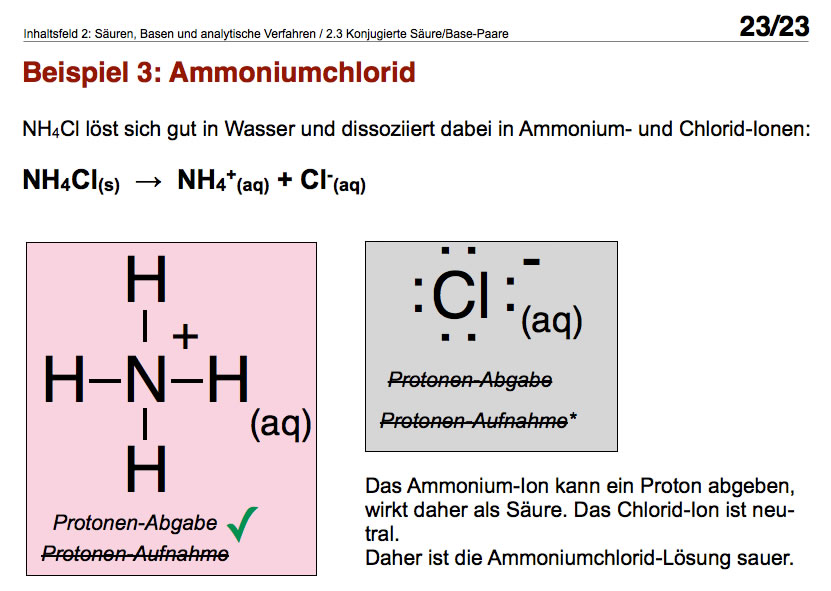
Ammoniumchlorid (NH4Cl), das ist unser Hauptdarsteller. Sagen wir mal, es ist wie ein kleiner, weißer, krümeliger Bösewicht, der darauf wartet, in Wasser (H2O) geworfen zu werden. Und dann… bam! Magie passiert! Oder eher, chemische Magie.
Wenn das Ammoniumchlorid mit Wasser in Berührung kommt, zerlegt es sich in zwei neue Teams: Ammonium-Ionen (NH4+) und Chlorid-Ionen (Cl-). Diese Ionen sind wie kleine, geladene Partikel, die im Wasser herumschwirren. Und das (aq) hinter den Ionen bedeutet einfach, dass sie in Wasser "aquatisiert" sind, also von Wassermolekülen umgeben und glücklich am Herumschwimmen sind.
Aber Moment mal… Was bedeutet dieses ⇌ Zeichen?
Dieses doppelte Pfeil-Ding (⇌) ist superwichtig! Es bedeutet, dass die Reaktion reversibel ist. Das heißt, die Reaktion geht nicht nur in eine Richtung (von Ammoniumchlorid zu Ionen), sondern auch in die andere Richtung (von Ionen zurück zu Ammoniumchlorid). Es ist wie ein chemisches Tauziehen, bei dem die beiden Seiten ständig versuchen, die Oberhand zu gewinnen.
Stellt euch vor, ihr habt eine Party. Auf der einen Seite stehen die "Ammoniumchlorid-Party-People", die am liebsten zusammenbleiben. Auf der anderen Seite sind die "Ionen-Einzelgänger", die es lieben, frei im Pool herumzutreiben (der Pool ist in diesem Fall das Wasser). Und das ⇌ Zeichen bedeutet, dass sich die Leute ständig entscheiden, ob sie zur Ammoniumchlorid-Gruppe gehören oder lieber alleine schwimmen gehen. Es ist ein ständiges Kommen und Gehen!
Und was ist mit der Temperatur?
Jetzt kommt der Clou: Wenn sich Ammoniumchlorid in Wasser auflöst, kühlt sich die Lösung ab! Ja, richtig gehört! Die Reaktion "zieht" Wärme aus der Umgebung. Das liegt daran, dass die Energie, die benötigt wird, um das Ammoniumchlorid in Ionen zu zerlegen, größer ist als die Energie, die freigesetzt wird, wenn die Ionen sich mit Wasser verbinden. Klingt kompliziert, ist aber eigentlich ganz einfach: Die Reaktion ist wie ein kleiner, chemischer Kühlschrank!
Ihr könnt das sogar selbst ausprobieren (aber bitte mit Vorsicht und unter Aufsicht eines Erwachsenen, wenn ihr noch jung seid!). Nehmt ein Glas Wasser, gebt Ammoniumchlorid hinzu und rührt um. Fasst das Glas an – es wird sich kälter anfühlen! Wow, ihr seid jetzt quasi kleine Chemiker!
Also, das nächste Mal, wenn ihr das Wort Ammoniumchlorid hört, denkt nicht an langweilige Chemie, sondern an kleine, tanzende Moleküle, ein Tauziehen zwischen Gruppen und Einzelgängern und einen kleinen Kühlschrank in eurem Wasserglas. Chemie kann so spannend sein!
Und falls ihr euch fragt, wofür man das Ganze überhaupt braucht: Ammoniumchlorid findet man in Düngemitteln, Batterien und sogar in Lakritz! Ja, richtig! Das Zeug, das eure Zunge kitzelt, könnte auch Ammoniumchlorid enthalten. Aber keine Sorge, in den Mengen ist es völlig harmlos (und lecker, je nach Geschmack!).
Also, auf in die Welt der Chemie! Es gibt noch so viel zu entdecken – und wer weiß, vielleicht findet ihr ja eure eigene, faszinierende chemische Reaktion!




+%2B+OH-(aq)+>+H2O(l).jpg)