Atomarten Mit Gleich Vielen Protonen Im Kern

Willkommen, liebe Reisende und Neuankömmlinge! Deutschland ist nicht nur ein Land der malerischen Landschaften und historischen Städte, sondern auch ein Hort wissenschaftlicher Innovationen. Vielleicht haben Sie sich schon immer gefragt, woraus die Welt besteht und wie die kleinsten Bausteine zusammenhängen. Keine Sorge, Sie brauchen keinen Doktortitel, um zu verstehen, worum es in diesem Artikel geht: Atomarten mit gleich vielen Protonen im Kern, auch bekannt als Elemente.
Die Grundlagen: Was sind Atome?
Stellen Sie sich vor, Sie zerlegen einen Gegenstand immer weiter in immer kleinere Teile. Irgendwann erreichen Sie eine Grenze, an der Sie den Gegenstand nicht mehr teilen können, ohne seine Eigenschaften zu verändern. Diese kleinste Einheit ist ein Atom. Atome sind die grundlegenden Bausteine aller Materie im Universum, von der Luft, die wir atmen, bis hin zu den prächtigen Schlössern, die wir in Deutschland bewundern.
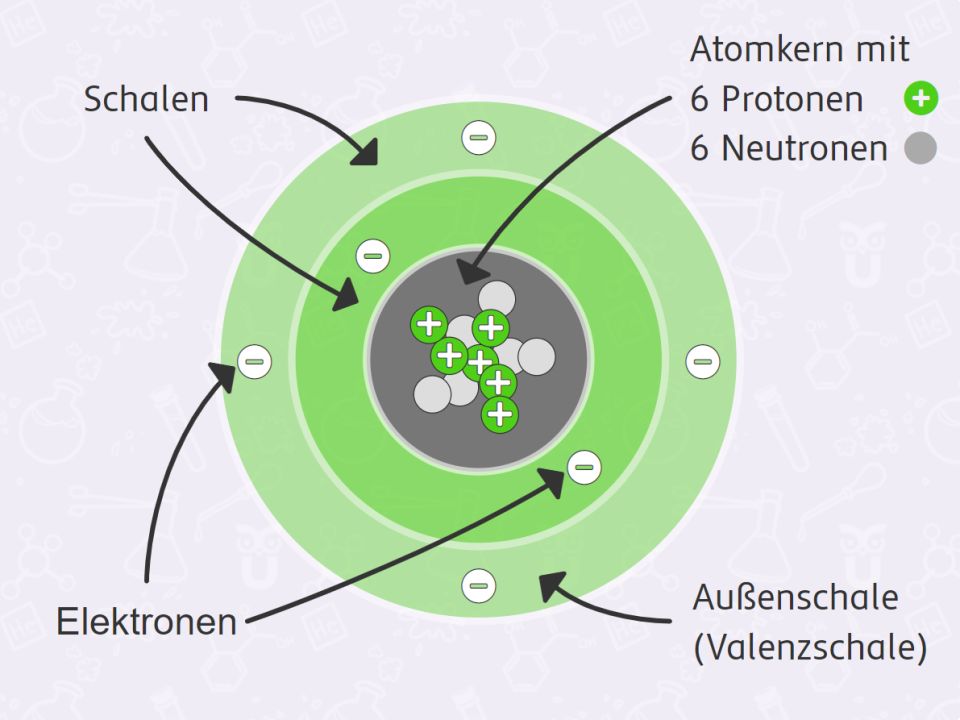
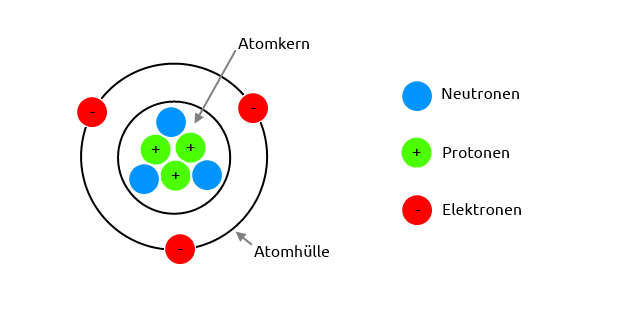
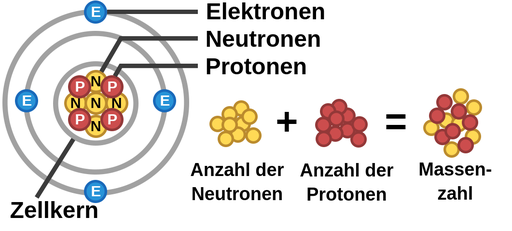
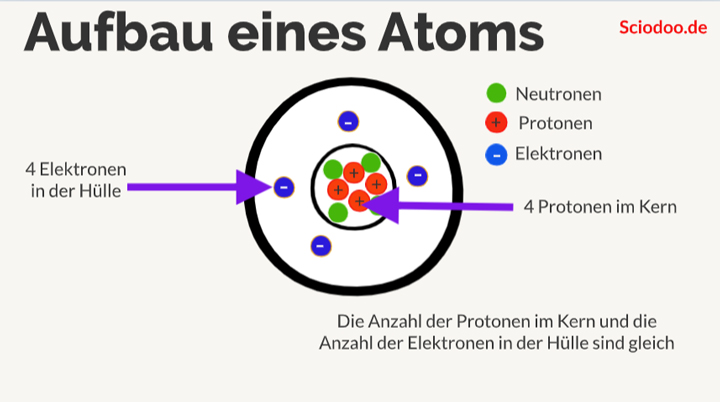
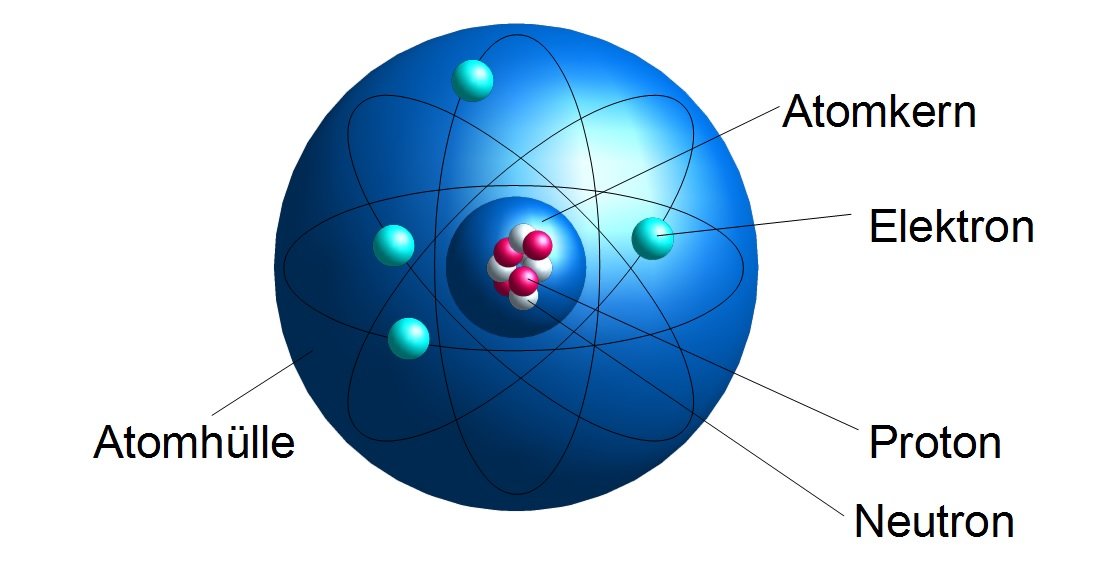
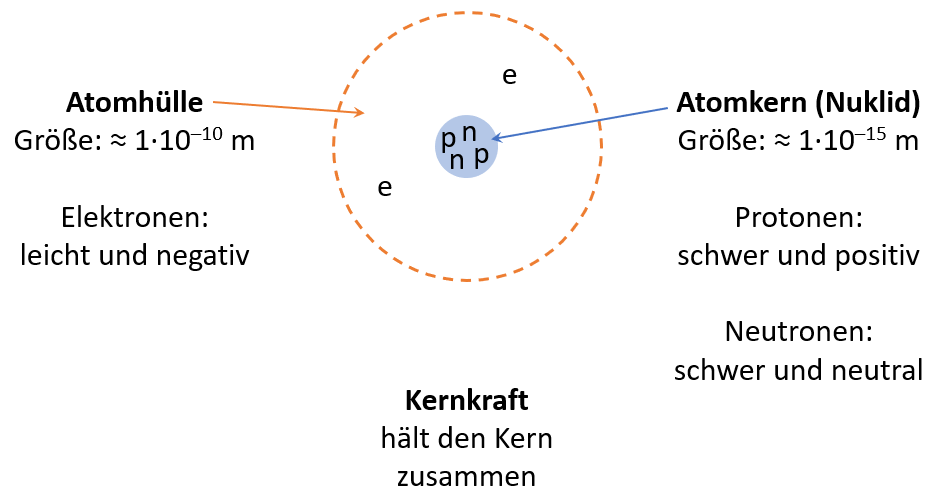
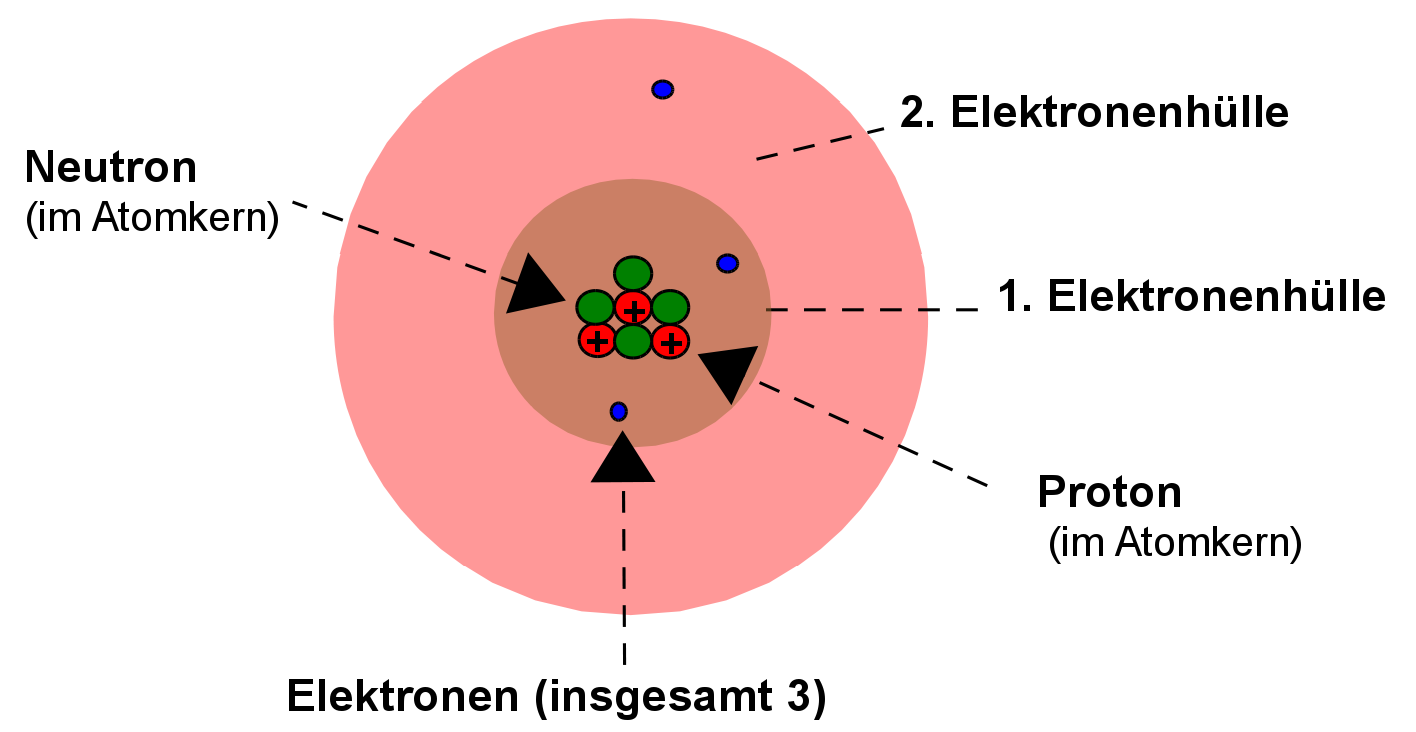
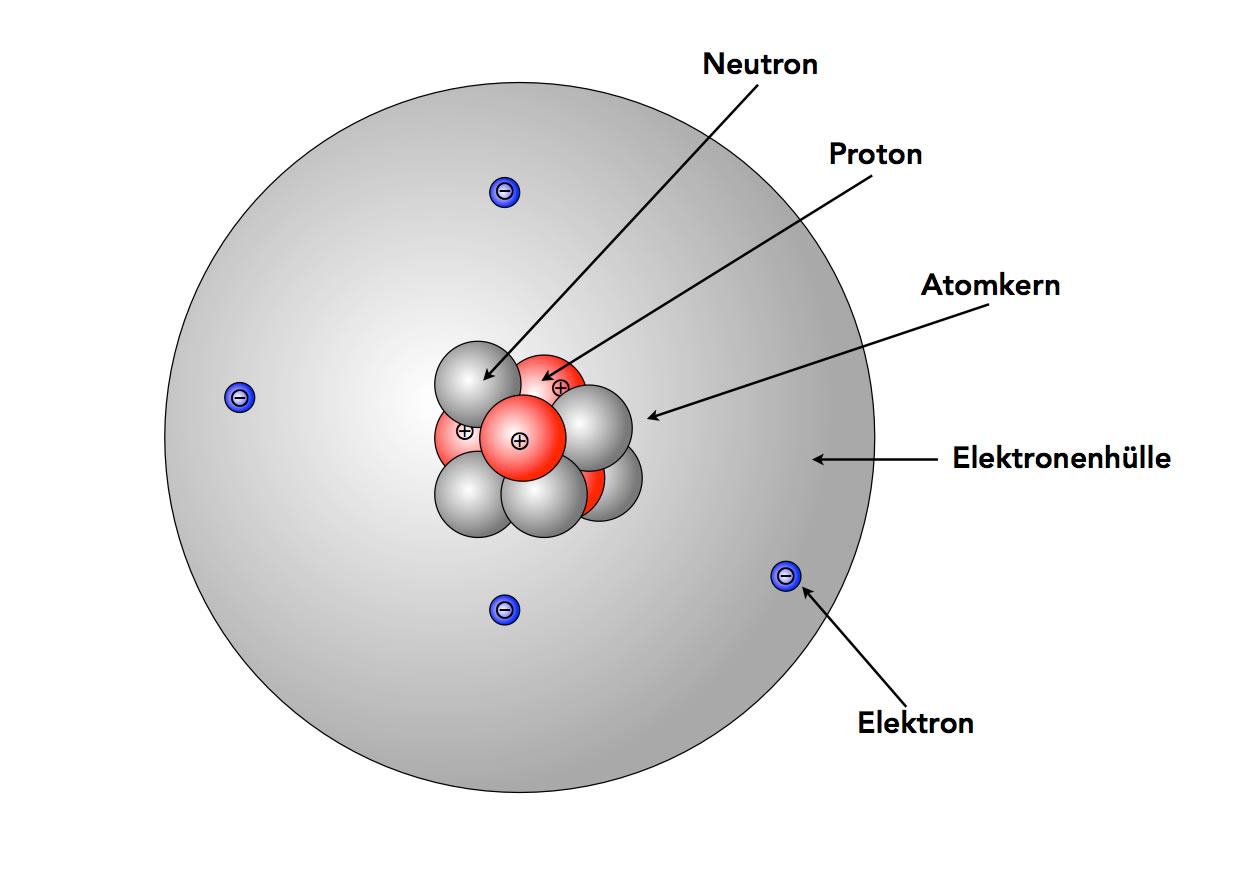
Jedes Atom besteht aus drei Hauptbestandteilen:
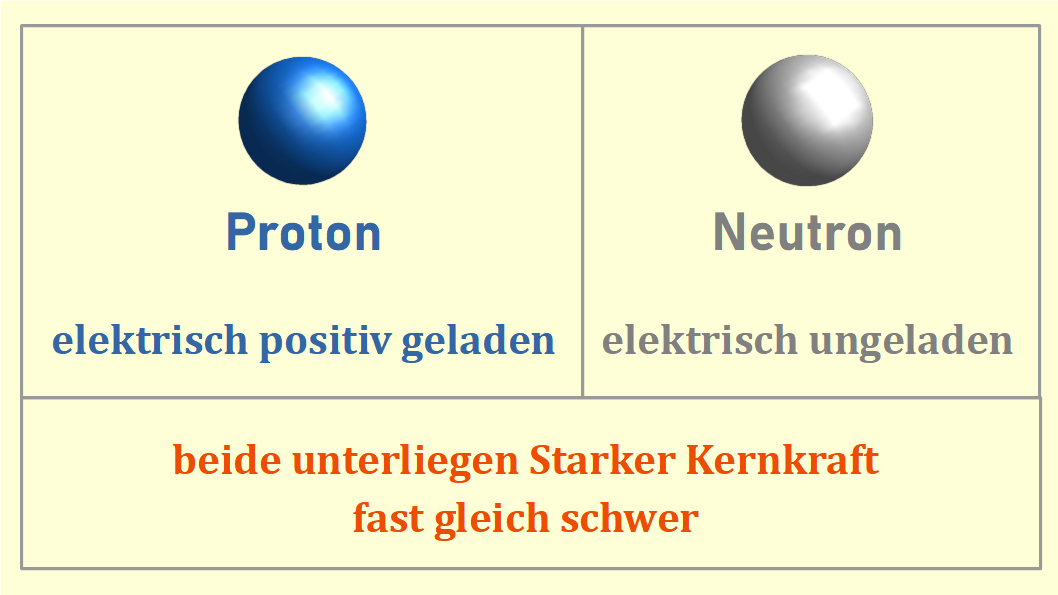
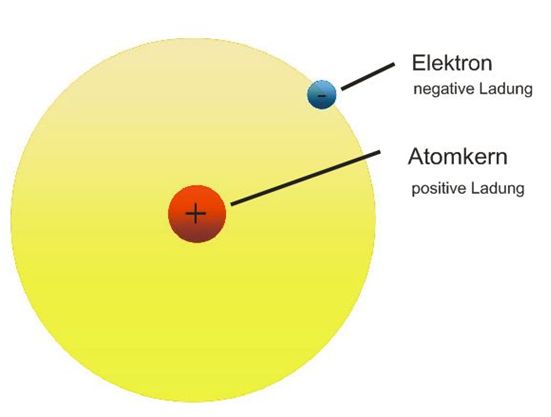
- Protonen: Positiv geladene Teilchen im Kern des Atoms. Die Anzahl der Protonen bestimmt, um welches Element es sich handelt.
- Neutronen: Neutrale (ungeladene) Teilchen, ebenfalls im Kern. Sie tragen zur Masse des Atoms bei.
- Elektronen: Negativ geladene Teilchen, die den Kern umkreisen. Sie bestimmen die chemischen Eigenschaften des Atoms.
Der Atomkern, der die Protonen und Neutronen enthält, ist das Zentrum des Atoms. Die Elektronen flitzen in Bahnen um den Kern herum, ähnlich wie Planeten um die Sonne kreisen (allerdings ist diese Analogie nicht ganz korrekt, da sich Elektronen quantenmechanisch verhalten). Die Anzahl der Protonen und Elektronen ist in einem neutralen Atom gleich, sodass sich die Ladungen ausgleichen.
Elemente: Die Welt ist aufgebaut wie ein Baukasten
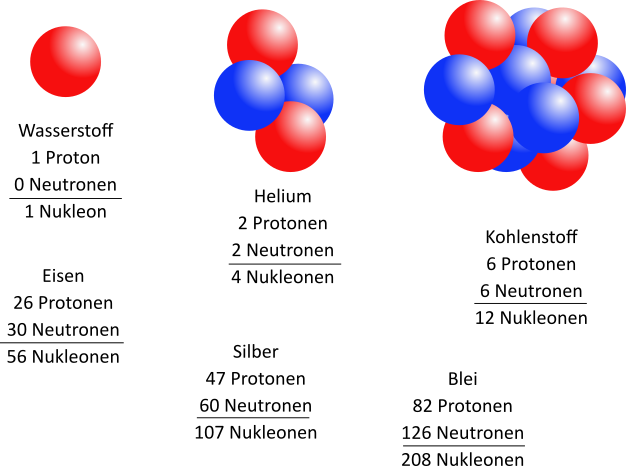
Jetzt kommt der springende Punkt: Atomarten mit gleich vielen Protonen im Kern definieren ein Element. Das bedeutet, dass alle Atome mit der gleichen Anzahl an Protonen zum selben Element gehören. Zum Beispiel haben alle Atome mit einem Proton im Kern das Element Wasserstoff (H), das leichteste und häufigste Element im Universum. Alle Atome mit sechs Protonen im Kern sind Kohlenstoff (C), das Element, das die Grundlage allen Lebens bildet und in Diamanten und Bleistiften vorkommt!
Diese Elemente sind in einem übersichtlichen System namens Periodensystem angeordnet. Das Periodensystem ist wie eine Landkarte der Elemente, die uns Informationen über ihre Eigenschaften und ihr Verhalten liefert. Die Elemente sind nach steigender Anzahl der Protonen (Ordnungszahl) angeordnet. Elemente in derselben Spalte (Gruppe) haben ähnliche chemische Eigenschaften.
Beispiele für Elemente und ihre Rolle in Deutschland:
- Eisen (Fe): Ein essentielles Element für den Bau von Brücken, Zügen und historischen Gebäuden. Deutschlands Ingenieurskunst ist ohne Eisen undenkbar.
- Kupfer (Cu): Verwendet in elektrischen Leitungen und Rohren. Die deutsche Industrie ist stark auf Kupfer angewiesen.
- Aluminium (Al): Ein leichtes und robustes Metall, das im Automobilbau und in der Luftfahrtindustrie eingesetzt wird. Deutschland ist ein bedeutender Standort für beide Branchen.
- Silizium (Si): Der Hauptbestandteil von Computerchips und Solarzellen. Deutschlands Innovationskraft in der Technologiebranche hängt maßgeblich von Silizium ab.
- Sauerstoff (O): Unentbehrlich für die Atmung und viele industrielle Prozesse. Die saubere Luft in Deutschlands Naturgebieten ist ein wichtiger Faktor für die Lebensqualität.
Isotope: Variationen innerhalb eines Elements
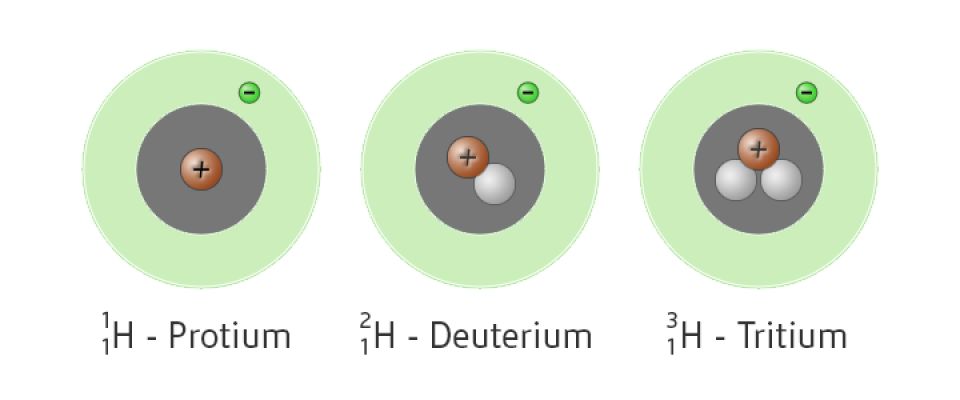
Es gibt eine interessante Wendung: Atome desselben Elements können unterschiedliche Anzahlen von Neutronen im Kern haben. Diese Varianten werden als Isotope bezeichnet. Beispielsweise hat Wasserstoff (ein Proton) drei Isotope:
- Protium: Kein Neutron.
- Deuterium: Ein Neutron.
- Tritium: Zwei Neutronen.
Obwohl Isotope die gleiche Anzahl an Protonen (und damit die gleichen chemischen Eigenschaften) haben, unterscheiden sie sich in ihrer Masse. Einige Isotope sind stabil, während andere radioaktiv sind. Radioaktive Isotope werden in der Medizin, der Archäologie (z.B. zur Altersbestimmung von Funden) und in der Industrie eingesetzt. In Deutschland gibt es zahlreiche Forschungseinrichtungen, die sich mit Isotopenforschung beschäftigen.
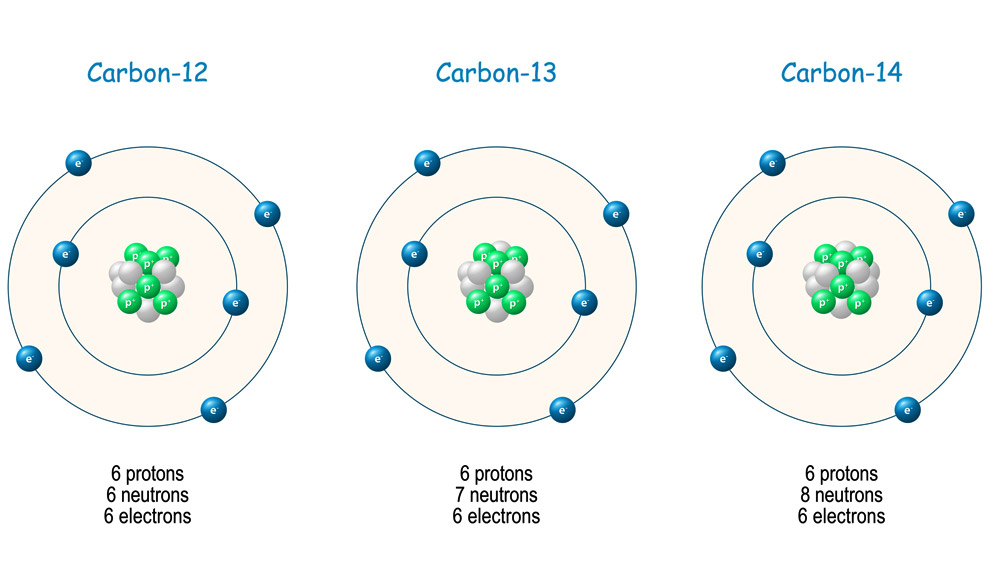
Ein Beispiel: Kohlenstoff-14-Datierung
Ein bekanntes Beispiel für die Anwendung von Isotopen ist die Kohlenstoff-14-Datierung. Kohlenstoff-14 ist ein radioaktives Isotop des Kohlenstoffs. Lebende Organismen nehmen Kohlenstoff-14 aus der Atmosphäre auf. Wenn ein Organismus stirbt, hört er auf, Kohlenstoff-14 aufzunehmen, und die Menge an Kohlenstoff-14 im Organismus nimmt durch radioaktiven Zerfall ab. Wissenschaftler können die Menge an Kohlenstoff-14 in einer Probe messen und so das Alter des Organismus bestimmen. Diese Methode wird häufig verwendet, um archäologische Funde zu datieren und die Geschichte Deutschlands zu rekonstruieren.
Ionen: Wenn Atome elektrisch geladen sind
Atome können auch Elektronen gewinnen oder verlieren. Wenn ein Atom ein Elektron verliert, wird es positiv geladen und wird als Kation bezeichnet. Wenn ein Atom ein Elektron gewinnt, wird es negativ geladen und wird als Anion bezeichnet. Geladene Atome werden als Ionen bezeichnet.
Ionen spielen eine wichtige Rolle in vielen Prozessen, die wir täglich erleben. Beispielsweise sind Natrium- und Chloridionen (Na+ und Cl-) die Hauptbestandteile von Kochsalz (NaCl). Ionen sind auch wichtig für die Funktion von Nerven und Muskeln im menschlichen Körper. In Deutschland werden Ionen in der Chemie, der Medizin und der Materialwissenschaft intensiv erforscht und eingesetzt.
Wichtig zum Merken: Die Anzahl der Protonen bestimmt, um welches Element es sich handelt. Die Anzahl der Neutronen bestimmt, welches Isotop es ist. Der Gewinn oder Verlust von Elektronen erzeugt Ionen.
Warum ist das wichtig für meinen Aufenthalt in Deutschland?
Auch wenn Sie nicht vorhaben, ein Labor zu betreten, ist ein grundlegendes Verständnis von Atomen und Elementen durchaus nützlich, um die Welt um Sie herum besser zu verstehen:
- Architektur und Materialien: Erkennen Sie, welche Elemente in den beeindruckenden Strukturen der deutschen Städte verwendet wurden. Die Stabilität einer Brücke hängt von den Eigenschaften von Eisen und Stahl ab. Die Schönheit eines Glasfensters verdankt sich den chemischen Eigenschaften verschiedener Metalle.
- Umweltbewusstsein: Verstehen Sie die Zusammensetzung der Luft und des Wassers. Wissen über Elemente hilft, Umweltprobleme wie Luftverschmutzung und Wasserqualität besser einzuordnen.
- Technologie: Deutschland ist ein Zentrum für Technologie. Wenn Sie die Rolle von Silizium in Computern und Solarzellen verstehen, können Sie die technologischen Fortschritte des Landes besser wertschätzen.
- Gesundheit und Ernährung: Erkennen Sie die Bedeutung von Mineralien (wie Eisen, Kalzium und Jod) in Ihrer Ernährung. Viele deutsche Produkte sind mit Informationen über ihren Mineralstoffgehalt gekennzeichnet.
Kurz gesagt, ein kleines bisschen Chemie kann Ihnen helfen, Deutschland auf einer tieferen Ebene zu erleben und zu verstehen! Genießen Sie Ihren Aufenthalt und die Entdeckungstour!
Wo kann ich mehr darüber erfahren?
Wenn Sie tiefer in die Welt der Atome und Elemente eintauchen möchten, gibt es zahlreiche Ressourcen:
- Wissenschaftsmuseen: Viele deutsche Städte haben exzellente Wissenschaftsmuseen mit interaktiven Ausstellungen über Chemie und Physik.
- Universitäten: Viele Universitäten bieten öffentliche Vorlesungen und Führungen durch ihre wissenschaftlichen Einrichtungen an.
- Online-Ressourcen: Es gibt unzählige Websites und Videos, die Ihnen die Grundlagen der Chemie erklären.
- Bücher: In jeder gut sortierten Buchhandlung finden Sie Bücher über Chemie für Einsteiger.
Wir hoffen, dieser kleine Ausflug in die Welt der Atome hat Ihnen gefallen! Gute Reise und viel Spaß beim Entdecken Deutschlands!