Aus Was Besteht Ein Atom
Atome sind die grundlegenden Bausteine aller Materie im Universum. Um die Welt um uns herum und ihre Eigenschaften zu verstehen, ist es wichtig zu wissen, woraus ein Atom besteht. Dieser Artikel gibt Ihnen einen klaren und praktischen Überblick über die atomare Struktur.
Die Hauptbestandteile eines Atoms
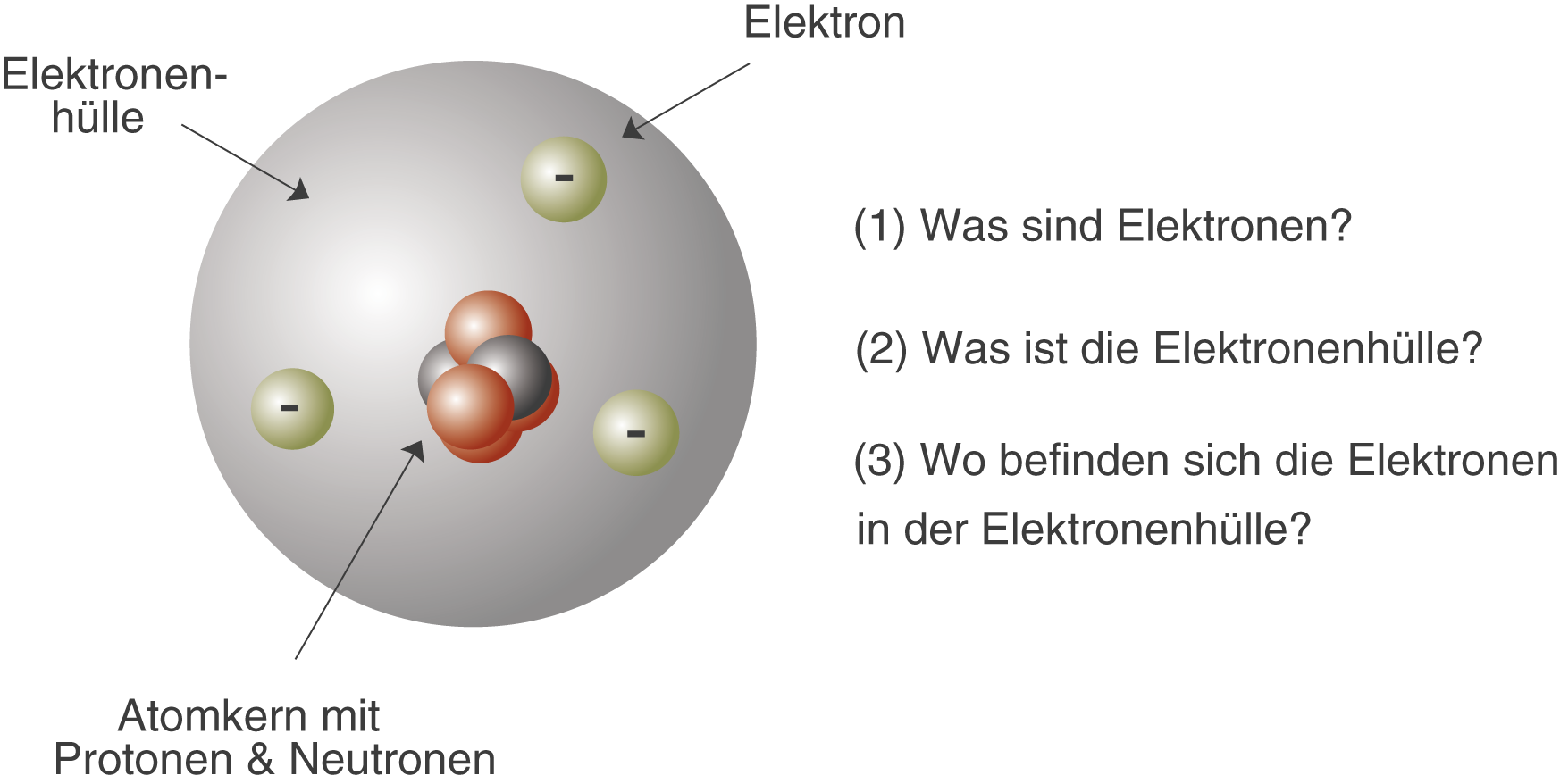
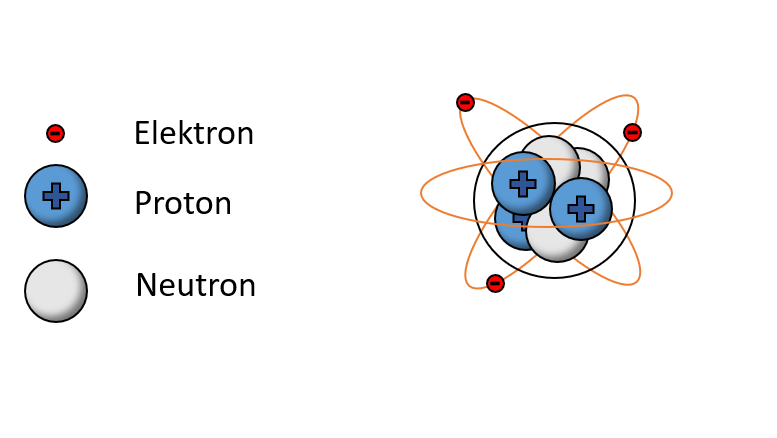
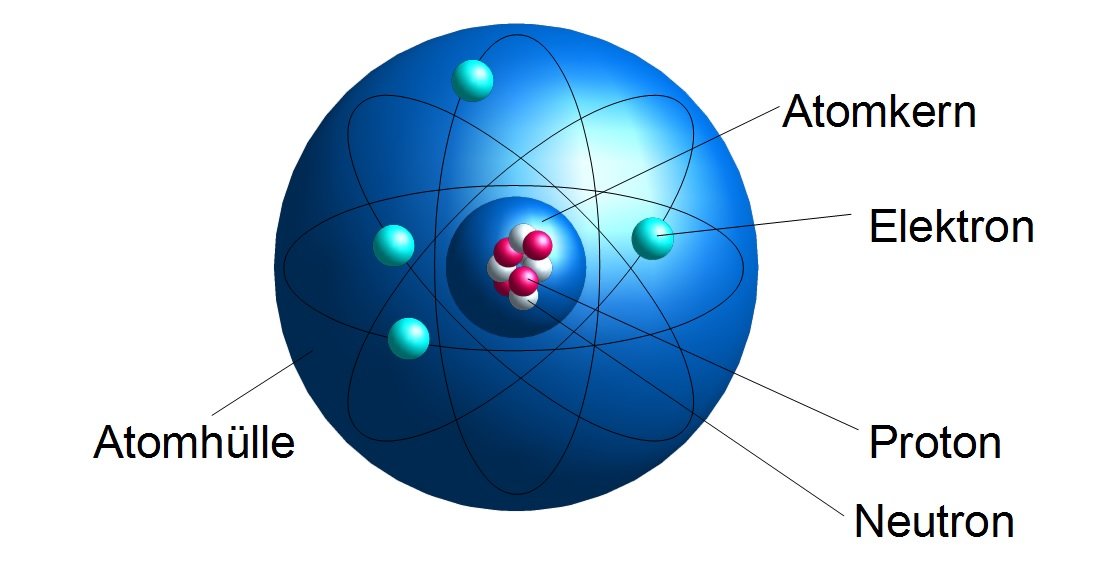
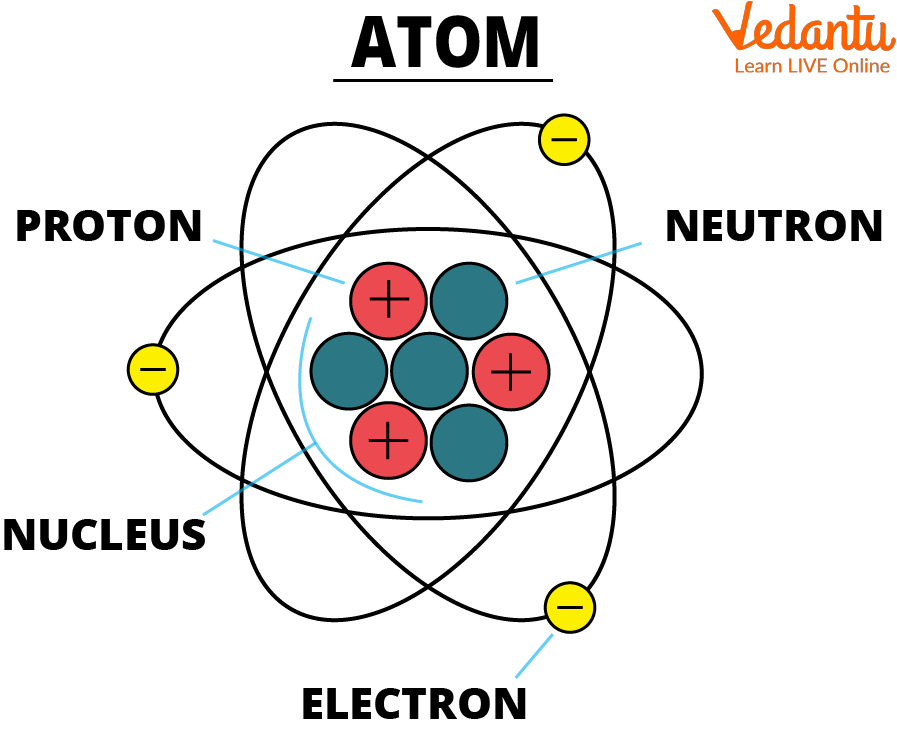
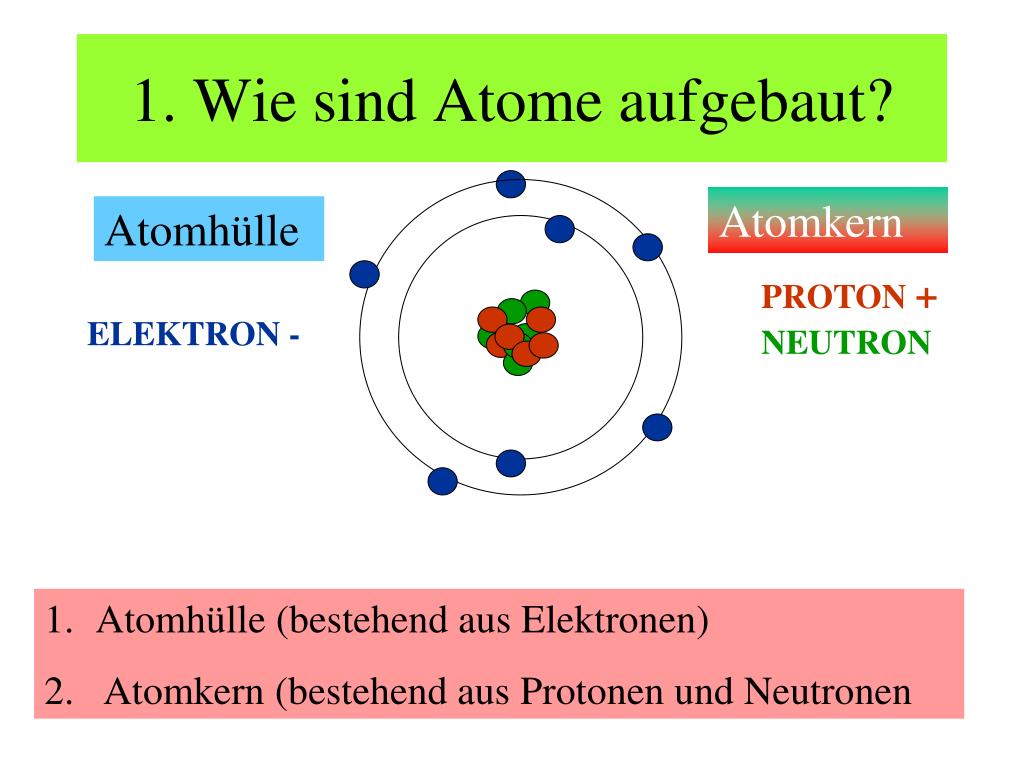
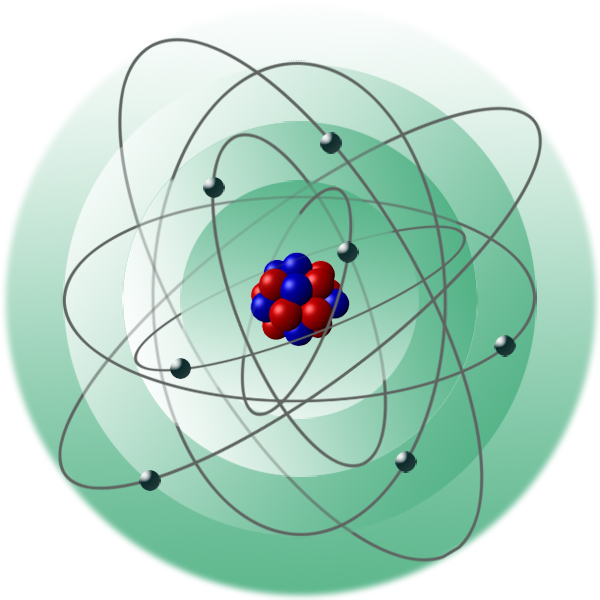
Ein Atom besteht hauptsächlich aus drei Arten von subatomaren Teilchen: Protonen, Neutronen und Elektronen.
Protonen
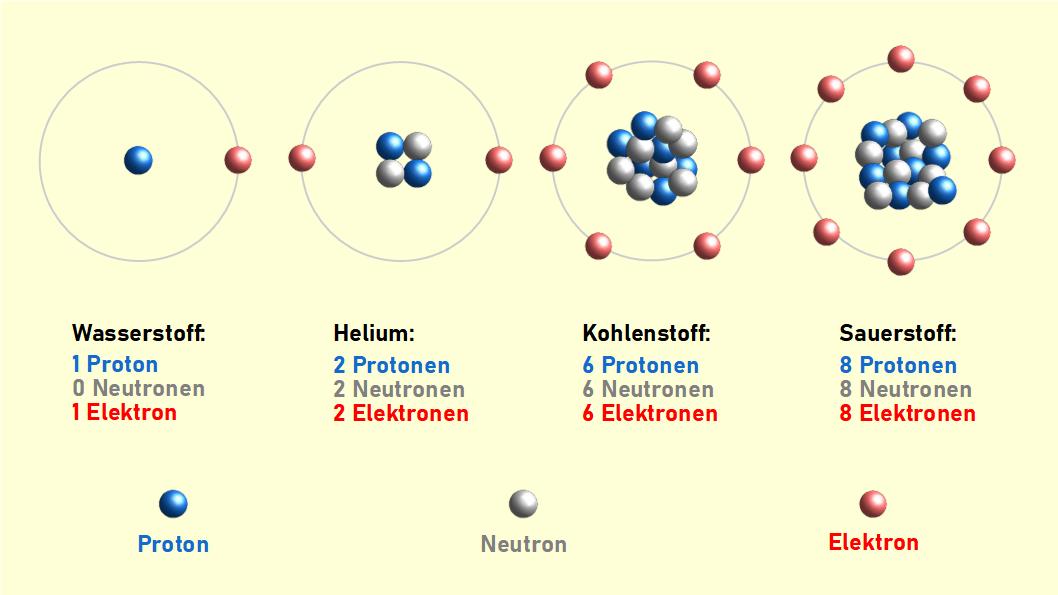
Protonen sind positiv geladene Teilchen, die sich im Kern (auch Nukleus genannt) des Atoms befinden. Die Anzahl der Protonen in einem Atomkern bestimmt, um welches chemische Element es sich handelt. Diese Zahl wird als Atomnummer bezeichnet. Beispielsweise hat jedes Atom des Elements Wasserstoff genau ein Proton, während jedes Atom des Elements Sauerstoff acht Protonen hat.
Neutronen
Neutronen sind elektrisch neutral (d.h. sie haben keine Ladung) und befinden sich ebenfalls im Atomkern. Zusammen mit den Protonen tragen sie zur Masse des Atoms bei. Atome desselben Elements können unterschiedliche Anzahlen von Neutronen haben. Diese Varianten werden Isotope genannt. Beispielsweise gibt es Wasserstoffatome mit null Neutronen (Protium), einem Neutron (Deuterium) und zwei Neutronen (Tritium). Alle sind Wasserstoff, aber mit unterschiedlichen Atommassen.
Elektronen
Elektronen sind negativ geladene Teilchen, die den Atomkern umkreisen. Sie sind viel leichter als Protonen und Neutronen. Elektronen bewegen sich nicht auf festen Bahnen, sondern in Regionen um den Kern, die als Atomorbitale oder Elektronenschalen bezeichnet werden. Diese Orbitale haben unterschiedliche Energieniveaus. Die Anordnung der Elektronen in diesen Schalen bestimmt die chemischen Eigenschaften eines Elements, d.h. wie es mit anderen Atomen interagiert.
Der Atomkern (Nukleus)
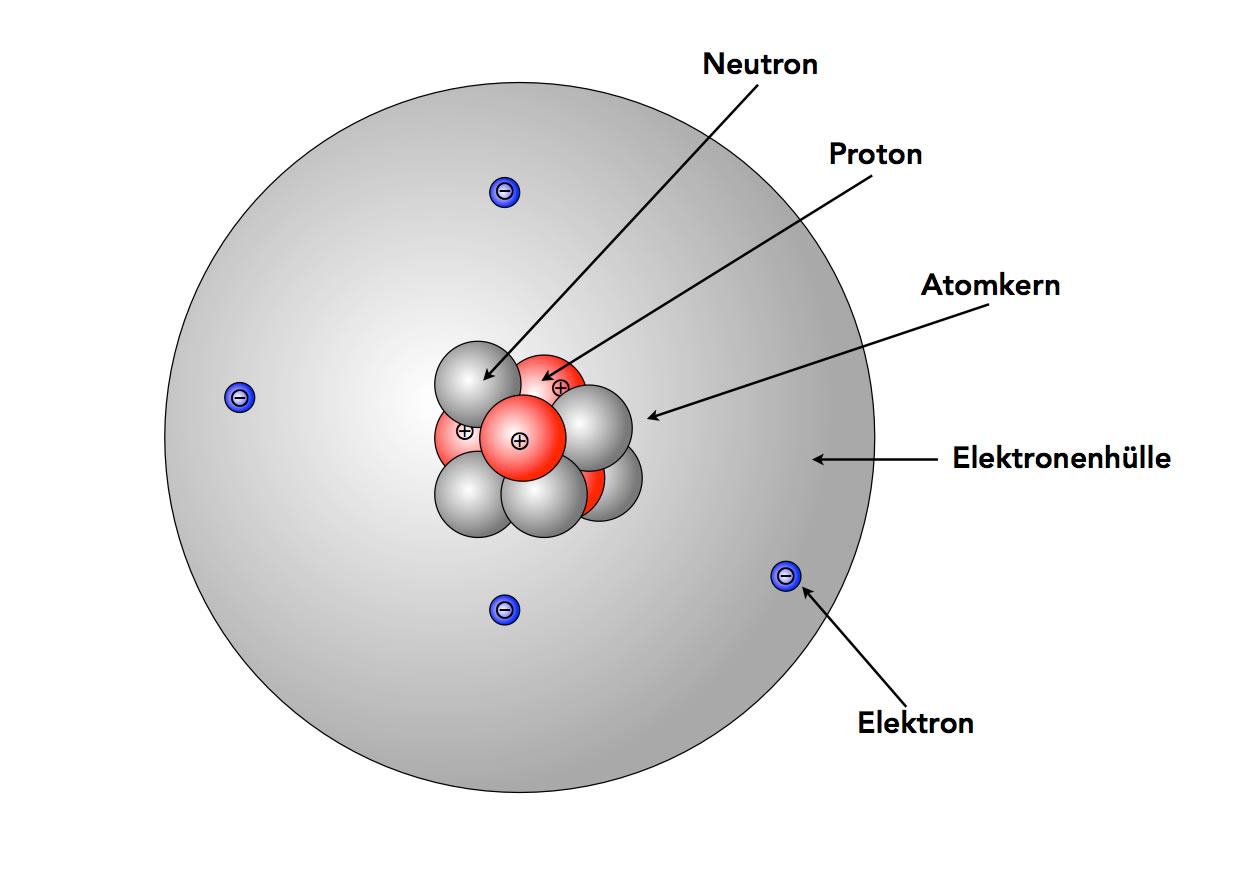
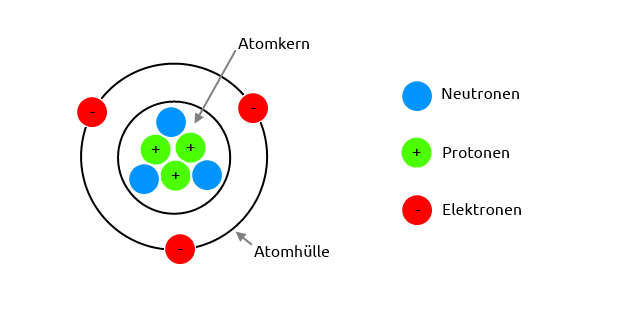
Der Atomkern ist das Zentrum des Atoms und enthält die Protonen und Neutronen. Er macht den größten Teil der Atommasse aus, obwohl er nur einen sehr kleinen Teil des Atomvolumens einnimmt. Die Kräfte, die Protonen und Neutronen im Kern zusammenhalten, sind sehr stark und werden als starke Kernkraft bezeichnet. Ohne diese Kraft würden sich die positiv geladenen Protonen aufgrund ihrer gleichen Ladung abstoßen und der Kern auseinanderfallen.
Elektronenhüllen und Atomorbitale
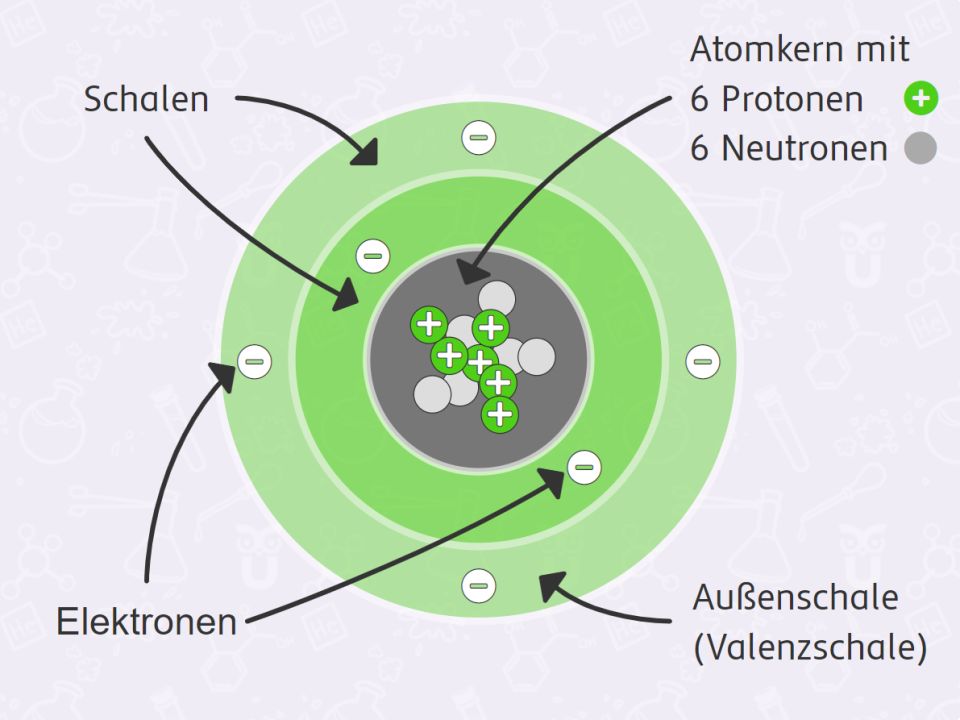
Elektronen umkreisen den Kern in bestimmten Energieniveaus, die als Elektronenschalen oder Hauptquantenzahlen bezeichnet werden. Jede Schale kann nur eine bestimmte Anzahl von Elektronen aufnehmen. Die innerste Schale (die Schale am nächsten zum Kern) kann maximal zwei Elektronen aufnehmen. Die nächste Schale kann bis zu acht Elektronen aufnehmen, und so weiter.
Innerhalb jeder Schale gibt es Atomorbitale. Orbitale sind dreidimensionale Regionen um den Kern, in denen die Wahrscheinlichkeit, ein Elektron zu finden, am höchsten ist. Es gibt verschiedene Arten von Orbitalen, die durch ihre Form gekennzeichnet sind, wie z.B. s-Orbitale (kugelförmig), p-Orbitale (hantelförmig) und d-Orbitale (komplexere Formen). Die Anordnung der Elektronen in diesen Orbitalen bestimmt die chemischen Eigenschaften des Atoms.
Die Elektronenkonfiguration, d.h. die Verteilung der Elektronen auf die verschiedenen Schalen und Orbitale, ist entscheidend für die chemische Reaktivität eines Elements. Atome streben danach, eine stabile Elektronenkonfiguration zu erreichen, typischerweise eine volle äußere Schale. Dies führt dazu, dass Atome Bindungen mit anderen Atomen eingehen, um Elektronen zu teilen oder zu übertragen, was zur Bildung von Molekülen führt.
Ionen: Geladene Atome
Ein Atom ist im Normalzustand elektrisch neutral, d.h. es hat die gleiche Anzahl von Protonen (positive Ladungen) und Elektronen (negative Ladungen). Wenn ein Atom jedoch Elektronen gewinnt oder verliert, wird es zu einem Ion.
- Anionen: Atome, die Elektronen aufnehmen, erhalten eine negative Ladung und werden als Anionen bezeichnet.
- Kationen: Atome, die Elektronen verlieren, erhalten eine positive Ladung und werden als Kationen bezeichnet.
Ionen spielen eine wichtige Rolle in chemischen Reaktionen und der Bildung von ionischen Verbindungen, wie z.B. Kochsalz (Natriumchlorid, NaCl), das aus Natrium-Kationen (Na+) und Chlorid-Anionen (Cl-) besteht.
Masse eines Atoms und Atomgewicht
Die Masse eines Atoms wird hauptsächlich durch die Anzahl der Protonen und Neutronen im Kern bestimmt. Die Masse eines Elektrons ist im Vergleich zu der von Protonen und Neutronen vernachlässigbar. Die Masse von Protonen und Neutronen ist sehr ähnlich, und sie werden beide auf etwa 1 atomare Masseneinheit (amu) festgelegt.
Das Atomgewicht eines Elements ist der gewichtete Durchschnitt der Massen aller natürlich vorkommenden Isotope dieses Elements, wobei die relative Häufigkeit jedes Isotops berücksichtigt wird. Das Atomgewicht wird im Periodensystem der Elemente angegeben.
Zusammenfassung
Hier ist eine kurze Zusammenfassung der wichtigsten Punkte:
- Atome sind die grundlegenden Bausteine aller Materie.
- Sie bestehen aus Protonen (positiv geladen), Neutronen (neutral) und Elektronen (negativ geladen).
- Protonen und Neutronen befinden sich im Atomkern. Die Anzahl der Protonen bestimmt das Element.
- Elektronen umkreisen den Kern in Elektronenschalen und Orbitalen.
- Ionen sind geladene Atome, die durch das Gewinnen oder Verlieren von Elektronen entstehen.
Das Verständnis der atomaren Struktur ist grundlegend für das Verständnis der Chemie und der physikalischen Eigenschaften von Stoffen. Es ermöglicht uns, die Art und Weise zu verstehen, wie Atome miteinander interagieren, um Moleküle und Materialien zu bilden, die die Welt um uns herum ausmachen.
Weiterführende Informationen
Wenn Sie Ihr Wissen über Atome weiter vertiefen möchten, können Sie die folgenden Ressourcen konsultieren:
- Lehrbücher der Chemie: Diese Bücher bieten detaillierte Erklärungen der atomaren Struktur und der chemischen Prinzipien.
- Online-Kurse: Es gibt viele Online-Kurse, die sich mit Chemie und atomarer Struktur befassen.
- Wissenschaftliche Artikel: Suchen Sie nach Artikeln in wissenschaftlichen Fachzeitschriften, um die neuesten Forschungsergebnisse in der Atomphysik und Chemie zu erhalten.
Indem Sie sich mit der atomaren Struktur auseinandersetzen, können Sie die Welt auf einer tieferen Ebene verstehen und die Grundlage für weitere wissenschaftliche Entdeckungen legen.

![Aus Was Besteht Ein Atom Atome einfach erklärt • Was ist ein Atom? · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2021/12/Was-ist-ein-Atom-1024x576.jpg)
![Aus Was Besteht Ein Atom Atome • Atombaustein, Elektronenhülle Atome · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2020/10/WordPress_Bilder_Aufbau-eines-Atoms-1-1024x576.png)





.jpg?1395315221)