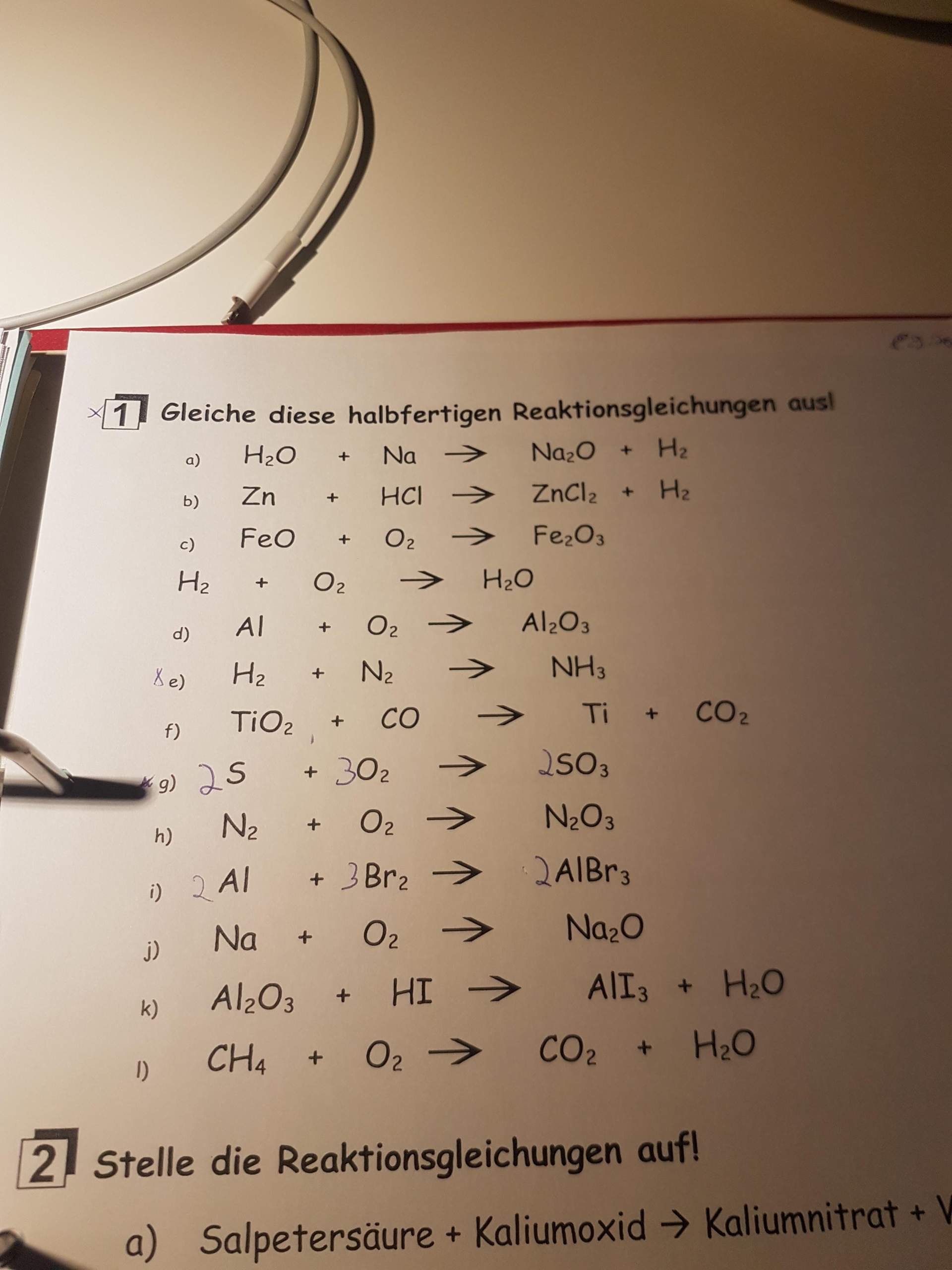
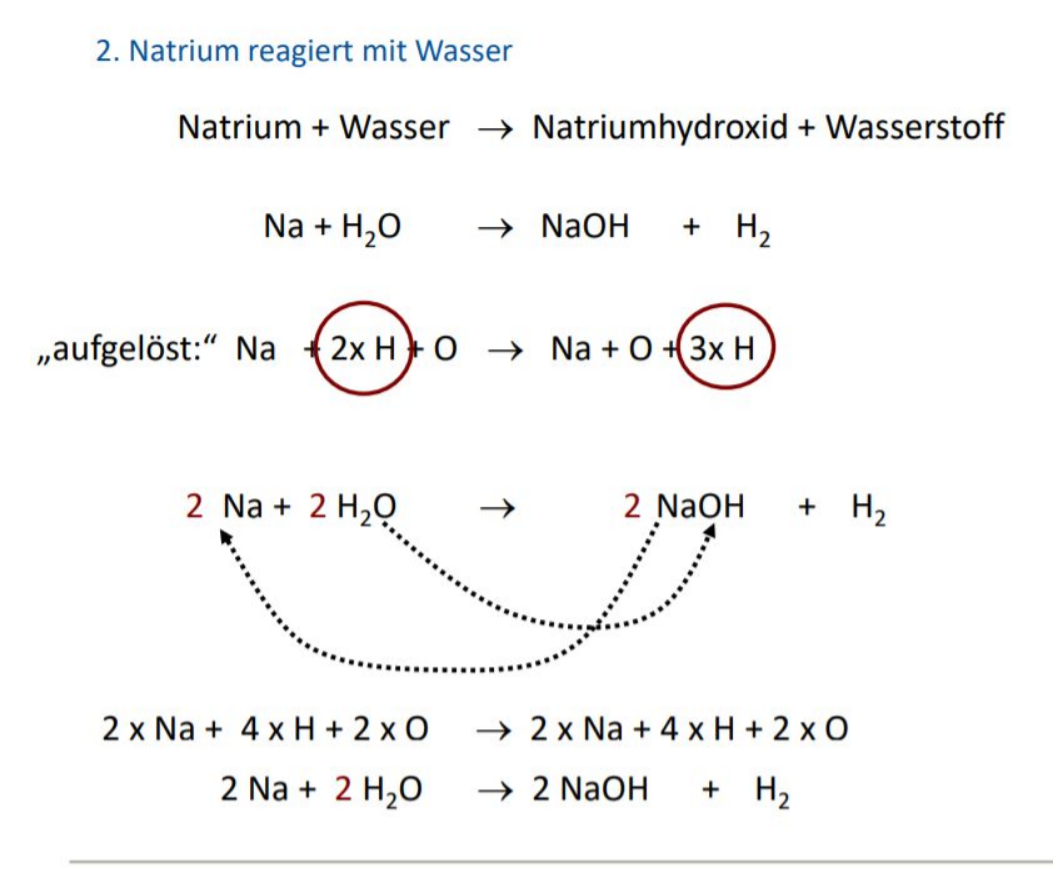
Ausgleichen Von Reaktionsgleichungen übungen

Hey du! Hast du jemals versucht, eine Reaktionsgleichung auszugleichen und dich gefühlt, als ob du versuchst, einen wild gewordenen Hamster in eine winzige Schuhschachtel zu zwängen? Keine Sorge, das geht vielen so! Aber glaub mir, es muss nicht so sein. Es kann sogar... Spaß machen? (Okay, vielleicht ein bisschen Spaß. Oder zumindest befriedigend, wenn man es endlich hinkriegt!)
Stell dir vor, du bist der Chefkoch in einer super-hippen Molekularküche. Deine Aufgabe? Ein perfektes Gericht zu kreieren, bei dem alle Zutaten in der richtigen Menge vorhanden sind. Wenn du zu viel Salz nimmst, ruiniert das den ganzen Teller. Zu wenig Pfeffer und es fehlt der gewisse Kick. Das Ausgleichen von Reaktionsgleichungen ist im Grunde dasselbe, nur dass wir statt Salz und Pfeffer mit Atomen und Molekülen hantieren.
Das große Zählen (und Fluchen… manchmal)
Okay, genug der Metaphern, ran ans Eingemachte! Nehmen wir mal eine einfache Gleichung, die so harmlos aussieht wie ein schlafendes Kätzchen: H2 + O2 → H2O
Wasser, denkst du, kein Problem! Aber warte! Schau genau hin. Auf der linken Seite (den Edukten, den Zutaten quasi) haben wir 2 Wasserstoffatome (H) und 2 Sauerstoffatome (O). Auf der rechten Seite (dem Produkt, dem fertigen Gericht) haben wir zwar immer noch 2 H-Atome, aber nur 1 O-Atom! Skandal! Die Welt geht unter! (Okay, vielleicht nicht die Welt, aber die Gleichung ist definitiv nicht ausgeglichen.)
Die magischen Koeffizienten
Hier kommen die Koeffizienten ins Spiel. Das sind die magischen Zahlen, die wir vor jede chemische Formel schreiben dürfen, um die Anzahl der Atome auszugleichen. Wir dürfen die Formeln selbst nicht verändern (wir können kein H3O erfinden, das wäre ja noch schöner!), sondern nur die Anzahl der Moleküle.
Also, was machen wir? Wir brauchen doppelt so viele Sauerstoffatome auf der rechten Seite. Also schreiben wir eine "2" vor das Wasser (H2O): H2 + O2 → 2 H2O
Juhu! Oder doch nicht? Jetzt haben wir zwar 2 Sauerstoffatome auf beiden Seiten, aber auf der rechten Seite plötzlich 4 Wasserstoffatome! Verflixt und zugenäht! Was nun? Keine Panik! Wir schreiben einfach eine "2" vor den Wasserstoff (H2) auf der linken Seite: 2 H2 + O2 → 2 H2O
TA-DAAAA! Wir haben es geschafft! Auf beiden Seiten haben wir 4 Wasserstoffatome und 2 Sauerstoffatome. Die Gleichung ist ausgeglichen! Wir sind Helden der Chemie! Zeit für eine Siegesrunde!
Übung macht den Meister (und manchmal auch den Wahnsinnigen)
Jetzt, wo du die Grundlagen kennst, ist es Zeit zu üben! Fang mit einfachen Gleichungen an und steigere dich langsam. Glaub mir, je mehr du übst, desto schneller wirst du darin, die Koeffizienten zu finden. Es ist wie ein Puzzle, bei dem jedes Teil (also jedes Atom) an den richtigen Platz muss.
Und wenn du mal gar nicht weiterweißt? Keine Schande! Es gibt unzählige Ressourcen online, die dir helfen können. Oder frag einfach deinen Lehrer oder einen Freund, der sich mit Chemie auskennt. Gemeinsam ist man stark!
Denk daran: Das Ausgleichen von Reaktionsgleichungen ist wie Fahrradfahren lernen. Am Anfang ist es wackelig und man fällt vielleicht ein paar Mal hin, aber irgendwann klappt es wie von selbst. Und wenn du es erstmal kannst, fühlst du dich wie ein echter Chemie-Superstar! Also, schnapp dir einen Bleistift, ein Blatt Papier und leg los! Die Welt der Chemie wartet auf dich!
Wichtiger Hinweis: Hab Geduld! Manche Gleichungen sind kniffliger als andere. Lass dich nicht entmutigen, wenn es nicht sofort klappt. Übung macht den Meister! Und vielleicht hilft es, dabei deine Lieblingsmusik zu hören.
Also, viel Spaß beim Ausgleichen! Und denk dran: Chemie ist nicht nur Wissenschaft, sondern auch ein bisschen Magie. Und du bist der Zauberer!




![Ausgleichen Von Reaktionsgleichungen übungen Reaktionsgleichungen Übungen • ausgleichen, aufstellen · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2022/06/Chemische_Reaktion_Thumbnail-1024x576.png)






![Ausgleichen Von Reaktionsgleichungen übungen Reaktionsgleichung · Reaktionsschema aufstellen · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2020/04/Reaktionsgleichung-Reaktionsschema-1-1024x576.png)