Bronsted Acid And Base

Habt ihr euch jemals gefragt, was passiert, wenn Zitrone mit Backpulver reagiert? Ein sprudelnder Spaß, oder? Aber da steckt mehr dahinter, als nur eine lustige Reaktion. Hier kommen Brønsted-Säuren und Brønsted-Basen ins Spiel! Klingt kompliziert? Keine Sorge, wir machen das ganz locker.
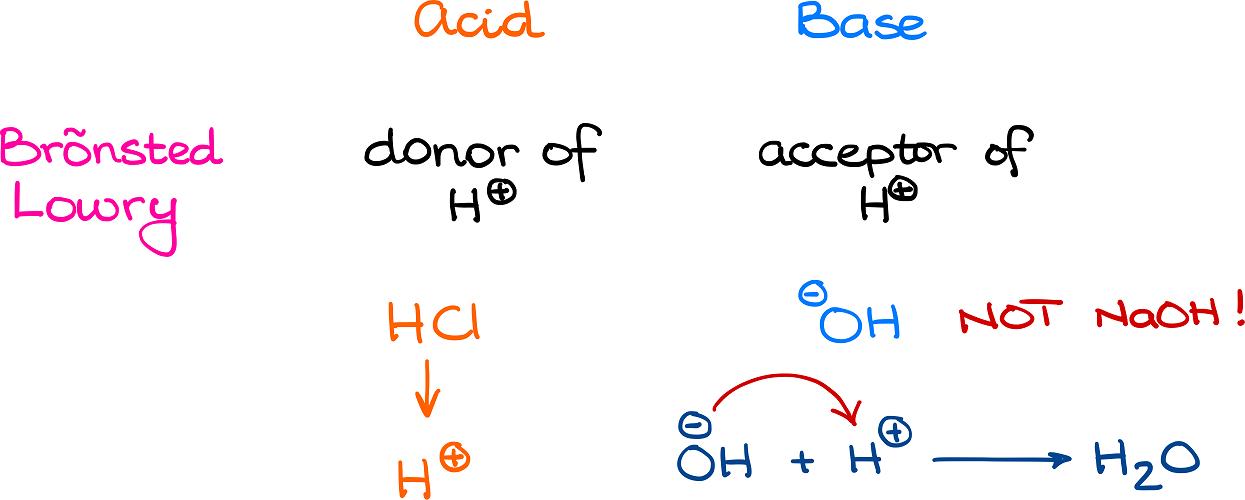
Säuren: Die Protonenspender
Stellt euch eine Säure als einen unglaublich freundlichen Menschen vor, der immer bereit ist, etwas zu geben – in diesem Fall ein Proton! Ein Proton ist im Grunde ein kleines, positiv geladenes Teilchen (ein Wasserstoffion, um genau zu sein). Eine Brønsted-Säure ist also jede Substanz, die ein Proton abgeben kann. Zitrone, Essig, ja sogar eure Magensäure (igitt, aber wichtig!) sind allesamt Beispiele für Säuren. Sie alle haben diesen Drang, Protonen zu verschenken, wie verrückt gewordene Weihnachtsmänner an Heiligabend.
Denkt an Zitronensaft. Er schmeckt sauer, weil die Zitronensäure fleißig Protonen abgibt. Diese Protonen kitzeln dann eure Geschmacksnerven und BAM! Saure Überraschung!
Basen: Die Protonenempfänger
Auf der anderen Seite haben wir die Basen. Sie sind das genaue Gegenteil von Säuren. Sie sind wie kleine Protonenstaubsauger, immer auf der Suche nach einem Proton zum Aufsaugen. Eine Brønsted-Base ist also jede Substanz, die ein Proton aufnehmen kann. Backpulver ist ein tolles Beispiel. Seife, Ammoniak und viele Reinigungsmittel sind ebenfalls Basen. Stellt sie euch als total dankbare Freunde vor, die sich riesig freuen, wenn ihr ihnen etwas schenkt – besonders Protonen!
Backpulver zum Beispiel liebt es, Protonen von Säuren aufzunehmen. Deshalb sprudelt es so schön, wenn ihr es mit Zitronensaft mischt! Die Base (Backpulver) schnappt sich eifrig die Protonen, die die Säure (Zitronensaft) so freigiebig abgibt.
Die große Säure-Base-Party
Was passiert also, wenn wir eine Säure und eine Base zusammenbringen? Eine Neutralisationsreaktion! Es ist wie ein perfekt ausbalanciertes Tanzpaar. Die Säure gibt ihr Proton ab, die Base nimmt es auf, und alle sind glücklich (oder zumindest neutral). Das Ergebnis ist oft Salz und Wasser. So simpel ist das!
Nehmt zum Beispiel die Reaktion von Salzsäure (einer starken Säure) mit Natronlauge (einer starken Base). Die Säure gibt ein Proton ab, die Base nimmt es auf, und heraus kommt Kochsalz (das ihr zum Würzen eures Essens verwendet) und Wasser!
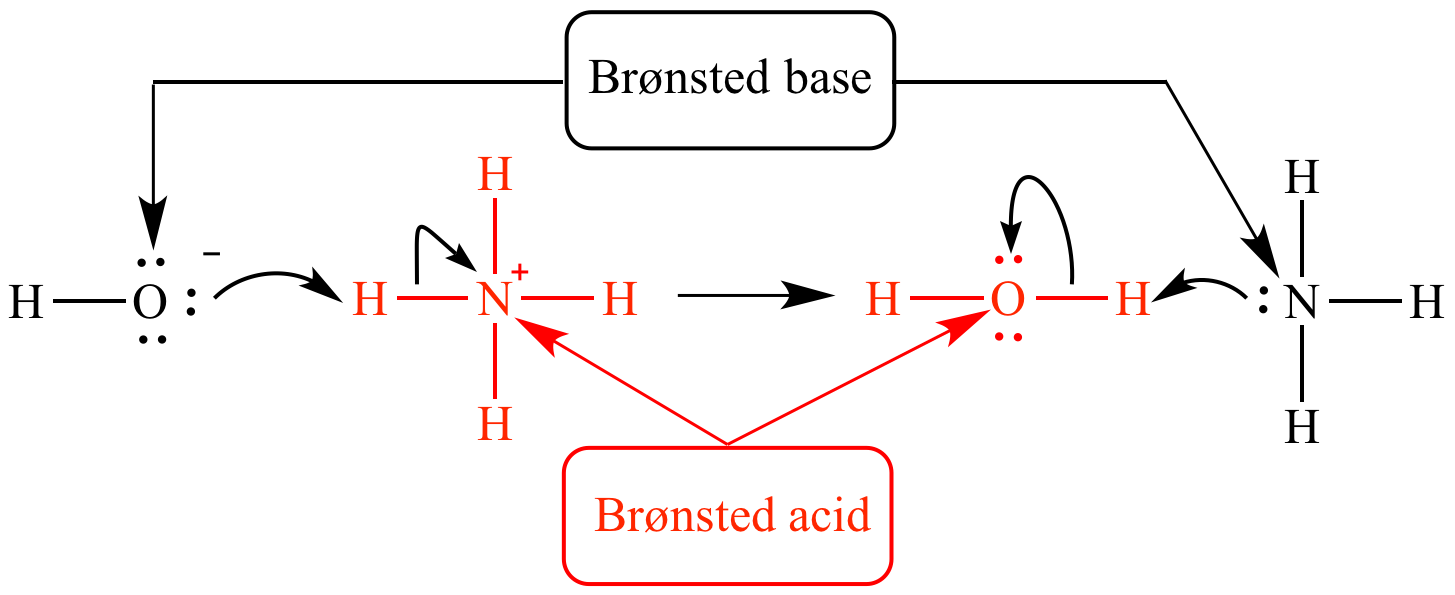
Konjugierte Säure-Base-Paare: Das Buddy-System der Chemie
Jetzt wird es ein bisschen komplizierter, aber keine Panik! Wenn eine Säure ein Proton abgibt, wird sie zu ihrer konjugierten Base. Umgekehrt wird eine Base, wenn sie ein Proton aufnimmt, zu ihrer konjugierten Säure. Es ist wie ein Buddy-System, bei dem jede Säure ihre Base und jede Base ihre Säure hat. Sie sind untrennbar miteinander verbunden.
Denkt an Essigsäure (die Säure in Essig). Wenn sie ein Proton abgibt, wird sie zum Acetat-Ion (ihrer konjugierten Base). Und Ammoniak (eine Base) wird zum Ammonium-Ion (seiner konjugierten Säure), wenn es ein Proton aufnimmt. Sie sind wie Ying und Yang, Tag und Nacht, Säure und Base!
Brønsted-Säuren und -Basen im Alltag
Ihr werdet überrascht sein, wo ihr überall Brønsted-Säuren und Brønsted-Basen begegnet. In eurem Gartenboden, in eurem Körper, in euren Lebensmitteln, sogar in euren Reinigungsmitteln. Sie sind überall! Die Kontrolle des pH-Wertes (der Maß für die Säure oder Basizität einer Lösung) ist in vielen Prozessen unglaublich wichtig, von der Herstellung von Medikamenten bis hin zur Aufrechterhaltung einer gesunden Umwelt.
Das nächste Mal, wenn ihr eine Zitrone auspresst oder Backpulver zum Backen verwendet, denkt daran: Ihr seid Zeuge einer faszinierenden chemischen Reaktion, die auf den Prinzipien der Brønsted-Säure-Base-Theorie beruht. Chemie ist überall, und sie ist überraschend spaßig!
Also, lasst uns die Säuren und Basen feiern – die stillen Helden unseres Alltags! Sie machen die Welt zu einem sprudelnden, neutralisierten und einfach besseren Ort.