Bronsted Theory Of Acid And Base

Säure und Base, das klingt nach Chemieunterricht und Formeln. Aber keine Angst, wir machen es spannend! Heute geht es um eine Idee, die das Verständnis von Säuren und Basen revolutioniert hat: die Brønsted-Theorie.
Stell dir vor, Säuren und Basen sind wie Tanzpartner. Der eine liebt es, ein Teilchen herzugeben, der andere nimmt es gerne an. Total harmonisch, oder? Genau das ist der Kern der Brønsted-Theorie.
Wer war dieser Brønsted überhaupt?
Johannes Nicolaus Brønsted war ein dänischer Chemiker. Klingt erstmal nicht so aufregend, aber warte ab! Er hatte eine geniale Idee, die unser Verständnis von Säuren und Basen für immer verändert hat. Zusammen mit seinem Kollegen Lowry entwickelte er diese Theorie im Jahr 1923. Ein echtes Dreamteam der Chemie!
Das Proton im Mittelpunkt
Was macht die Brønsted-Theorie so besonders? Sie konzentriert sich auf das Proton. Ein Proton ist im Grunde ein Wasserstoffion (H+). Denk dran: ein Wasserstoffatom ohne sein Elektron. Super klein und positiv geladen.
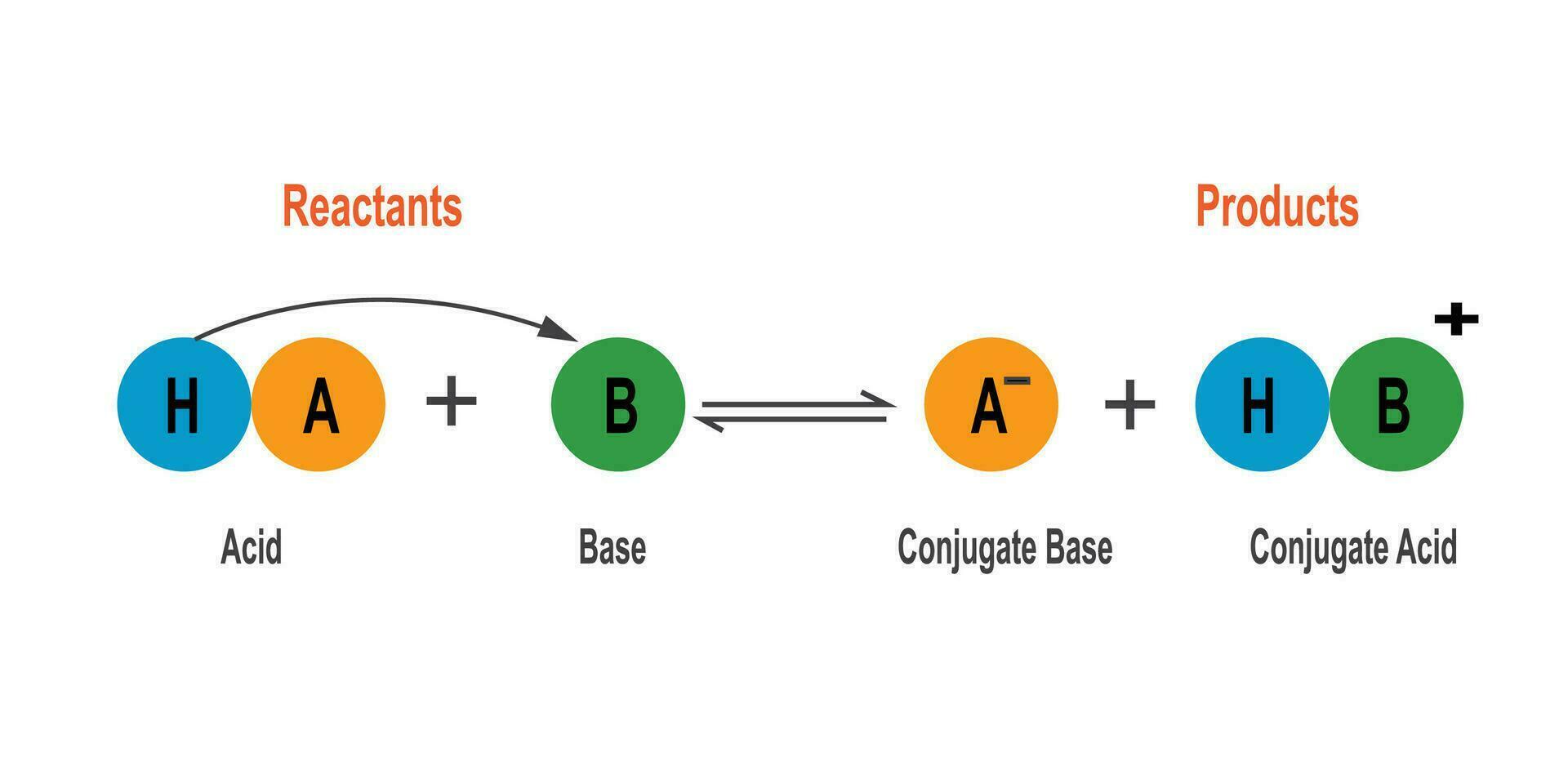
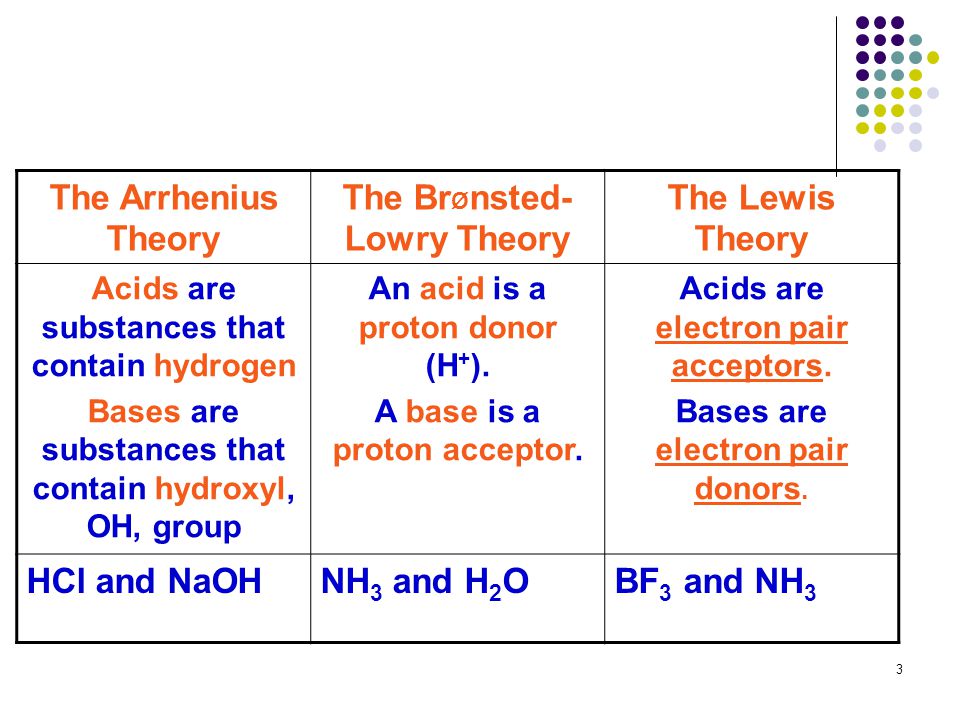
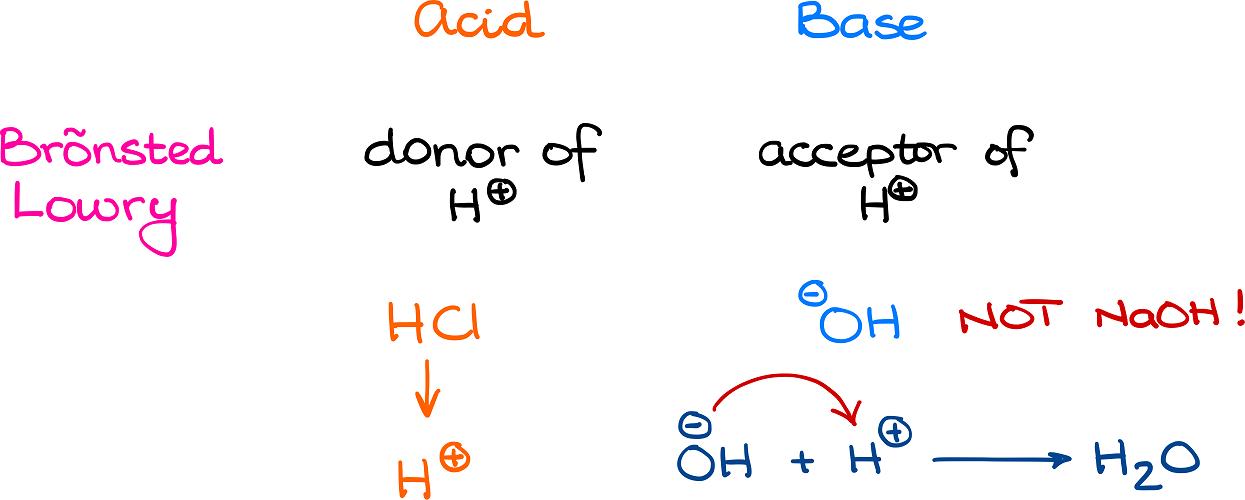
Die Brønsted-Theorie sagt: Eine Säure ist ein Stoff, der Protonen abgeben kann, ein sogenannter Protonendonator. Eine Base ist ein Stoff, der Protonen aufnehmen kann, ein Protonenakzeptor. Ganz einfach, oder?
"Säuren sind Protonendonatoren, Basen sind Protonenakzeptoren."
Das ist wie beim Ballspielen: Die Säure wirft den Ball (das Proton), und die Base fängt ihn auf. So entsteht eine chemische Reaktion. Und das ist das Schöne an der Brønsted-Theorie: Sie erklärt, wie Säuren und Basen miteinander reagieren!
Säure und Base, ein ewiges Hin und Her
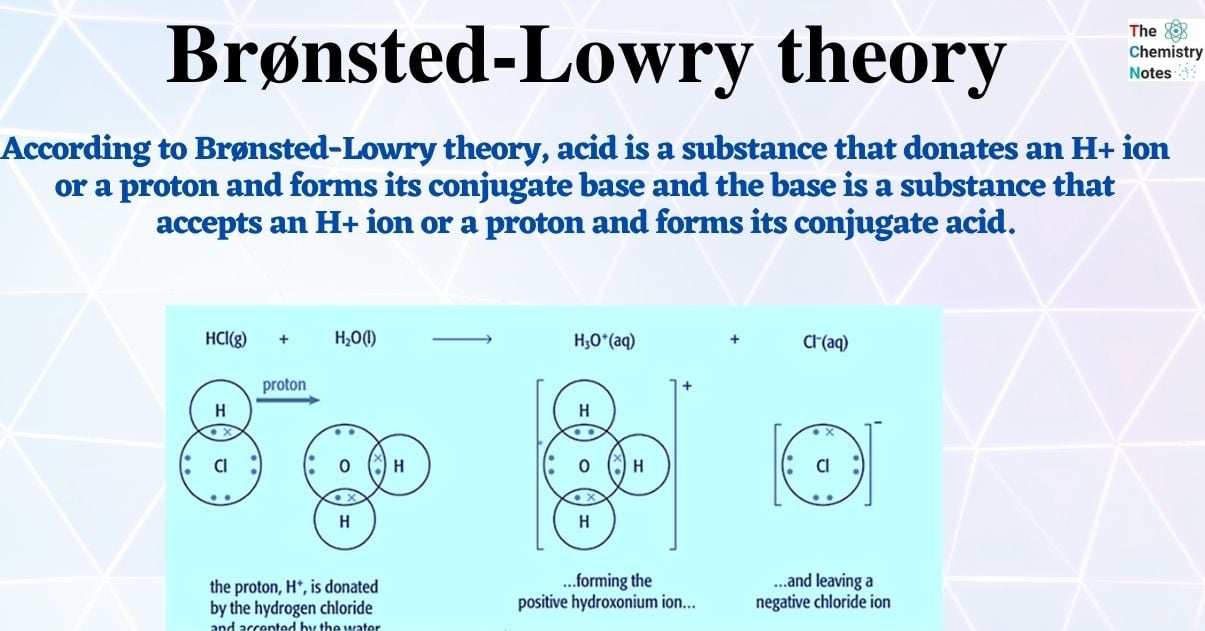
Nehmen wir ein Beispiel: Salzsäure (HCl) in Wasser (H2O). Die Salzsäure gibt ein Proton an das Wasser ab. HCl wird zur Chlorid-Ion (Cl-), und das Wasser wird zum Hydronium-Ion (H3O+). Die Salzsäure ist hier die Säure, weil sie das Proton abgibt. Das Wasser ist die Base, weil es das Proton aufnimmt.
Aber jetzt kommt der Clou: Das Chlorid-Ion (Cl-) kann theoretisch ein Proton aufnehmen, um wieder zu HCl zu werden. Und das Hydronium-Ion (H3O+) kann ein Proton abgeben, um wieder zu Wasser (H2O) zu werden. Das bedeutet, dass sie sich wie ein Team ergänzen. Genial, oder?
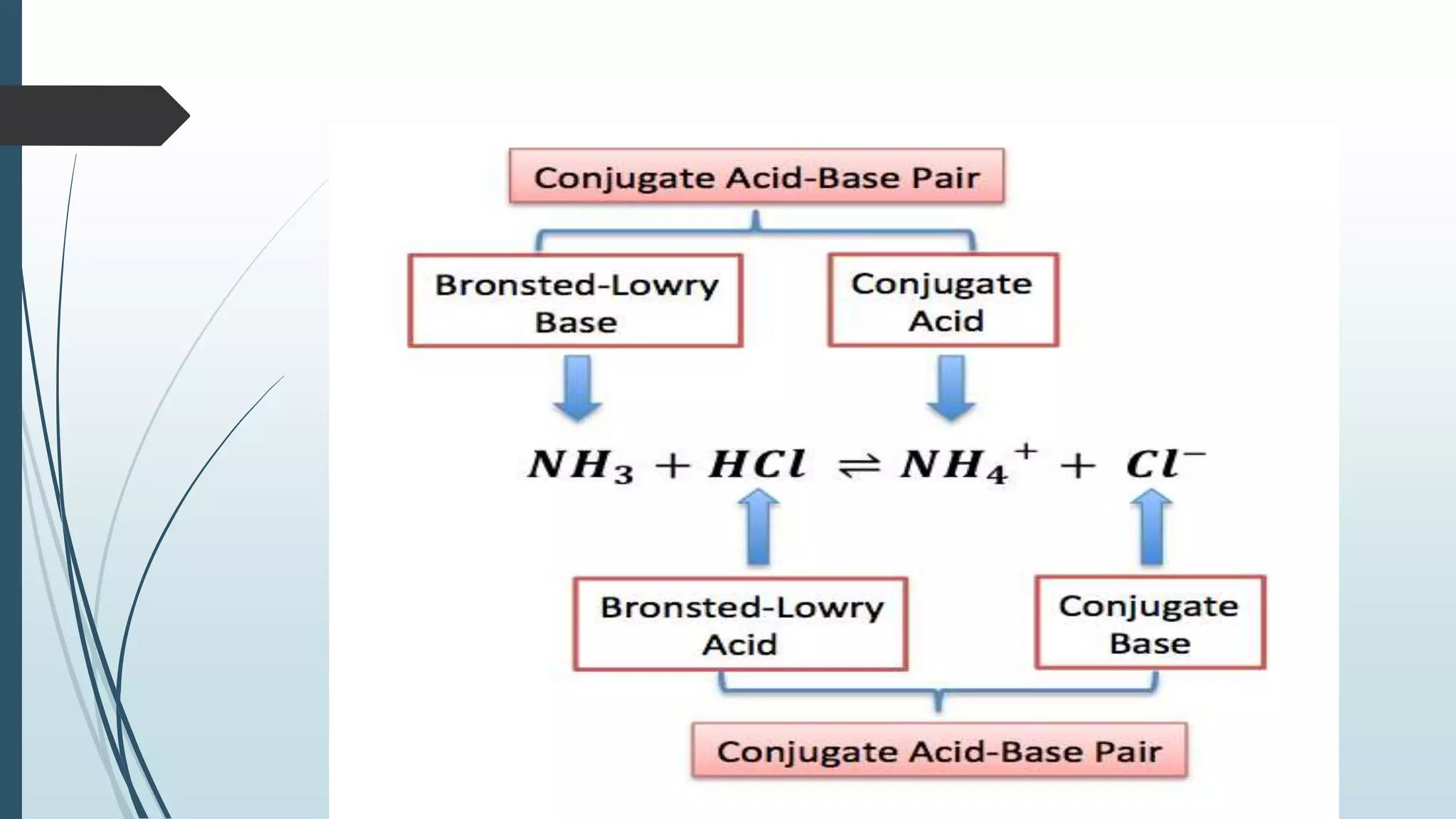
Diese Paare nennt man konjugierte Säure-Base-Paare. Das Chlorid-Ion (Cl-) ist die konjugierte Base der Salzsäure (HCl). Und das Hydronium-Ion (H3O+) ist die konjugierte Säure des Wassers (H2O).
Ampholyte: Die Chamäleons der Chemie
Und es wird noch interessanter! Manche Stoffe können sowohl als Säure als auch als Base reagieren. Das nennt man Ampholyte. Wasser ist das beste Beispiel dafür. Wasser kann ein Proton aufnehmen (und zur Säure werden) oder ein Proton abgeben (und zur Base werden). Ein echter Alleskönner!
Warum ist die Brønsted-Theorie so wichtig?
Die Brønsted-Theorie ist viel breiter anwendbar als ältere Definitionen von Säuren und Basen. Sie erklärt, warum bestimmte Stoffe sauer oder basisch reagieren, selbst wenn keine Hydroxid-Ionen (OH-) im Spiel sind. Das macht sie zu einem unverzichtbaren Werkzeug für Chemiker.
Sie hilft uns zu verstehen, wie chemische Reaktionen ablaufen, wie wir pH-Werte messen und wie wir chemische Prozesse steuern können. Kurz gesagt: Die Brønsted-Theorie ist ein Schlüssel zum Verständnis der Chemie!
Ob in der Medizin, der Landwirtschaft oder der Industrie - die Brønsted-Theorie spielt überall eine wichtige Rolle. Sie hilft uns, Medikamente zu entwickeln, Düngemittel herzustellen und chemische Prozesse zu optimieren.
Die Brønsted-Theorie ist wie ein Detektiv, der uns hilft, die Geheimnisse der chemischen Welt zu entschlüsseln. Sie ist ein faszinierendes Konzept, das uns die Augen für die Schönheit und Komplexität der Chemie öffnet. Also, worauf wartest du noch? Tauche ein in die Welt der Säuren und Basen und lass dich von der Brønsted-Theorie begeistern!
Also, schnapp dir dein (virtuelles) Laborbuch und fang an zu experimentieren! Die Welt der Säuren und Basen wartet darauf, von dir entdeckt zu werden. Und denk dran: Chemie ist nicht nur ein Fach in der Schule, sondern ein spannendes Abenteuer!