Chemische Einheit Der Stoffmenge
.jpg?1394457633)
Habt ihr euch jemals gefragt, wie man eigentlich zählt, wenn es um winzigste Dinge geht? Also, nicht Ameisen im Garten (die sind schon schwer genug!), sondern Atome und Moleküle, die Bausteine von allem um uns herum? Das ist nämlich gar nicht so einfach, wie man denkt. Stell dir vor, du sollst alle Reiskörner in einem riesigen Silo zählen. Klingt spaßig, oder? Eher nicht! Aber genau vor so einer Herausforderung stehen Chemiker ständig.
Die magische Zahl: Eine Handvoll ist nicht genug
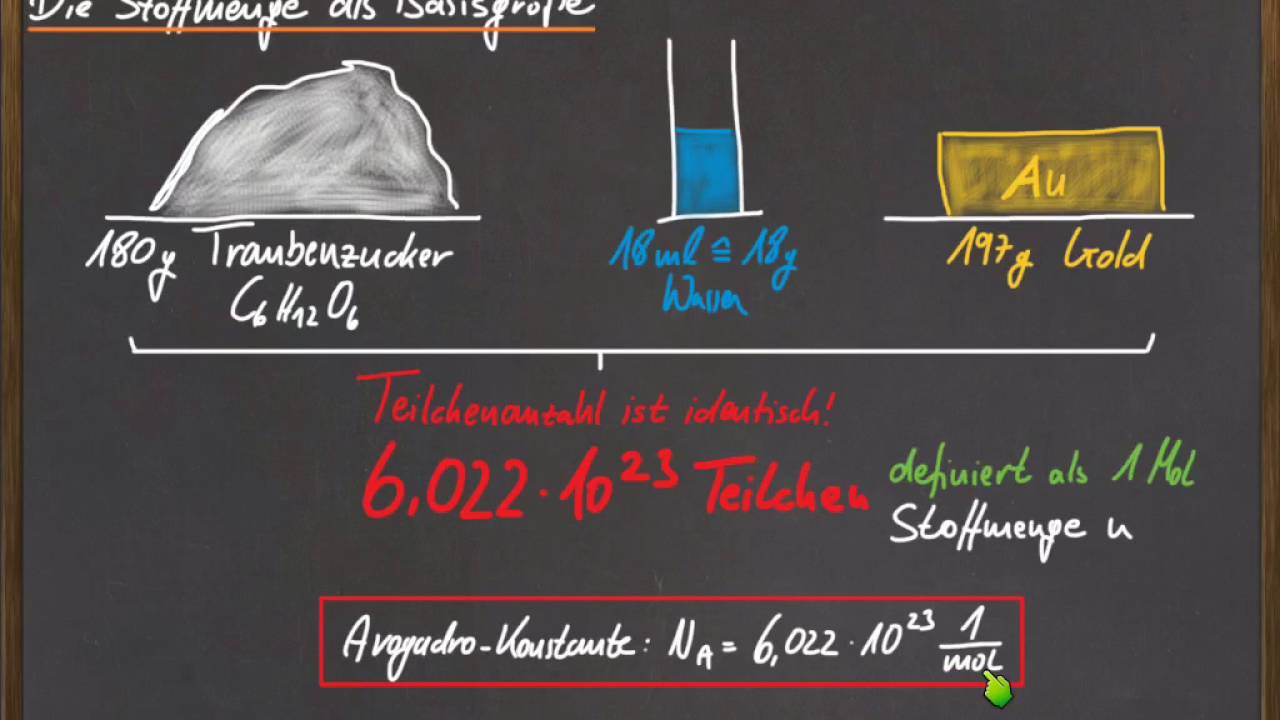
Hier kommt eine ziemlich clevere Lösung ins Spiel: die Stoffmenge, gemessen in der Einheit Mol. Was zur Hölle ist ein Mol, fragt ihr euch jetzt vielleicht? Keine Sorge, es ist nicht so kompliziert. Stell dir vor, ein Mol ist wie ein Rucksack. In diesen Rucksack packst du immer eine ganz bestimmte Anzahl von Dingen rein. Und zwar eine verdammt große Anzahl! Genauer gesagt, 6,022 x 1023 Teilchen. Das ist eine Zahl mit 23 Nullen! Diese gigantische Zahl nennt man die Avogadro-Konstante, benannt nach dem italienischen Wissenschaftler Amedeo Avogadro. Ich wette, er hätte nie gedacht, dass seine Arbeit mal so cool wird!
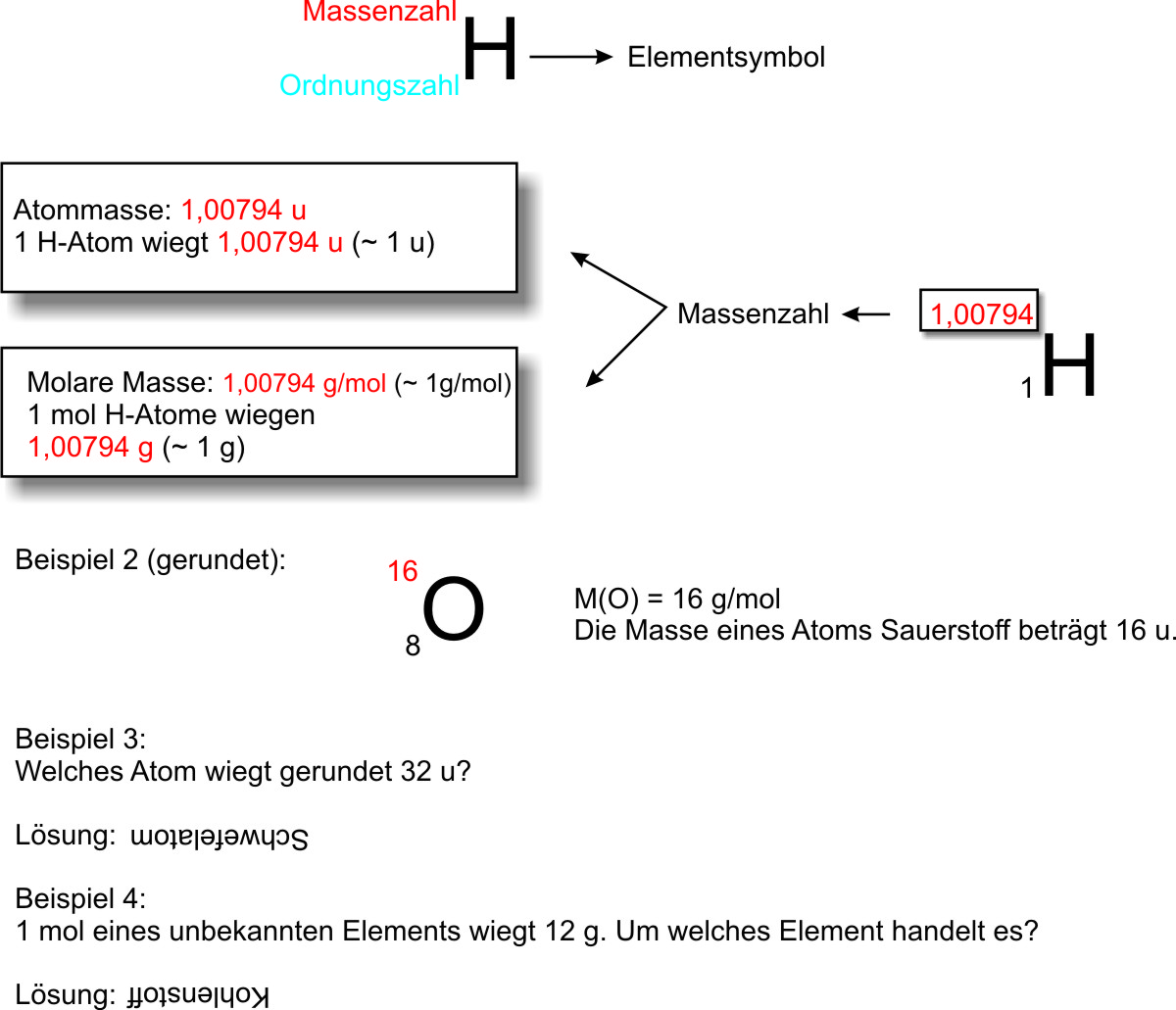
Warum aber gerade diese Zahl? Nun, sie ist so gewählt, dass ein Mol eines Stoffes immer eine Masse in Gramm hat, die dem Atomgewicht (oder Molekulargewicht) des Stoffes in atomaren Masseneinheiten (u) entspricht. Klingt kompliziert, ist aber eigentlich genial einfach. Ein Mol Kohlenstoff wiegt beispielsweise 12 Gramm, weil ein Kohlenstoffatom ungefähr 12 u wiegt. Ein Mol Wasser wiegt 18 Gramm (ca. 2 kleine Schnapsgläser voll), weil ein Wassermolekül ungefähr 18 u wiegt. So können Chemiker Stoffe wiegen und wissen trotzdem, wie viele Teilchen sie haben!
Das Mol im Alltag: Mehr als nur Chemie
Okay, genug Theorie. Was bringt uns das Mol im Alltag? Eine ganze Menge! Denk mal an die Backstube. Ein Bäcker mischt Zutaten in bestimmten Verhältnissen, um das perfekte Brot zu backen. Chemiker machen im Prinzip dasselbe, nur mit Atomen und Molekülen. Sie nutzen das Mol, um die richtigen Mengen an Reaktanten für eine chemische Reaktion zu bestimmen. Wenn du also ein Medikament nimmst, kannst du dir sicher sein, dass die Dosis genau berechnet wurde, dank des Mols!
Und es wird noch besser! Stell dir vor, du willst eine Party für alle Menschen auf der Erde schmeißen. Du bräuchtest ungefähr 12 M Mol Sandwiches, wenn jeder Mensch ein Sandwich isst. Das wäre ganz schön viel Sand! Zum Glück müsstest du das nicht alleine zubereiten!
Hier noch ein paar lustige Fakten zum Thema Mol: Wenn wir ein Mol Murmeln hätten, würde das Volumen aller Murmeln ungefähr dem der Erde entsprechen! Und wenn wir ein Mol Dollar hätten, könnten wir jedem Menschen auf der Erde mehr als eine Billion Dollar geben!
Das Mol: Ein super Werkzeug, nicht nur für Wissenschaftler
Das Mol ist also viel mehr als nur eine obskure Einheit im Chemieunterricht. Es ist ein unglaublich nützliches Werkzeug, um die Welt der winzigsten Dinge zu verstehen und zu manipulieren. Es ermöglicht uns, Reaktionen zu steuern, Medikamente zu entwickeln und neue Materialien zu erschaffen. Und das alles, weil wir eine clevere Art gefunden haben, unvorstellbar große Mengen von Teilchen zu zählen!
Also, das nächste Mal, wenn du von der Stoffmenge hörst, denk daran: Es ist nicht nur eine abstrakte Zahl, sondern der Schlüssel zu einem tiefen Verständnis der Materie und der Welt um uns herum. Und wer weiß, vielleicht inspiriert dich das Mol ja auch zu neuen, grandiosen Ideen! Vielleicht erfindest du ja die nächste bahnbrechende Technologie, die auf den Prinzipien der Chemie basiert. Die Möglichkeiten sind grenzenlos! Und wer weiss, vielleicht schreibst du dann einen Artikel über *deine* Entdeckung... und verwendest das Mol, um sie zu erklären.
Denkt daran, dass die ganze Welt aus Atomen besteht und die Stoffmenge uns ermöglicht, diese zu verstehen und zu manipulieren. Und das ist ziemlich cool, findet ihr nicht?
"Das Mol ist der Freund des Chemikers." - Ein weiser Chemiker (wahrscheinlich)









![Chemische Einheit Der Stoffmenge Stoffmenge berechnen • Stoffmenge Formel und Rechenbeispiel · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2022/05/Thumbnail_Stoffmengenkonzentration-1024x576.png)