Diffusion Und Osmose Einfach Erklärt

Diffusion und Osmose sind zwei grundlegende physikalische Prozesse, die in der Natur allgegenwärtig sind und eine entscheidende Rolle in vielen biologischen Systemen spielen. Sie beeinflussen, wie Nährstoffe in Zellen gelangen, wie Abfallprodukte entfernt werden und wie Pflanzen Wasser aufnehmen. Obwohl sie miteinander verwandt sind, gibt es wichtige Unterschiede zwischen den beiden Prozessen.
Diffusion einfach erklärt
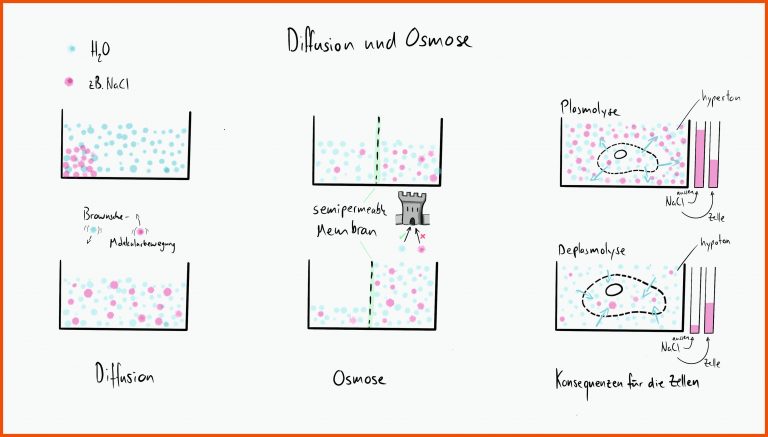
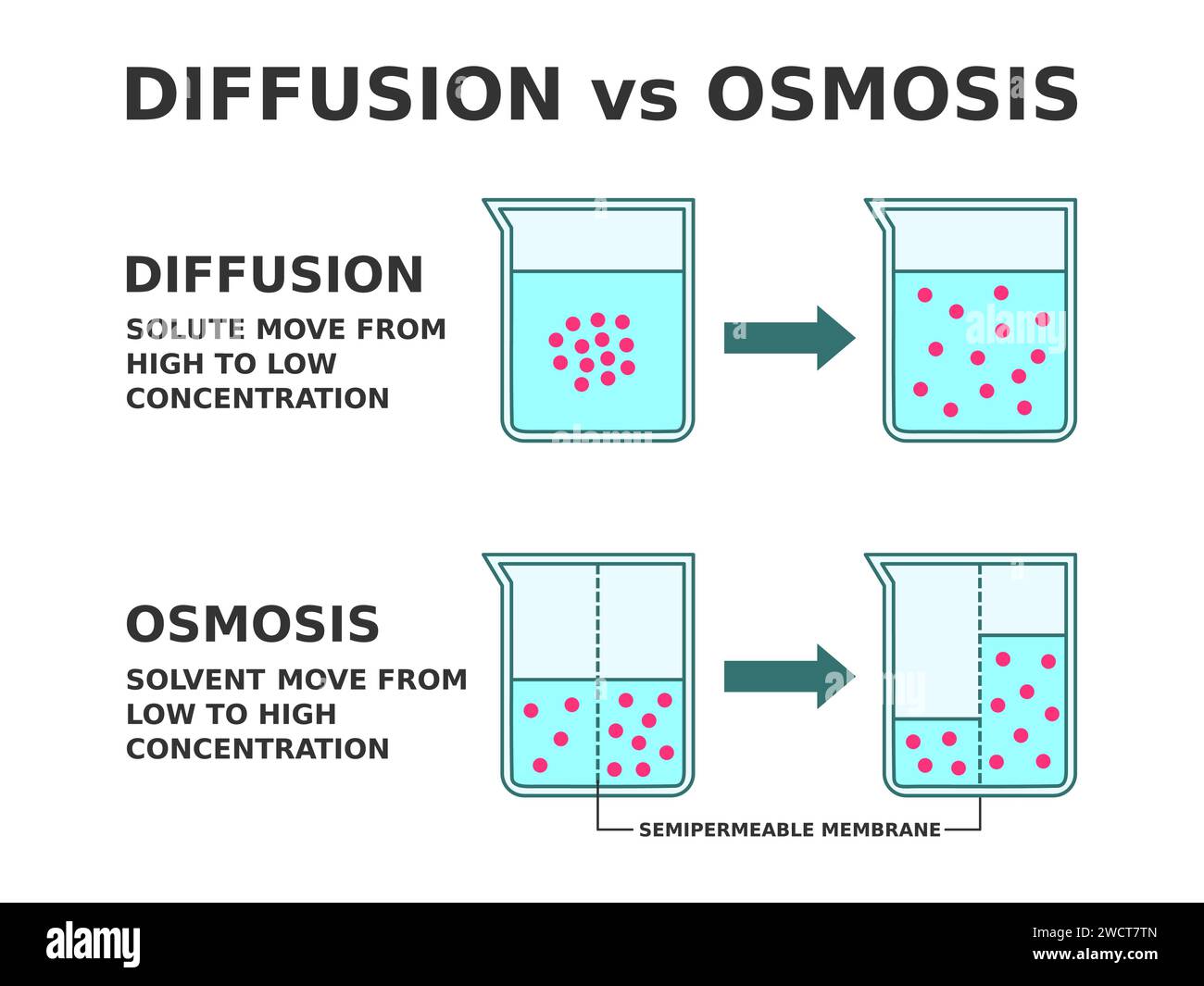
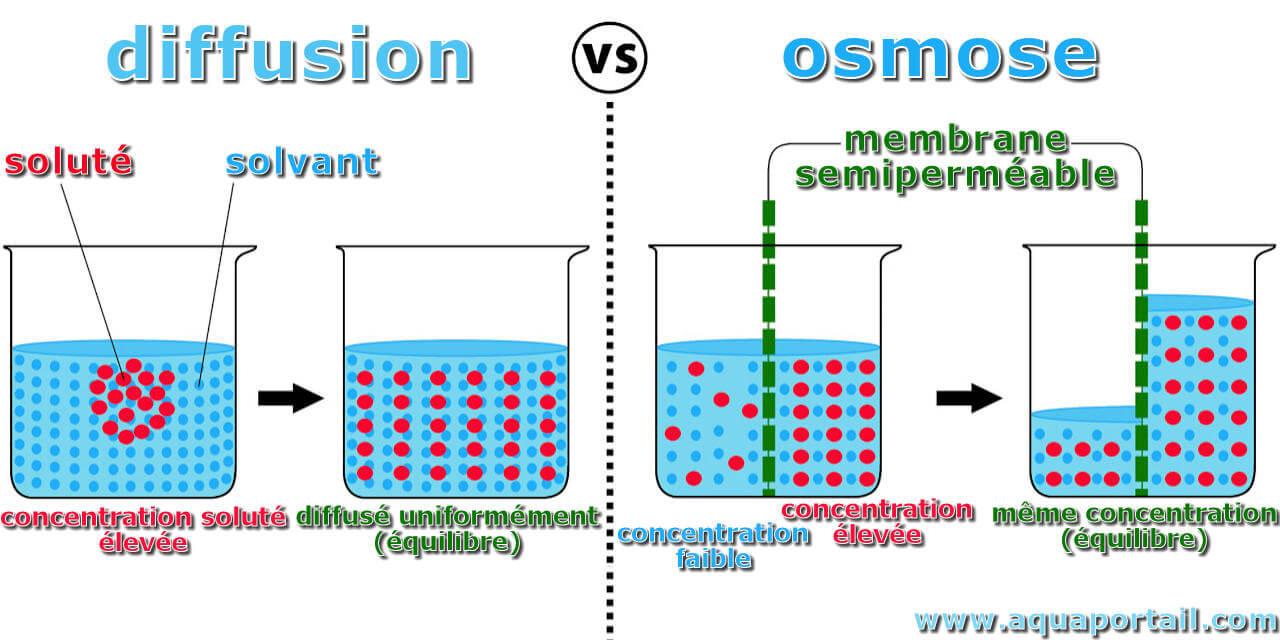
Diffusion beschreibt die Bewegung von Teilchen (Atomen, Ionen, Molekülen) von einem Bereich hoher Konzentration zu einem Bereich niedriger Konzentration. Dieser Prozess wird durch die zufällige thermische Bewegung der Teilchen angetrieben, die als Brownsche Bewegung bekannt ist. Stell dir vor, du versprühst ein Deodorant in einer Ecke eines Raumes. Nach einer Weile riecht es im ganzen Raum. Das liegt daran, dass die Duftmoleküle sich durch Diffusion von dem Bereich hoher Konzentration (dem Ort des Versprühens) in den Bereich niedriger Konzentration (den Rest des Raumes) bewegen, bis sie sich gleichmäßig verteilt haben.
Die treibende Kraft der Diffusion
Die treibende Kraft der Diffusion ist der Konzentrationsgradient, also der Unterschied in der Konzentration zwischen zwei Bereichen. Je größer der Konzentrationsgradient, desto schneller die Diffusion. Die Teilchen "wandern" von selbst, ohne dass Energie von außen zugeführt werden muss. Diffusion ist also ein passiver Transportprozess. Andere Faktoren, die die Diffusionsgeschwindigkeit beeinflussen, sind:
- Temperatur: Höhere Temperaturen bedeuten schnellere Teilchenbewegung und somit schnellere Diffusion.
- Größe der Teilchen: Kleinere Teilchen diffundieren schneller als größere.
- Medium: Diffusion in Gasen ist schneller als in Flüssigkeiten, und in Flüssigkeiten schneller als in Feststoffen. Die Viskosität des Mediums spielt ebenfalls eine Rolle.
Beispiele für Diffusion
- Gasaustausch in der Lunge: Sauerstoff diffundiert aus der Lunge ins Blut, während Kohlendioxid aus dem Blut in die Lunge diffundiert.
- Aufnahme von Nährstoffen im Darm: Verdaute Nährstoffe diffundieren durch die Darmwand ins Blut.
- Verteilung von Duftstoffen: Wie bereits erwähnt, die Ausbreitung von Duftstoffen im Raum.
- Vermischung von Farbstoffen in Wasser: Wenn du Tinte in ein Glas Wasser gibst, verteilt sich die Farbe durch Diffusion im gesamten Wasser.
Osmose einfach erklärt
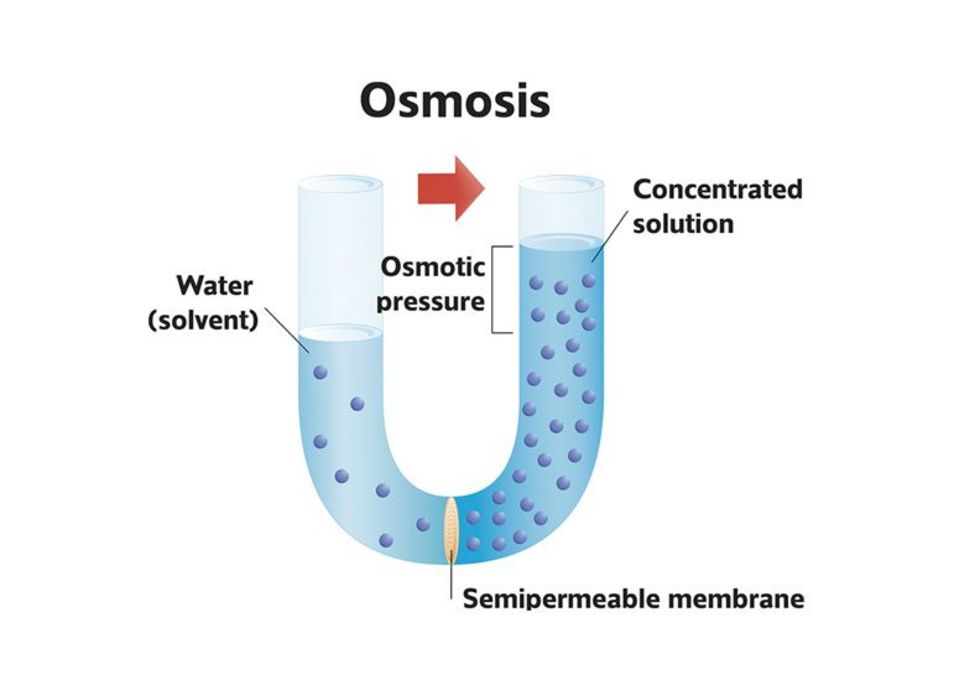
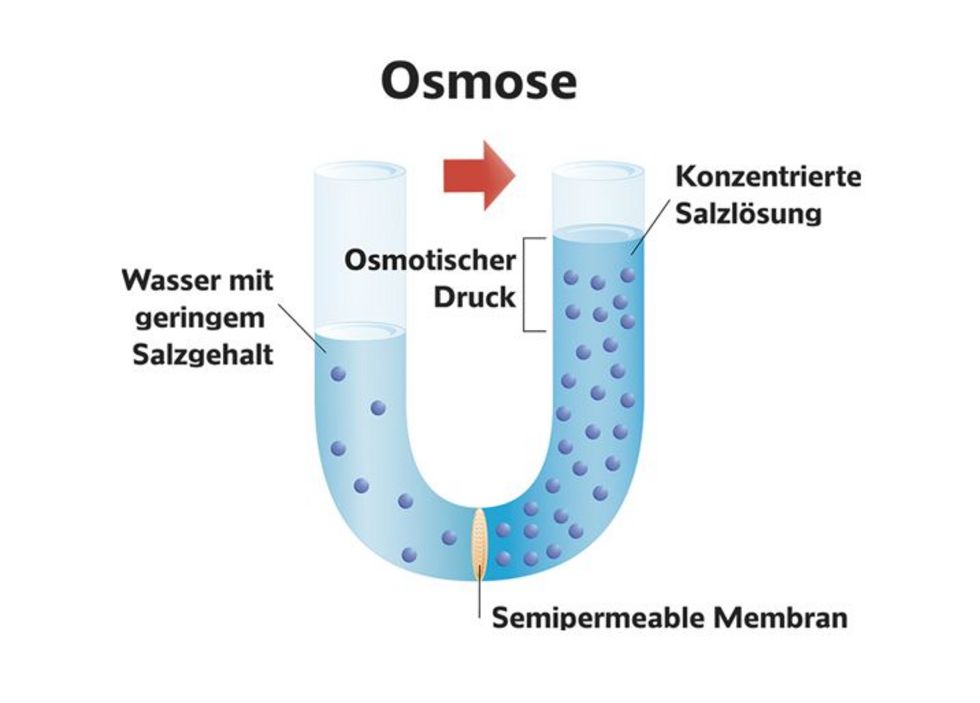
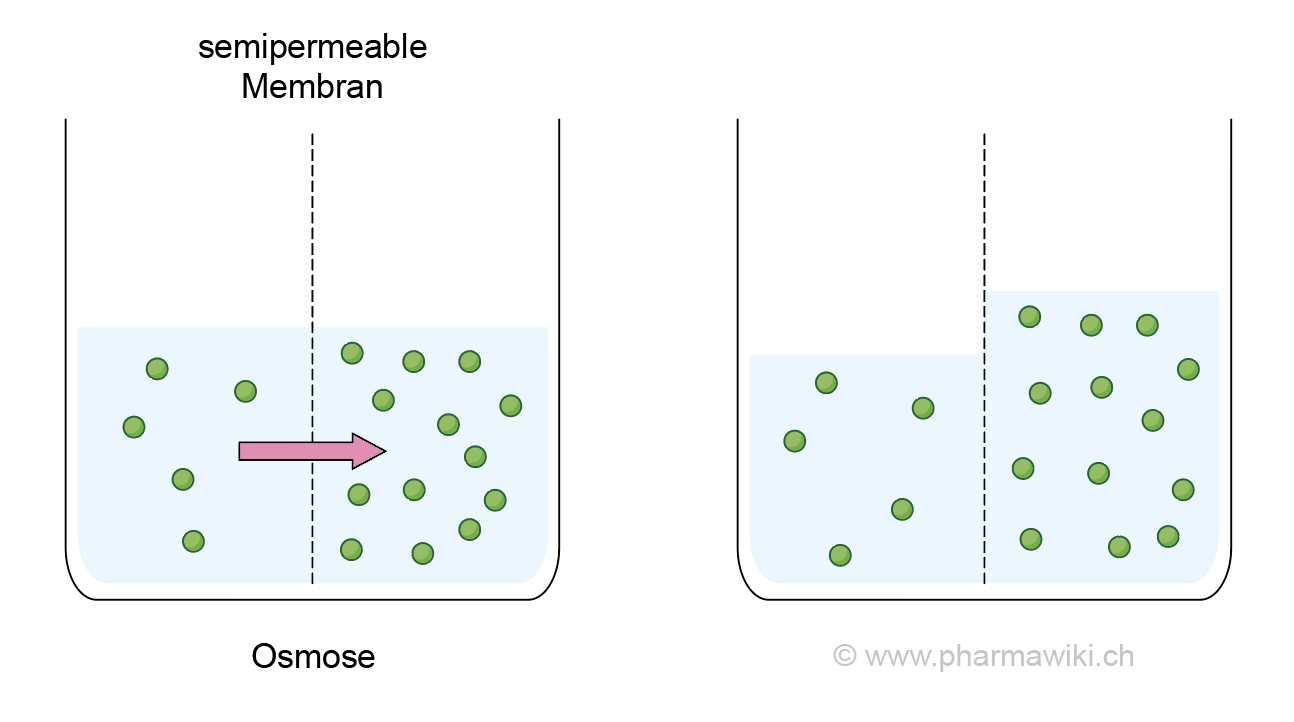
Osmose ist ein Spezialfall der Diffusion. Sie beschreibt die Bewegung von Wasser (oder eines anderen Lösungsmittels) durch eine semipermeable Membran von einem Bereich hoher Wasserkonzentration (niedrige Konzentration an gelösten Stoffen) zu einem Bereich niedriger Wasserkonzentration (hohe Konzentration an gelösten Stoffen). Eine semipermeable Membran ist eine Membran, die Wasser passieren lässt, aber bestimmte gelöste Stoffe zurückhält. Denke an ein Sieb, das kleine Sandkörner durchlässt, aber größere Steine zurückhält.
Die treibende Kraft der Osmose
Die treibende Kraft der Osmose ist der Unterschied im Wasserpotenzial zwischen zwei Bereichen, der durch den Unterschied in der Konzentration der gelösten Stoffe verursacht wird. Vereinfacht gesagt, das Wasser versucht, die Konzentration der gelösten Stoffe auf beiden Seiten der Membran auszugleichen, indem es sich dorthin bewegt, wo mehr gelöste Stoffe sind. Auch hier ist Osmose ein passiver Transportprozess und benötigt keine zusätzliche Energie.
Osmotischer Druck
Der osmotische Druck ist der Druck, der erforderlich ist, um die Osmose zu stoppen. Er ist ein Maß für die Tendenz des Wassers, sich in einen Bereich hoher Konzentration gelöster Stoffe zu bewegen. Je höher die Konzentration der gelösten Stoffe, desto höher der osmotische Druck.
Beispiele für Osmose
- Wasseraufnahme in Pflanzenwurzeln: Pflanzen nehmen Wasser aus dem Boden durch Osmose auf. Die Konzentration der gelösten Stoffe in den Wurzelzellen ist höher als im Bodenwasser, wodurch Wasser in die Wurzeln strömt.
- Blutkörperchen in unterschiedlichen Lösungen: Wenn rote Blutkörperchen in eine hypertonische Lösung (höhere Salzkonzentration als im Zellinneren) gelegt werden, schrumpfen sie, da Wasser aus den Zellen austritt. In einer hypotonischen Lösung (niedrigere Salzkonzentration als im Zellinneren) platzen sie, da Wasser in die Zellen einströmt. In einer isotonischen Lösung (gleiche Salzkonzentration wie im Zellinneren) bleiben sie normal.
- Konservierung von Lebensmitteln: Durch das Salzen oder Zuckern von Lebensmitteln wird die Wasserkonzentration in der Umgebung des Lebensmittels gesenkt, was dazu führt, dass Mikroorganismen durch Osmose Wasser verlieren und absterben.
- Gurken einlegen: Der Einlegeprozess basiert auf Osmose. Die Gurken verlieren Wasser an die salzige oder saure Lake, wodurch sie schrumpfen und haltbarer werden.
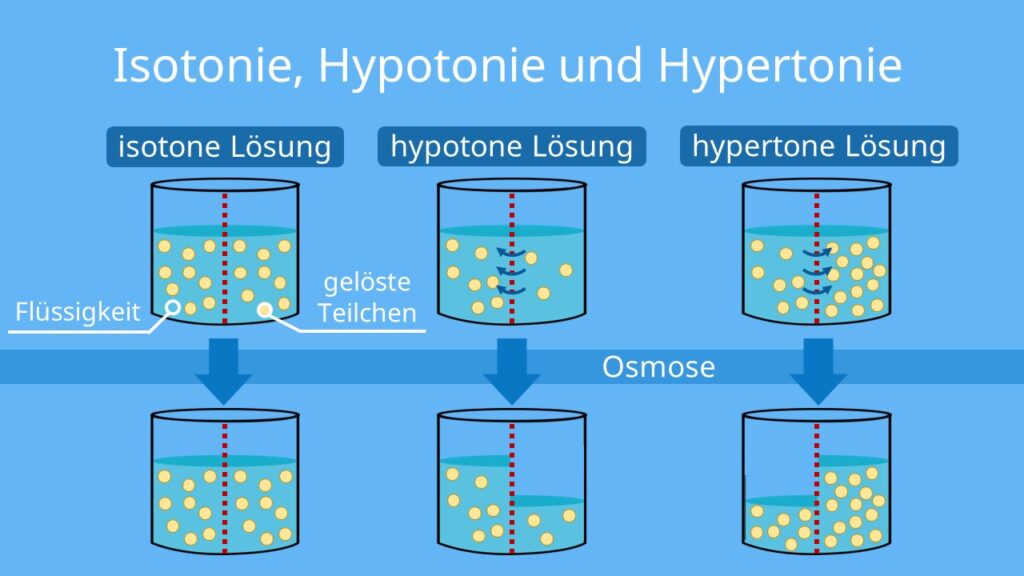
Tonizität
Der Begriff Tonizität beschreibt die relative Konzentration gelöster Stoffe in zwei Lösungen, die durch eine semipermeable Membran getrennt sind. Er wird oft verwendet, um die Auswirkungen einer Lösung auf Zellen zu beschreiben:
- Isotonisch: Die Konzentration der gelösten Stoffe ist gleich auf beiden Seiten der Membran. Es gibt keinen Nettofluss von Wasser.
- Hypertonisch: Die Lösung hat eine höhere Konzentration gelöster Stoffe als die andere Lösung. Wasser strömt aus der anderen Lösung (z.B. einer Zelle) in die hypertonische Lösung.
- Hypotonisch: Die Lösung hat eine niedrigere Konzentration gelöster Stoffe als die andere Lösung. Wasser strömt aus der hypotonischen Lösung in die andere Lösung (z.B. eine Zelle).
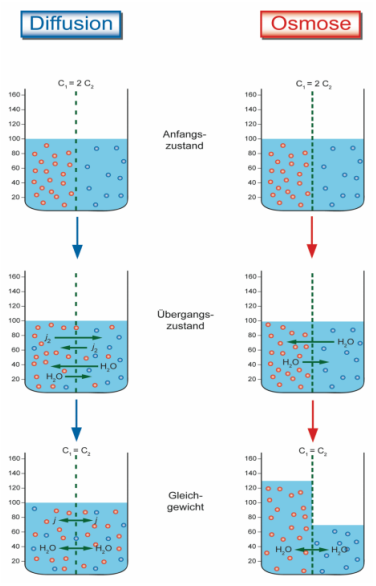
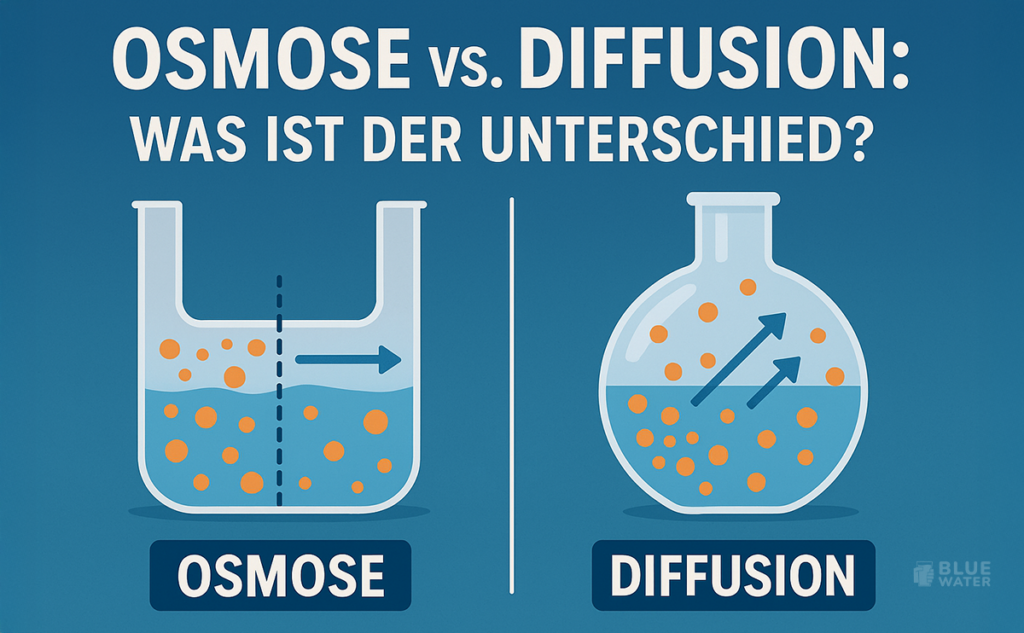
Der Unterschied zwischen Diffusion und Osmose
Obwohl sowohl Diffusion als auch Osmose passive Transportprozesse sind, die durch Konzentrationsgradienten angetrieben werden, gibt es wichtige Unterschiede:
| Merkmal | Diffusion | Osmose |
|---|---|---|
| Bewegung von | Teilchen (Atome, Ionen, Moleküle) | Wasser (oder anderes Lösungsmittel) |
| Membran erforderlich | Nein | Ja, semipermeable Membran |
| Treibende Kraft | Konzentrationsgradient der Teilchen | Unterschied im Wasserpotenzial (Konzentrationsgradient des Wassers) |
| Spezifisch für | Alle Arten von Teilchen | Wasser (oder anderes Lösungsmittel) |
Zusammenfassend lässt sich sagen: Diffusion ist die Bewegung von Teilchen von einem Bereich hoher zu einem Bereich niedriger Konzentration, während Osmose die Bewegung von Wasser durch eine semipermeable Membran von einem Bereich hoher Wasserkonzentration zu einem Bereich niedriger Wasserkonzentration ist.
Bedeutung für das Verständnis biologischer Prozesse
Diffusion und Osmose sind essentielle Prozesse für das Leben, wie wir es kennen. Sie ermöglichen den Transport von Nährstoffen, Abfallprodukten und Wasser über Zellmembranen und durch den Körper. Das Verständnis dieser Prozesse ist entscheidend für das Verständnis vieler biologischer Funktionen, von der Atmung über die Verdauung bis hin zur Regulation des Wasserhaushaltes.
Das Verständnis von Diffusion und Osmose ist nicht nur für Biologen oder Chemiker wichtig. Es hilft uns allen, die Welt um uns herum besser zu verstehen.
Für Expats und Neuankömmlinge in Deutschland kann dieses Wissen auch im Alltag hilfreich sein, beispielsweise beim Verständnis von Kochprozessen, bei der Auswahl der richtigen Reinigungs- und Waschmittel oder bei der Pflege von Pflanzen.
![Diffusion Und Osmose Einfach Erklärt Osmose • Anwendungen und Osmoregulation · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2023/04/WP-Bilder_Osmose_Diffusion-von-Tinte-in-Wasser-1024x576.jpg)
![Diffusion Und Osmose Einfach Erklärt Osmose einfach erkärt • Ablauf und Beispiele · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2021/12/WP-Bild_Osmose-einfach-erklärt-1024x576.jpg)





![Diffusion Und Osmose Einfach Erklärt Osmose einfach erkärt • Ablauf und Beispiele · [mit Video]](https://d3f6gjnauy613m.cloudfront.net/system/production/videos/004/095/c5a578085b613c3cb0ab7c515335b394fdb0e580/Thumbnail_Osmose-einfach-erklärt.png?1731480618)