Ideales Gas Innere Energie

Stell dir vor, du bist auf einer gigantischen Party. Aber nicht irgendeiner Party, sondern einer, bei der sich Moleküle tummeln! Und was machen diese Moleküle? Sie flitzen herum, stoßen aneinander und haben einfach eine gute Zeit. Wir sprechen hier von einem idealen Gas. Ja, ich weiß, "ideal" klingt vielleicht ein bisschen langweilig, aber glaub mir, es wird spannend!
Die Innere Energie: Der Party-Akku der Moleküle
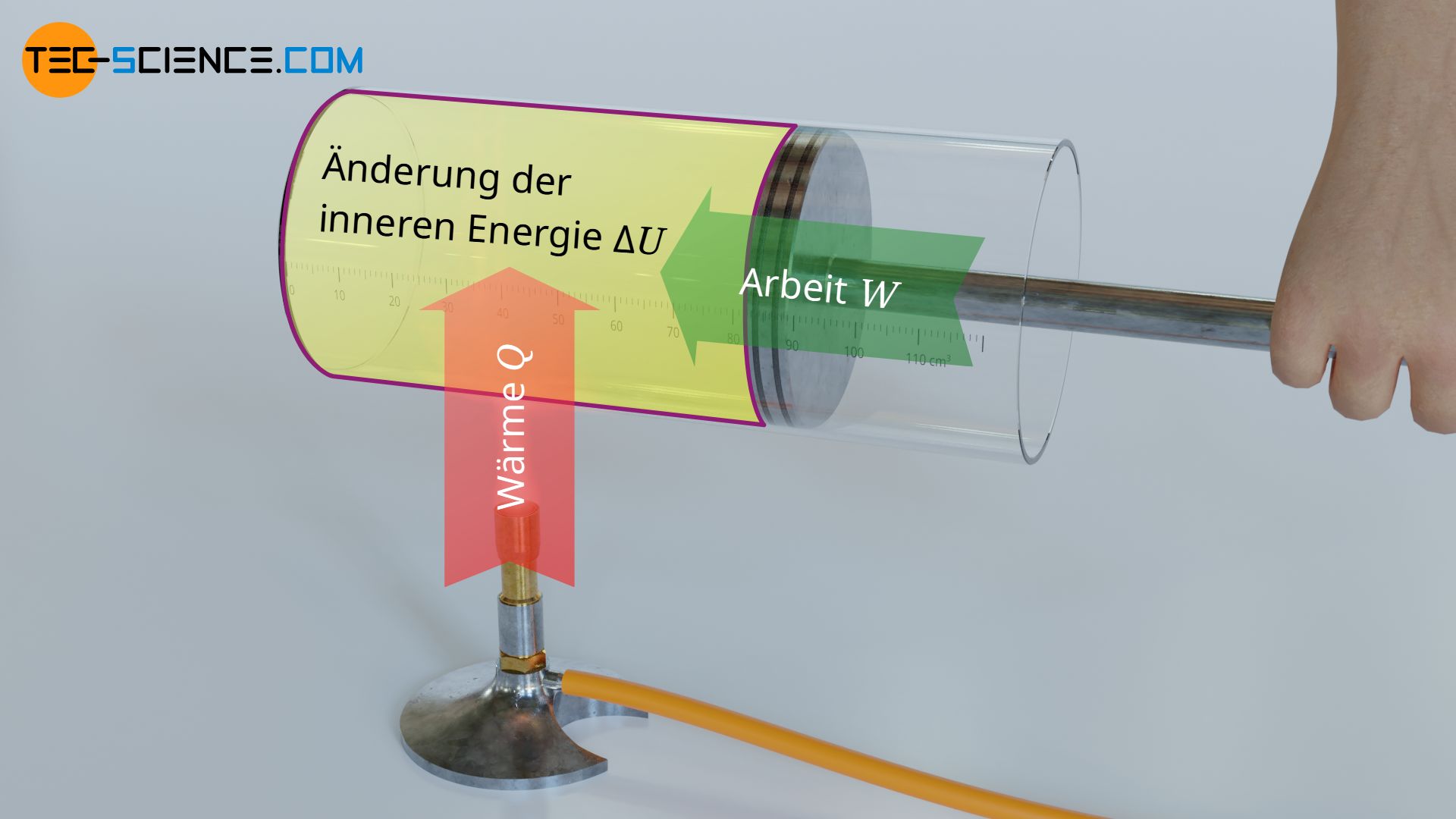
Jede Party braucht Energie, oder? Und auch unsere Molekül-Party hat so etwas: die innere Energie. Denk an sie als den Party-Akku, der all die Bewegung antreibt. Je mehr Energie da ist, desto wilder die Party, desto schneller flitzen die Moleküle umher.
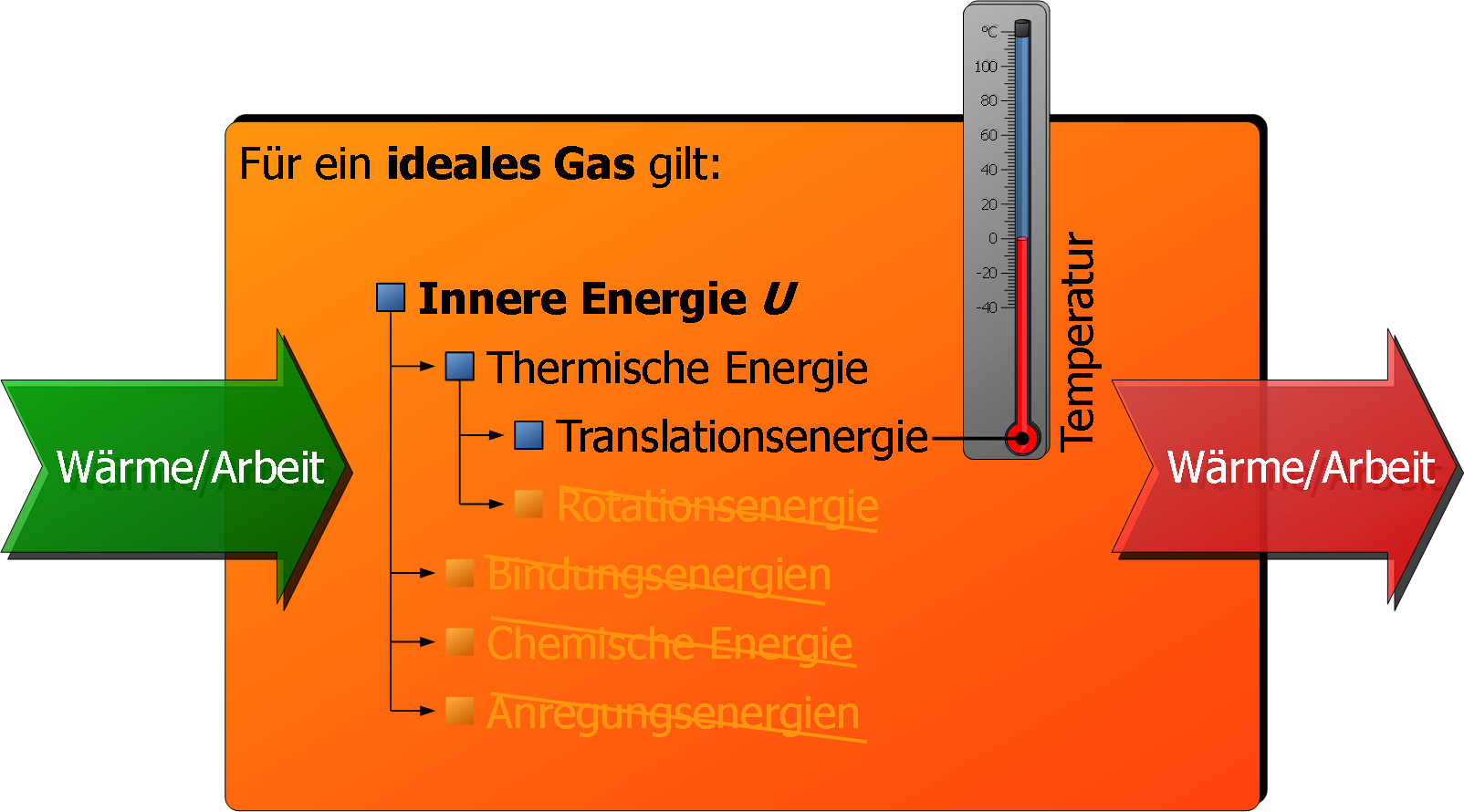
Was genau steckt aber in diesem Akku? Nun, bei einem idealen Gas ist das ziemlich einfach. Die innere Energie ist im Grunde nur die gesamte kinetische Energie aller Moleküle. Kinetische Energie? Keine Panik, das ist nur ein schickes Wort für Bewegungsenergie. Je schneller sich ein Molekül bewegt, desto mehr kinetische Energie hat es, und desto voller ist der Party-Akku.
Temperatur: Der DJ der Molekül-Party
Und wer bestimmt, wie wild die Party wird? Der DJ natürlich! Und in unserem Fall ist der DJ die Temperatur. Stell dir vor, du drehst die Temperatur auf. Was passiert? Die Moleküle drehen auf, bewegen sich schneller und die innere Energie steigt! Andersherum, wenn du die Temperatur runterregelst, chillen die Moleküle und die innere Energie sinkt. Es ist ein simpler Zusammenhang, aber er ist der Schlüssel zum Verständnis.
Hier kommt der Clou: Bei einem idealen Gas hängt die innere Energie ausschließlich von der Temperatur ab. Das bedeutet, egal ob du das Gas in einen winzigen Ballon quetschst oder in einem riesigen Raum herumlaufen lässt, solange die Temperatur gleich bleibt, bleibt auch die innere Energie gleich. Verrückt, oder?
„Die innere Energie eines idealen Gases ist wie ein Thermostat: Sie reagiert nur auf die Temperatur!", würde vielleicht ein etwas exzentrischer Professor sagen.
Keine Anziehungskräfte, keine Probleme!
Was ein ideales Gas so "ideal" macht, ist die Tatsache, dass wir davon ausgehen, dass die Moleküle sich nicht gegenseitig anziehen oder abstoßen. Sie sind wie unabhängige kleine Partytiere, die ihr eigenes Ding machen. In der echten Welt ist das natürlich nicht ganz so. Echte Gase haben schon ein bisschen Anziehungskraft zwischen den Molekülen, was die Sache etwas komplizierter macht. Aber für unsere idealen Gase gilt: keine Anziehungskräfte, keine zusätzlichen Energiekosten! Alle Energie geht direkt in die Bewegung.
Stell dir vor, du wärst auf einer Party, auf der alle ständig versuchen, sich an dich zu klammern. Das würde dich doch auch Energie kosten, oder? Bei idealen Gasen gibt es diesen Stress nicht. Sie können sich voll und ganz auf ihre Bewegung konzentrieren.
Warum das Ganze wichtig ist?
Okay, okay, genug Party-Analogie. Warum sollten wir uns überhaupt mit der inneren Energie idealer Gase beschäftigen? Nun, weil es ein super nützliches Konzept ist! Es hilft uns, das Verhalten von Gasen zu verstehen und vorherzusagen. Das ist wichtig für alles, von der Entwicklung von Motoren bis zur Herstellung von Kühlschränken. Und wer weiß, vielleicht hilft es uns auch, die perfekte Molekül-Party zu planen!
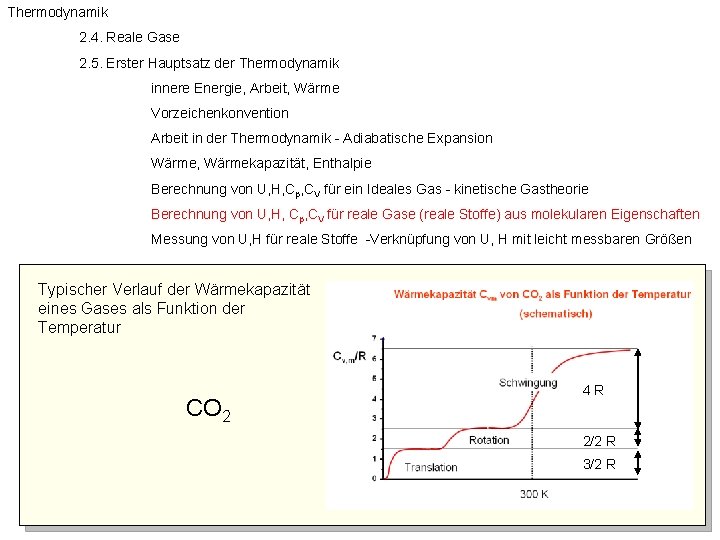
Die Formel für die innere Energie eines idealen Gases sieht übrigens so aus: U = (f/2) * n * R * T. Aber keine Sorge, du musst sie dir nicht merken. Wichtig ist nur, dass du weißt, dass die innere Energie (U) direkt proportional zur Temperatur (T) ist. Der Rest sind nur Konstanten und die Anzahl der Moleküle (n). Der Faktor f steht für die Freiheitsgrade, also die Art und Weise wie sich ein Molekül bewegen kann, z.B. nur vor und zurück oder auch rotieren.
Also, das nächste Mal, wenn du ein Gas siehst, denk daran: Da drin tobt eine Party! Und die innere Energie ist der Akku, der alles am Laufen hält. Und die Temperatur? Die ist der DJ, der die Stimmung bestimmt. Party on!