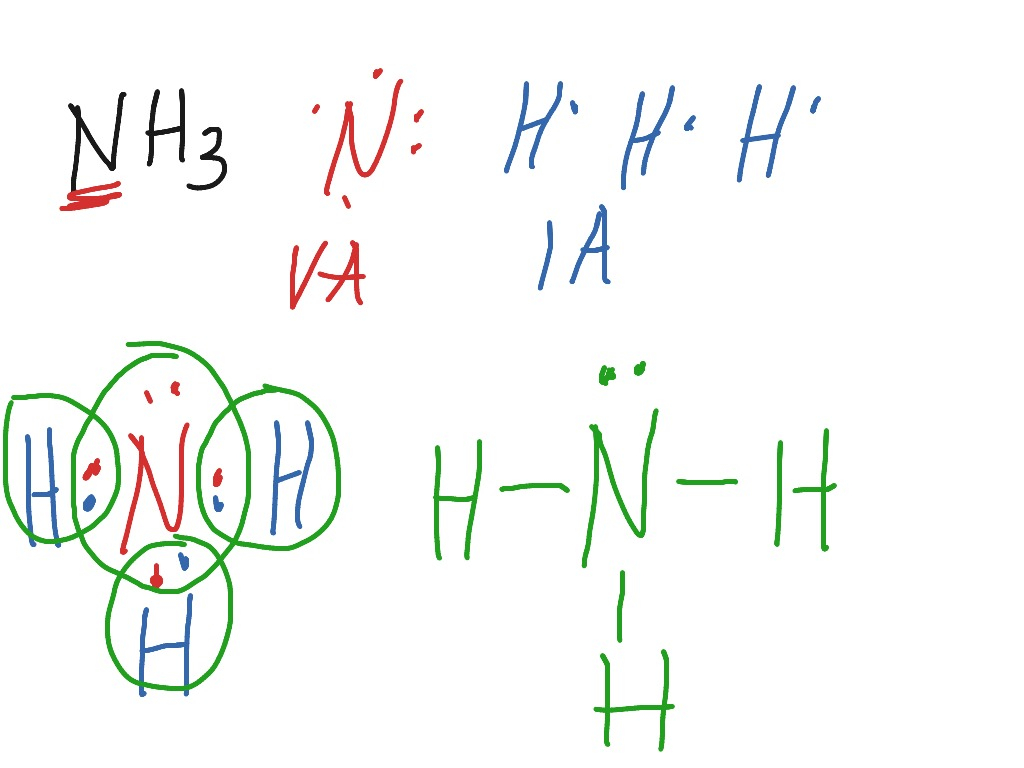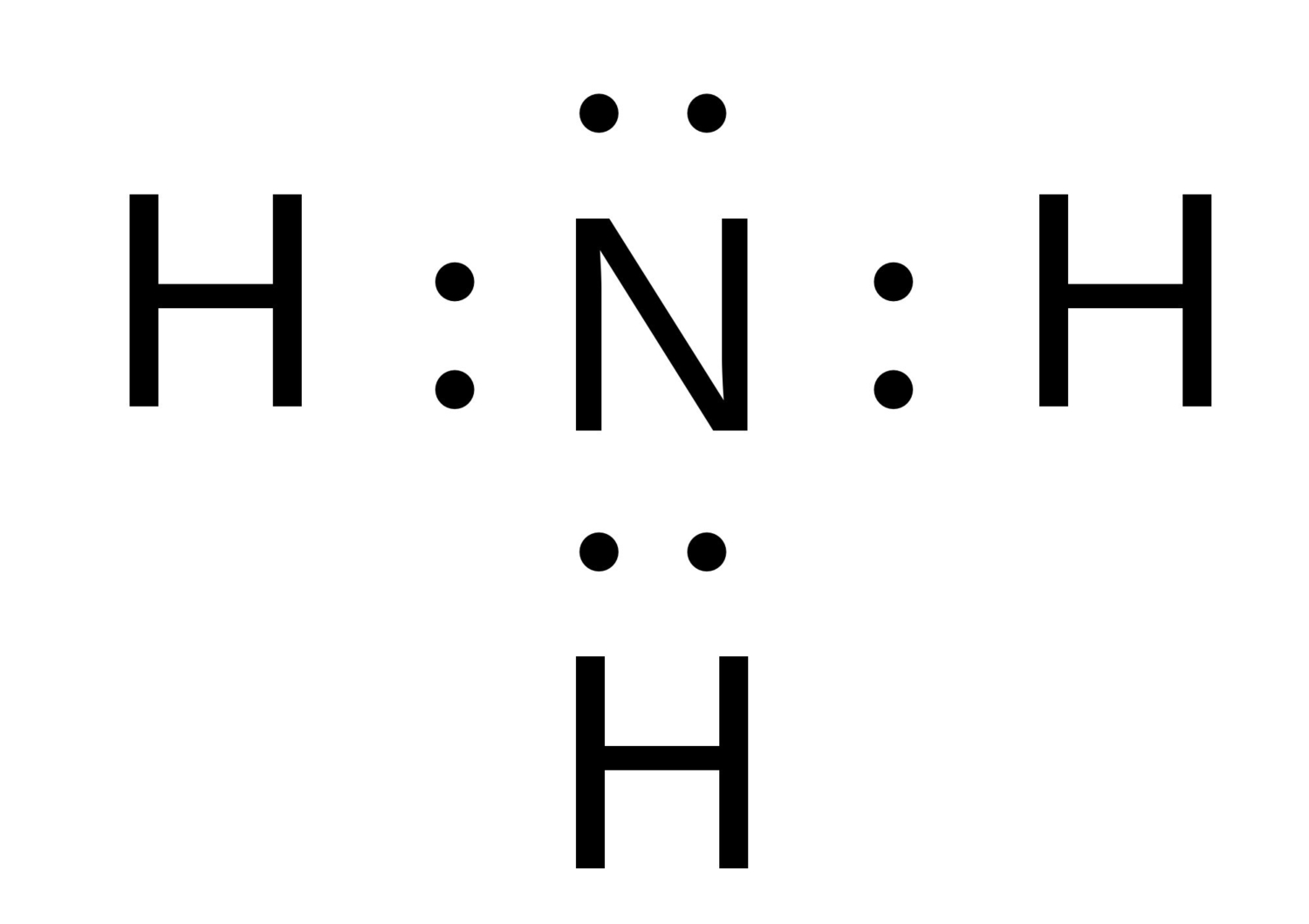Lewis Dot Structure For Nh3
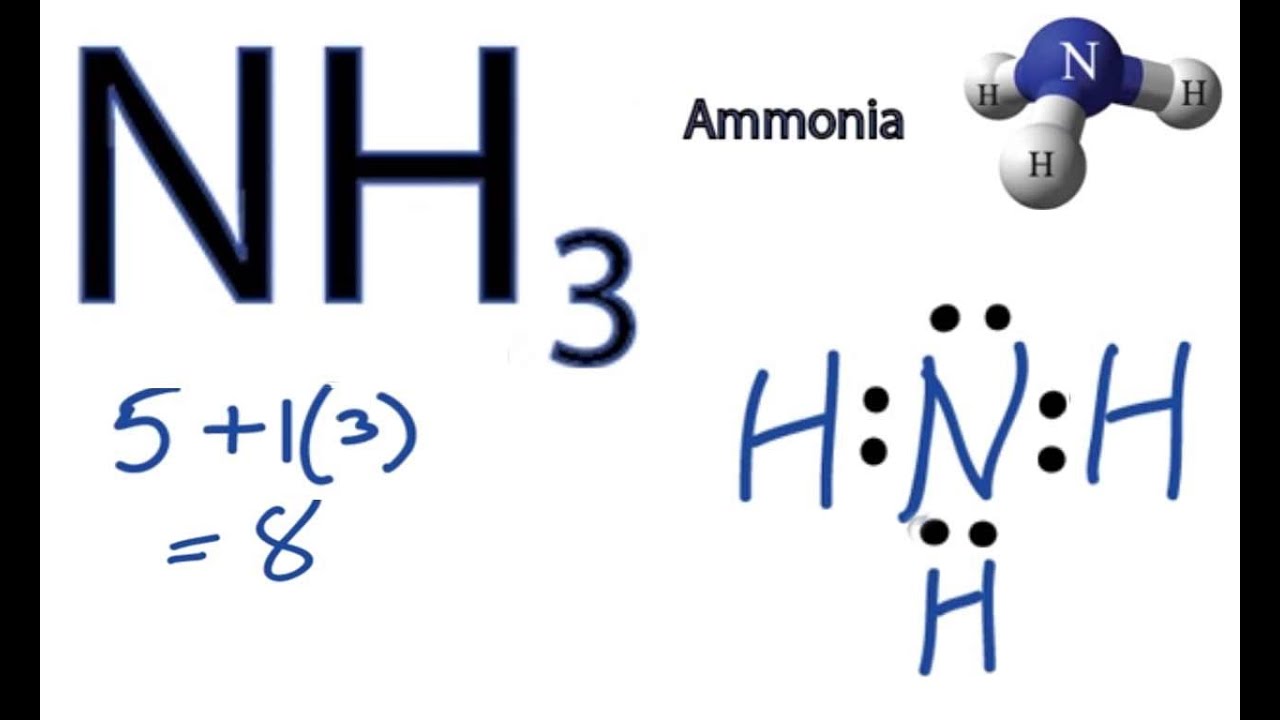
Habt ihr euch jemals gefragt, wie Atome ihre Hände schütteln, um Moleküle zu bilden? Nein, nicht wirklich Hände, sondern eher ihre winzigen elektronischen Wolken! Und wie wir das auf Papier kritzeln können, ohne einen Atomphysik-Doktortitel zu brauchen? Voilà, hier kommt die Lewis-Punkt-Struktur ins Spiel! Stell dir vor, es ist wie ein vereinfachtes Comic über Atomverbindungen.
Heute nehmen wir uns NH3, besser bekannt als Ammoniak, zur Brust. Ammoniak ist überall! Es putzt deine Fenster (als Reinigungsmittel, natürlich!), hilft Pflanzen beim Wachsen (als Dünger), und ist sogar ein wichtiger Baustein für viele Chemikalien. Kurzum: Ammoniak ist ein Star! Aber wie sieht seine atomare Besetzung aus?
Die Zutaten: Stickstoff und Wasserstoff
Unser Starmolekül, NH3, besteht aus einem Stickstoffatom (N) und drei Wasserstoffatomen (H). Stell dir vor, Stickstoff ist der Chefkoch, der drei hungrige kleine Wasserstoff-Azubis um sich schart.
Stickstoff: Der zentrale Boss
Stickstoff, unser Chefkoch, hat 5 wertvolle *Valenzelektronen*. Valenzelektronen sind wie die Zutaten, die ein Atom zum Kochen braucht – sie sind die einzigen, die sich an der Bindung mit anderen Atomen beteiligen. Denk an sie wie kleine Lego-Steine, die darauf warten, sich mit anderen zu verbinden. Wir schreiben das Symbol für Stickstoff, N, und malen dann 5 Punkte drumherum. Tadaa! Das ist Stickstoffs Lewis-Punkt-Darstellung. Fast wie ein kleines Atom-Emoji, oder?
Wasserstoff: Die hungrigen Azubis
Wasserstoff hingegen ist sehr bescheiden. Er hat nur *ein* Valenzelektron. Ein winziges Lego-Steinchen! Also schreiben wir das Symbol für Wasserstoff, H, und malen einen Punkt drumherum. Supersimpel!
Das große Krabbeln: Die Bindung
Jetzt kommt der spannende Teil: Wie verbinden sich Stickstoff und die drei Wasserstoffatome? Stickstoff, der Boss mit 5 Valenzelektronen, will eigentlich 8 haben! Das nennt man die *Oktettregel*. Er will sich wie ein Edelgas fühlen, mit einer voll besetzten Elektronenschale. Wasserstoff hingegen ist zufrieden mit nur 2 Elektronen (Duettregel). Er ist halt genügsam.
Also "leiht" sich Stickstoff von jedem Wasserstoff-Azubi ein Elektron aus. Stell dir vor, jeder Wasserstoff-Azubi gibt dem Chefkoch ein Legostein. Jeder Wasserstoff ist jetzt glücklich, weil er sein Duett erreicht hat (ein eigenes Elektron + ein "geliehenes" vom Stickstoff). Und Stickstoff? Er hat jetzt 8 Elektronen um sich herum (5 eigene + 3 von den Wasserstoffatomen). Oktettregel: Check! Glücklicher Stickstoff-Chefkoch!
Wie zeichnen wir das? Ganz einfach: Wir verbinden jedes Wasserstoffatom mit dem Stickstoffatom durch eine Linie. Jede Linie steht für *ein* Elektronenpaar (zwei Legosteine). Also: H-N-H, mit einem H oben oder unten, je nachdem, wie man es zeichnet.
Moment mal! Stickstoff hatte ja 5 Valenzelektronen, und jetzt haben wir nur 3 Linien gezeichnet (für die Bindungen zu den 3 Wasserstoffatomen). Das bedeutet, dass Stickstoff noch ein Elektronenpaar übrig hat! Dieses Elektronenpaar ist *nicht* an einer Bindung beteiligt. Es sitzt einfach nur faul auf dem Stickstoffatom herum. Wir zeichnen dieses Elektronenpaar als zwei Punkte oben oder unten am Stickstoffatom.
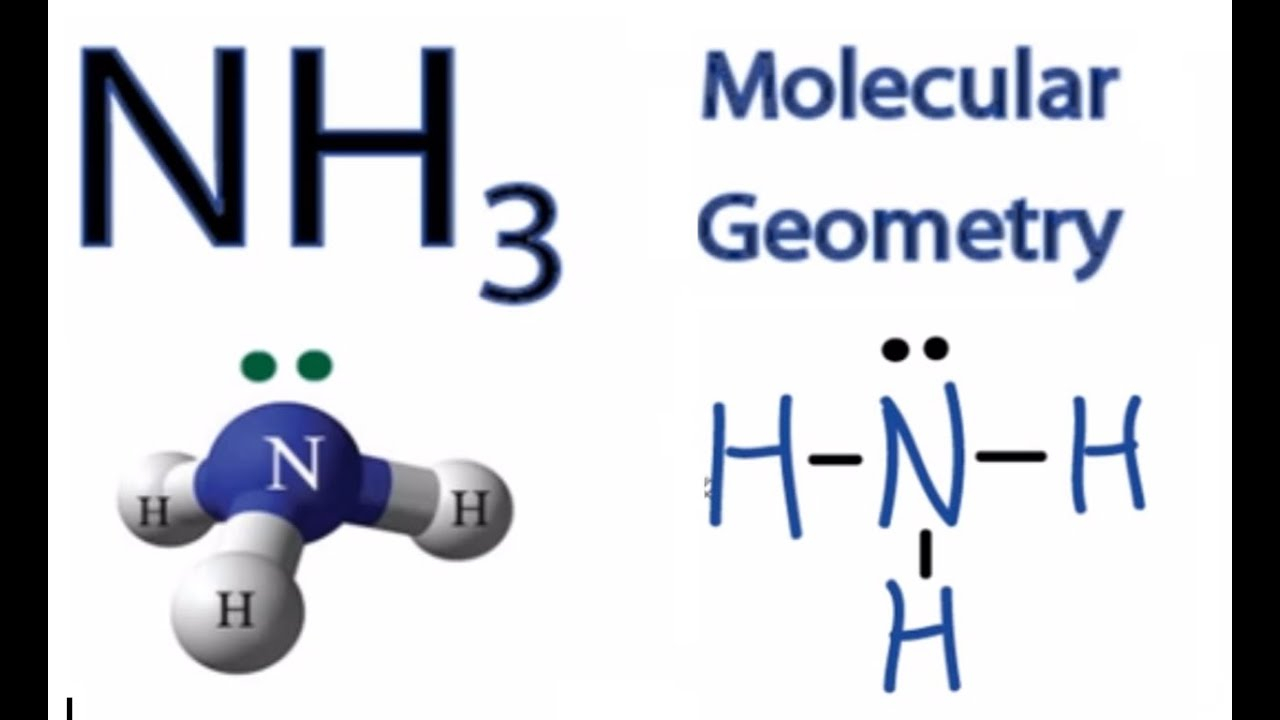
Das Endergebnis: Die Lewis-Punkt-Struktur von NH3
Die vollständige Lewis-Punkt-Struktur von NH3 sieht also so aus:
H
|
H - N - H
|
••
Die Punkte (••) über dem N symbolisieren das freie Elektronenpaar. Die Linien stehen für die Bindungen zwischen dem Stickstoff und den Wasserstoffatomen. Voila! Eine wunderschöne, einfache Darstellung, die uns zeigt, wie die Atome in Ammoniak verbunden sind!
Merke dir: Die Lewis-Punkt-Struktur ist wie eine vereinfachte Landkarte der atomaren Verbindungen. Sie hilft uns zu verstehen, wie Atome ihre Elektronen teilen, um stabile Moleküle zu bilden.
Und jetzt, geh raus und beeindrucke deine Freunde mit deinem neu erworbenen Wissen über die Lewis-Punkt-Struktur von Ammoniak! Vielleicht kannst du sogar erklären, warum Ammoniak so gut Fenster putzt (obwohl das wahrscheinlich etwas mehr Chemie erfordert...). Aber hey, du hast den ersten Schritt gemacht! Du bist jetzt ein zertifizierter NH3-Lewis-Punkt-Struktur-Experte!