Magnesium Und Salzsäure Reaktionsgleichung

Stell dir vor, du bist in der Küche. Vielleicht machst du dir gerade einen Salat an, oder vielleicht stehst du vor einem angefangenen Kuchenteig. Was du wahrscheinlich nicht erwartest, ist, dass du gleich eine kleine, kontrollierte Explosion verursachen wirst. Aber genau das passiert im Prinzip, wenn wir uns die Reaktion von Magnesium und Salzsäure genauer anschauen! Keine Sorge, du brauchst keinen Schutzanzug – zumindest nicht für diese gedankliche Reise.
Was passiert da überhaupt?
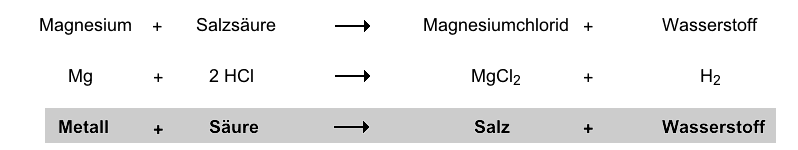
Okay, lass uns die Magnesium und Salzsäure Reaktionsgleichung mal ein bisschen auseinandernehmen, ohne dass es gleich nach Chemieunterricht klingt. Stell dir Magnesium als einen kleinen, drahtigen Muskelprotz vor. Er ist wirklich heiß darauf, mit anderen Atomen zu interagieren. Salzsäure, die wir in verdünnter Form auch als Magensäure kennen, ist wie ein ungeduldiger Türsteher, der jedem sagt, wo es langgeht.
Wenn diese beiden aufeinandertreffen, dann kracht es! Der Magnesium-Muskelprotz schnappt sich die Chlorid-Ionen aus der Salzsäure und bildet Magnesiumchlorid. Das ist wie ein chemischer Partnerwechsel auf der Tanzfläche. Aber das ist noch nicht alles! Bei dieser ganzen Umverteilung wird auch Wasserstoffgas freigesetzt. Und genau das ist der Clou.
Die Bläschen-Party
Das Wasserstoffgas, das bei dieser Reaktion entsteht, ist nämlich ein ganz besonderer Gast. Es ist leicht entzündlich! Stell dir vor, du wirfst einen kleinen Magnesiumspan in verdünnte Salzsäure. Du würdest sofort Bläschen sehen, die aufsteigen. Das ist das Wasserstoffgas, das sich verabschiedet. Und wenn du eine Flamme in die Nähe dieser Bläschen hältst… *Plopp*! Eine kleine, harmlose Verpuffung. Klingt fast wie eine Miniatur-Silvesterfeier, oder?
Warum ist das lustig? Weil wir hier über etwas sprechen, das in jedem Chemielabor passiert, aber im Grunde genommen eine ziemlich dramatische Inszenierung ist. Ein Metall, das mit einer Säure interagiert und dabei ein entzündliches Gas freisetzt. Das ist fast schon Actionfilm-verdächtig. Nur eben im Kleinformat und ohne Michael Bay.
Mehr als nur eine Gleichung
Die Reaktion von Magnesium und Salzsäure ist aber mehr als nur eine lustige chemische Reaktion. Sie ist ein Beispiel für etwas Grundlegendes in der Chemie: Reaktionen sind Energieaustausch. Magnesium ist sozusagen sehr motiviert, Magnesiumchlorid zu werden. Diese Motivation setzt Energie frei, in diesem Fall in Form von Wärme und der Bildung von Wasserstoffgas.
Denk mal drüber nach. Das Universum strebt immer nach dem energieärmsten Zustand. Dinge wollen sich stabilisieren. Und die Reaktion von Magnesium und Salzsäure ist ein kleiner, aber deutlicher Beweis dafür.
"Chemie ist die Lehre von der Veränderung der Materie,"
hat mal jemand gesagt. Und die Reaktion von Magnesium und Salzsäure ist ein wunderschönes Beispiel für diese Veränderung.
Wo begegnet uns diese Reaktion noch?
Auch wenn du vielleicht nicht jeden Tag Magnesium in Salzsäure wirfst (was auch gut so ist!), begegnet dir die zugrundeliegende Chemie oft im Alltag. Zum Beispiel bei Batterien. Viele Batterien nutzen chemische Reaktionen, um elektrische Energie zu erzeugen. Und oft sind Metalle und Säuren oder Basen beteiligt.
Auch in der Industrie spielt die Reaktion eine Rolle. Magnesiumchlorid, das bei der Reaktion entsteht, hat viele Anwendungen, zum Beispiel in der Medizin oder bei der Herstellung von bestimmten Baumaterialien.
Ein letzter Gedanke
Die nächste Frage ist natürlich: Könnte man diese Reaktion nutzen, um ein Auto anzutreiben? Theoretisch ja! Wasserstoffgas kann als Treibstoff verwendet werden. Aber die praktische Umsetzung ist natürlich viel komplizierter. Und wahrscheinlich auch nicht so lustig wie die kleine Bläschen-Party im Chemielabor.
Vielleicht ist es ja gerade das, was die Chemie so faszinierend macht: Sie ist voller kleiner Überraschungen und potentieller Möglichkeiten. Und manchmal reicht ein Magnesiumspan und etwas Salzsäure, um uns daran zu erinnern, dass die Welt um uns herum voller verborgener Reaktionen steckt. Man muss nur genau hinschauen… oder eben eine kleine, kontrollierte Explosion auslösen!
Und das nächste Mal, wenn du Magnesiumtabletten einnimmst (vielleicht gegen Muskelkrämpfe, ironischerweise), denk daran, was passiert, wenn das Magnesium in deinem Magen mit der Salzsäure in Kontakt kommt. Keine Sorge, es gibt keine Explosion. Aber es ist schon irgendwie cool zu wissen, dass da im Kleinen etwas passiert, das auf einer winzigen, atomaren Ebene ganz schön viel los ist. Chemie ist eben überall – auch in uns selbst!