Molare Masse Von Sauerstoff
Habt ihr euch jemals gefragt, warum Chemiker so vernarrt in Zahlen sind? Und warum eine bestimmte Zahl, die mit Sauerstoff zu tun hat, so faszinierend ist? Lasst uns eintauchen in die Welt der molaren Masse von Sauerstoff! Es ist überraschend unterhaltsam, versprochen!
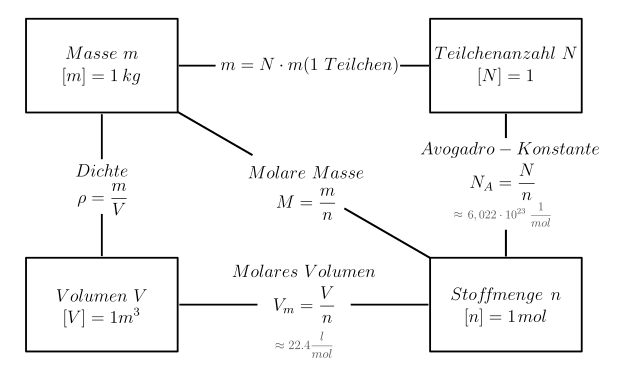
Was ist diese "molare Masse" überhaupt?
Stellt euch vor, ihr backt einen Kuchen. Ihr braucht eine bestimmte Menge Mehl, Zucker und Eier, richtig? Die molare Masse ist wie ein Rezept, aber für Atome und Moleküle! Sie sagt uns, wie viel ein Mol von einem bestimmten Stoff wiegt. Ein Mol ist einfach eine bestimmte Anzahl von Teilchen (ungefähr 6,022 x 10^23, falls ihr's genau wissen wollt, aber keine Panik, das müssen wir uns nicht merken!).
Denkt daran als eine riesige Tüte voller Sauerstoffatome. Die molare Masse sagt uns, wie schwer diese riesige Tüte wäre. Praktisch, oder?
Warum ist Sauerstoff so besonders?
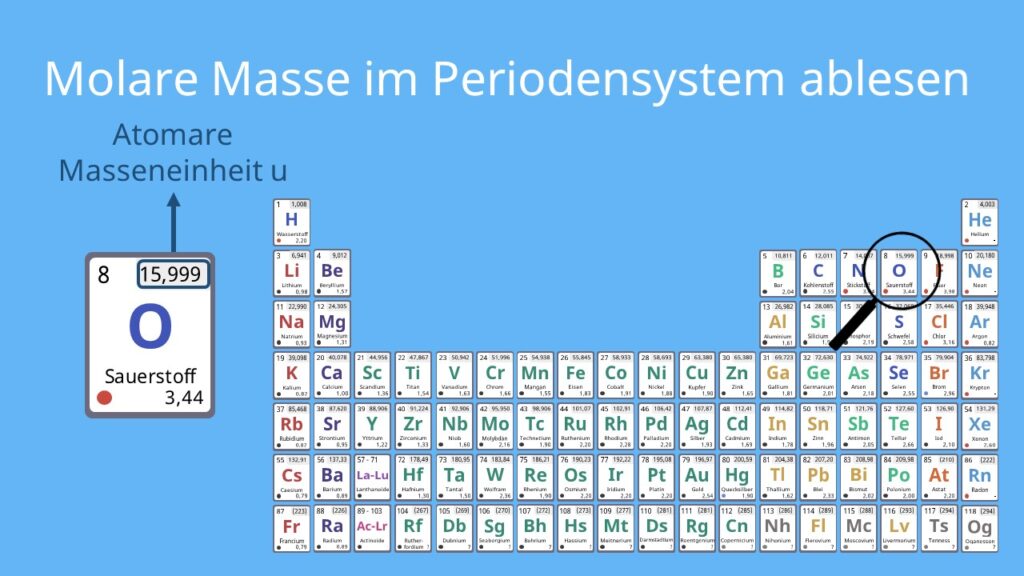
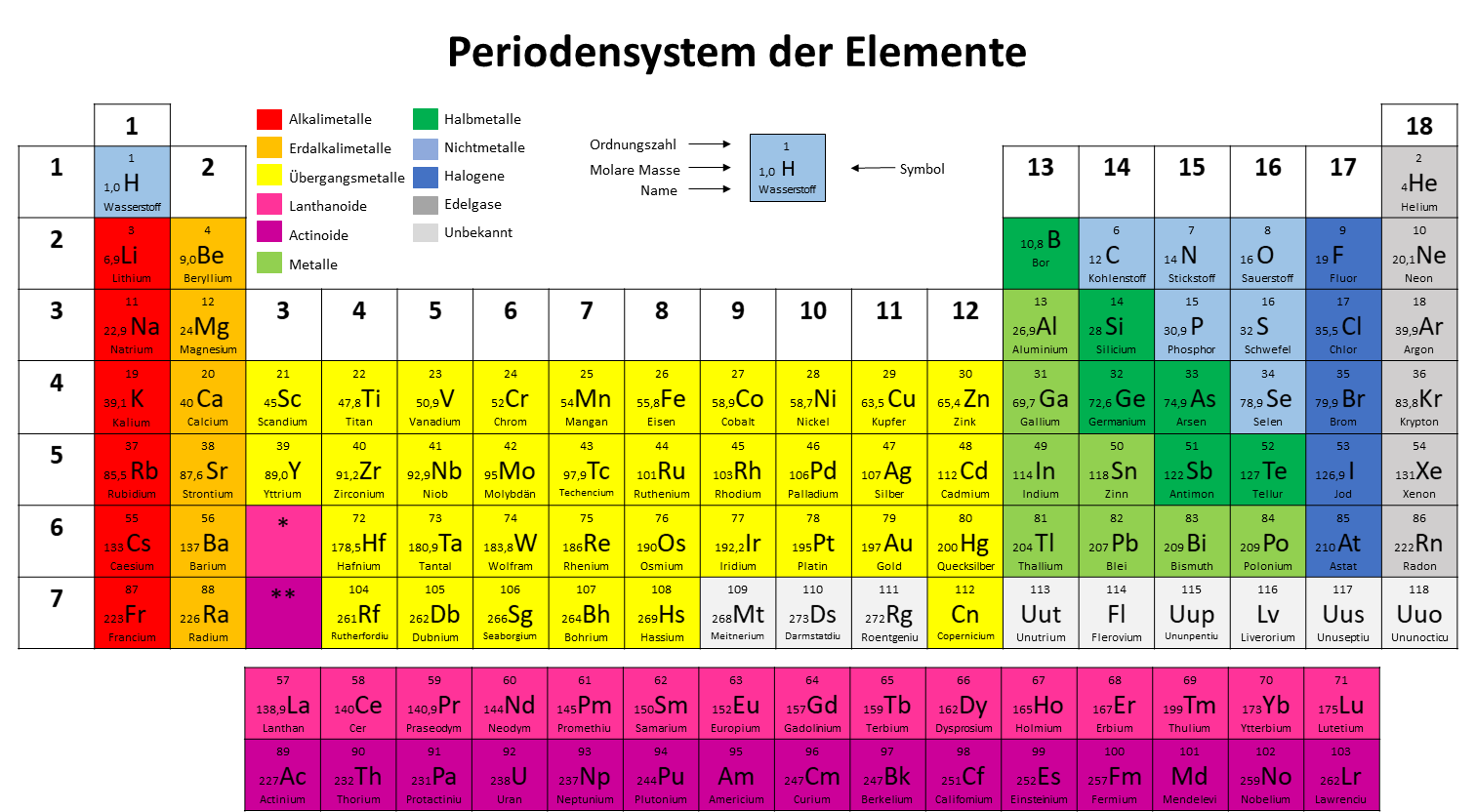
Sauerstoff, das O im Periodensystem, ist ein echter Star! Wir atmen ihn, Pflanzen produzieren ihn, und ohne ihn würde kein Feuer brennen. Er ist überall! Und deshalb ist es so nützlich, seine molare Masse zu kennen.
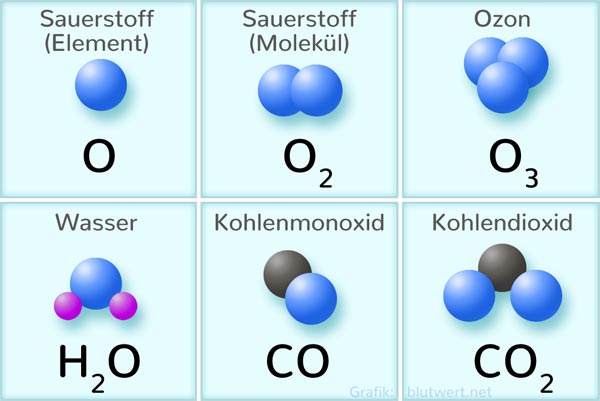
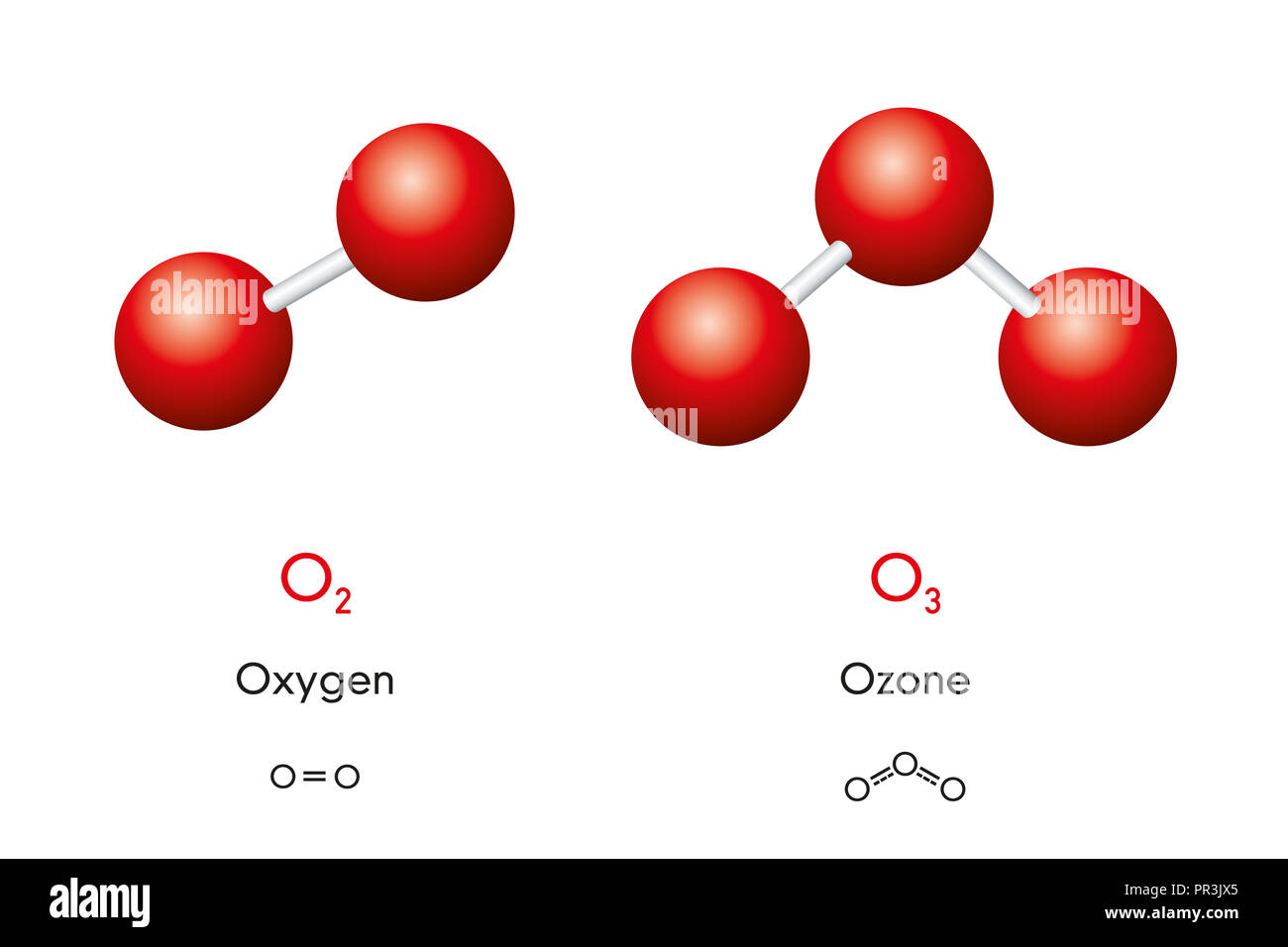
Aber hier kommt der Clou: Sauerstoff kommt normalerweise nicht allein vor. Er liebt es, sich mit einem anderen Sauerstoffatom zu verbinden und O2 zu bilden. Das ist der Sauerstoff, den wir atmen! Das bedeutet, dass wir bei der molaren Masse von Sauerstoff oft über die molare Masse von Sauerstoffmolekülen sprechen, also O2, und nicht nur über ein einzelnes O-Atom. Das ist wie der Unterschied zwischen einem einzelnen Gummibärchen und einer ganzen Tüte!
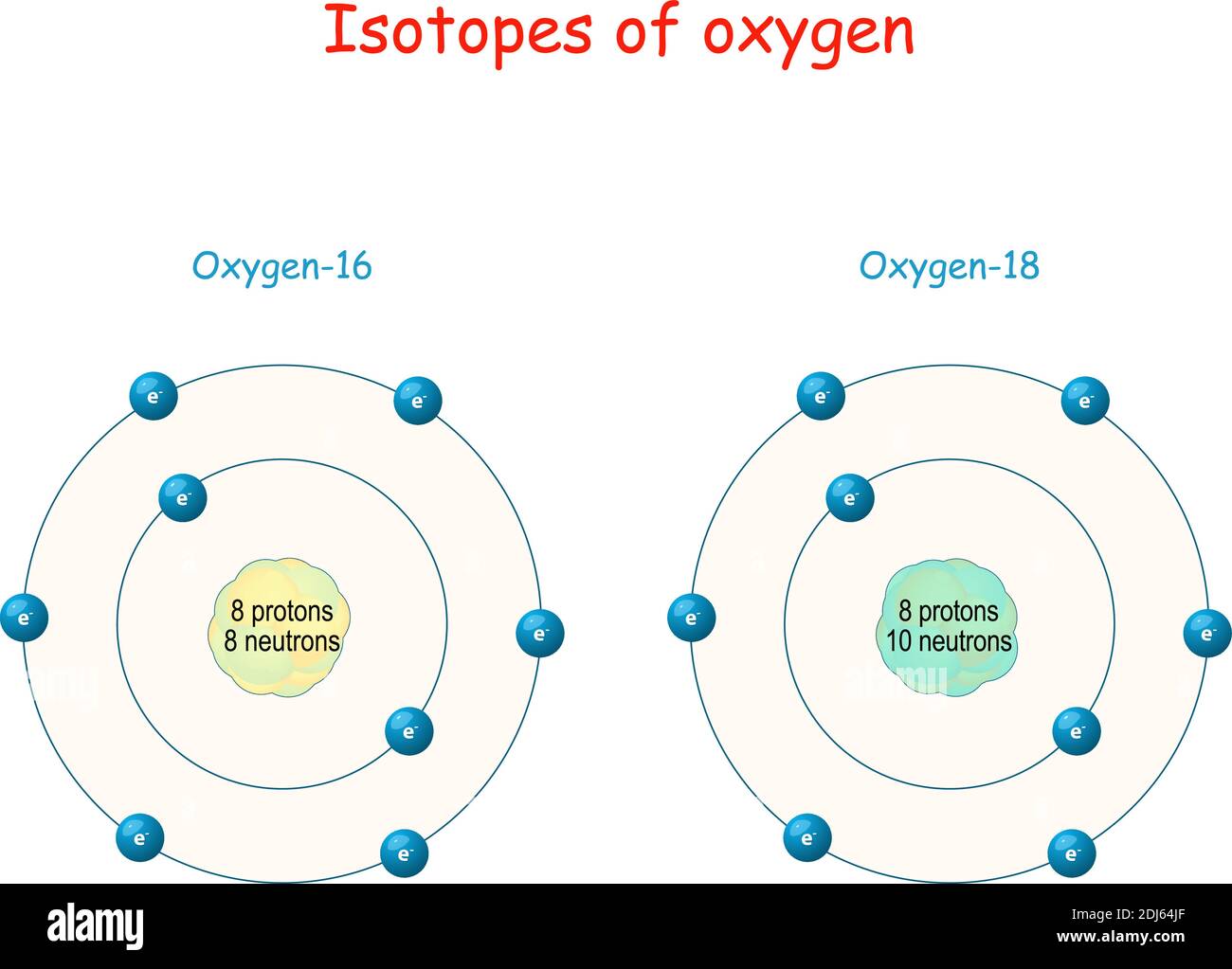
Die magische Zahl: 16 (oder doch 32?)
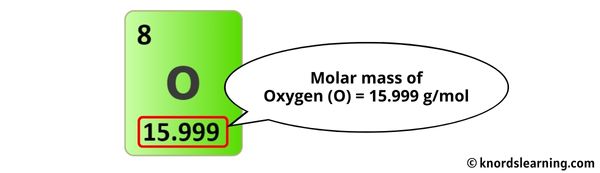
Ein einzelnes Sauerstoffatom (O) hat eine molare Masse von ungefähr 16 Gramm pro Mol (g/mol). Aber Moment mal! Da Sauerstoff normalerweise als O2 vorkommt, müssen wir die 16 verdoppeln. Das bedeutet, die molare Masse von O2 ist etwa 32 g/mol. Boom! Da haben wir's!
Merkt euch: Sauerstoff (O2) hat eine molare Masse von ungefähr 32 g/mol. Das ist eine Zahl, die sich Chemiker merken, so wie sich Bäcker das perfekte Verhältnis von Mehl und Zucker merken!
Warum ist das so unterhaltsam?
Okay, vielleicht ist "unterhaltsam" etwas übertrieben. Aber denkt darüber nach! Diese Zahl (32 g/mol) ist der Schlüssel zu so vielen Berechnungen in der Chemie. Wir können sie verwenden, um herauszufinden, wie viel Sauerstoff in einem bestimmten Volumen Luft ist, wie viel Sauerstoff bei einer chemischen Reaktion verbraucht wird, und vieles mehr! Es ist wie ein kleines Werkzeug, das uns hilft, die Welt um uns herum besser zu verstehen.
Und das ist doch irgendwie cool, oder?
Wo begegnet uns die molare Masse von Sauerstoff?
Überall! In der Medizin, wenn es um die Sauerstoffversorgung von Patienten geht. In der Umweltwissenschaft, wenn es um die Untersuchung der Luftqualität geht. In der Industrie, wenn es um die Herstellung von Chemikalien geht, die Sauerstoff benötigen. Die molare Masse von Sauerstoff ist ein stiller Held, der im Hintergrund wirkt.
Stellt euch vor, ihr seid in einem Labor und müsst berechnen, wie viel Sauerstoff benötigt wird, um eine bestimmte Menge von etwas zu verbrennen. Ohne die molare Masse von Sauerstoff wärt ihr aufgeschmissen! Sie ist wie der Decoder für ein geheimes Rezept.
Inspiration für Entdecker!
Die Chemie ist voller solcher faszinierender Details. Die molare Masse von Sauerstoff ist nur ein kleiner Einblick in eine riesige, komplexe und unglaublich spannende Welt. Wenn ihr jetzt neugierig geworden seid, dann taucht tiefer ein! Es gibt unendlich viel zu entdecken.
Vielleicht werdet ihr ja der nächste Marie Curie oder der nächste Linus Pauling! (Okay, vielleicht nicht ganz, aber man darf ja träumen!). Die Welt braucht kluge Köpfe, die die Geheimnisse der Chemie entschlüsseln können.
Also, das nächste Mal, wenn ihr tief Luft holt, denkt an die magische Zahl 32. Und denkt daran, dass hinter jedem Atemzug eine ganze Welt der Wissenschaft steckt!
Viel Spaß beim Entdecken!






![Molare Masse Von Sauerstoff Sauerstoff • einfach erklärt: Steckbrief, Nachweis · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2021/04/Orbitalmodell-Sauerstoff-1-1024x576.jpg)


.jpg?1394457633)
![Molare Masse Von Sauerstoff Molare Masse • einfach erklärt und Beispiel · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2022/05/Thumbnail_Mol-1024x576.jpg)
