Molecular Mass Of Na2co3

Habt ihr euch jemals gefragt, was eigentlich hinter den einfachen Dingen steckt, die wir täglich benutzen? Nehmen wir zum Beispiel Natriumcarbonat, chemisch korrekt Na2CO3. Klingt erstmal nach einem Zungenbrecher für den Chemieunterricht, aber keine Sorge, wir machen daraus ein vergnügliches Abenteuer!
Ein Ausflug in die Welt der Moleküle
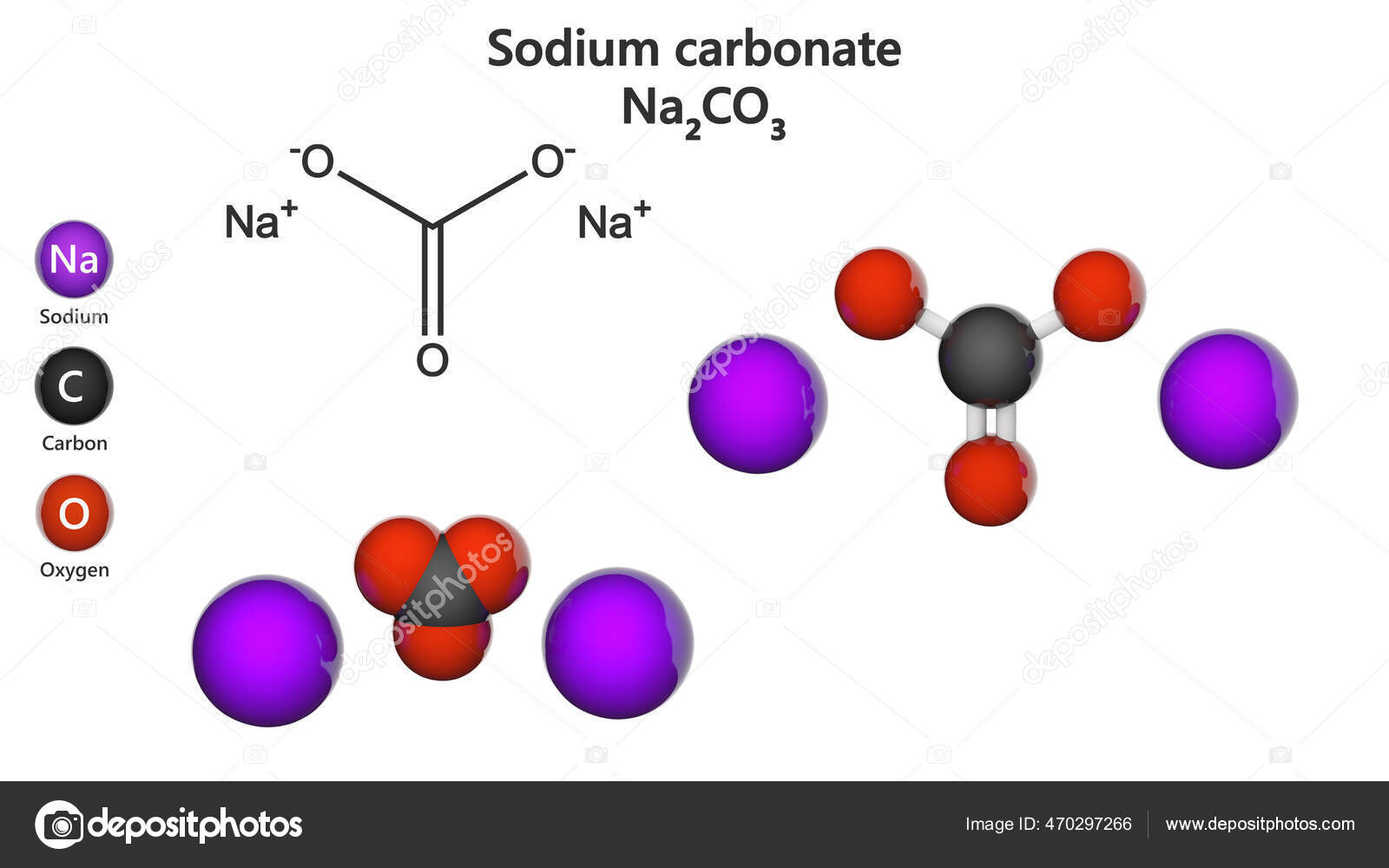
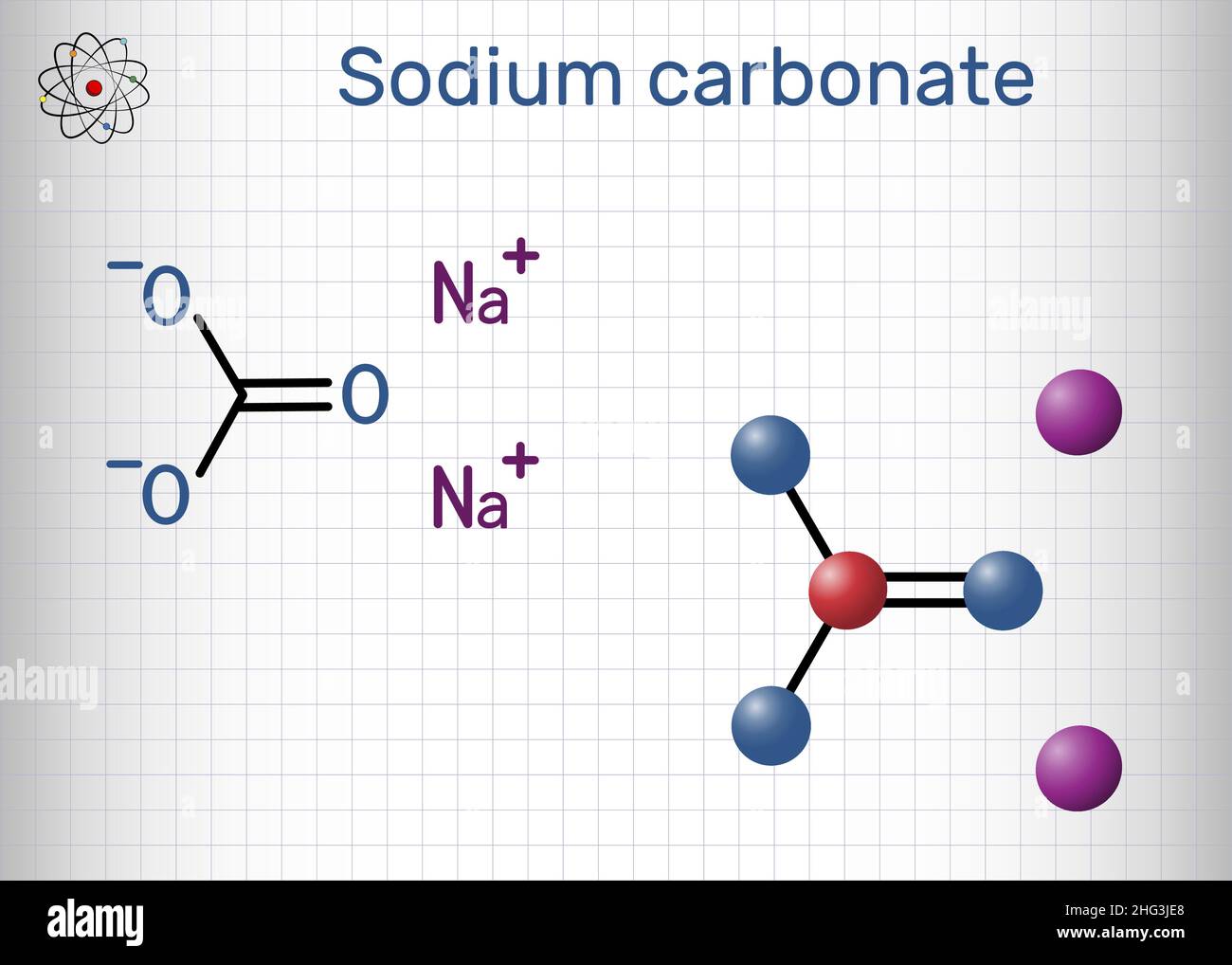
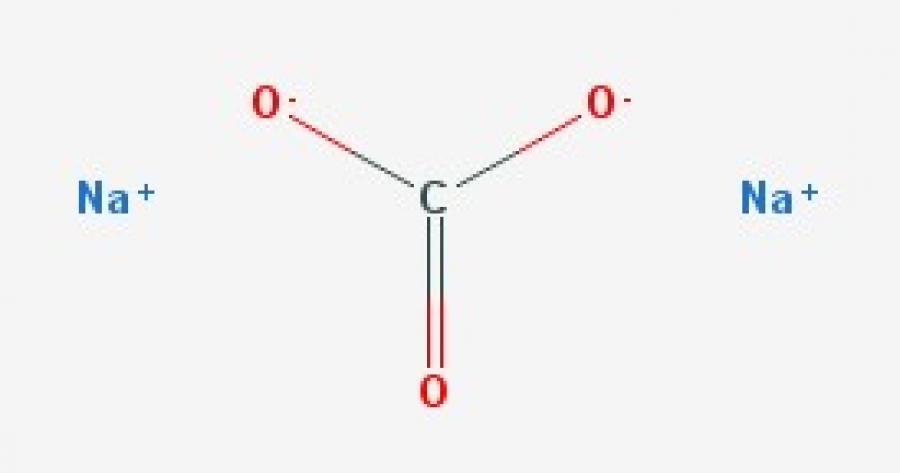
Stellt euch vor, ihr backt einen Kuchen. Ihr braucht Eier, Mehl, Zucker – alles Zutaten, die sich zu einem leckeren Ganzen verbinden. Genauso ist es mit Na2CO3. Es besteht aus einzelnen "Zutaten", nämlich Atomen: Natrium (Na), Kohlenstoff (C) und Sauerstoff (O). Jedes dieser Atome hat ein bestimmtes Gewicht, eine Art Persönlichkeit auf der Waage der Elemente.
Was wiegt denn so ein Atom?
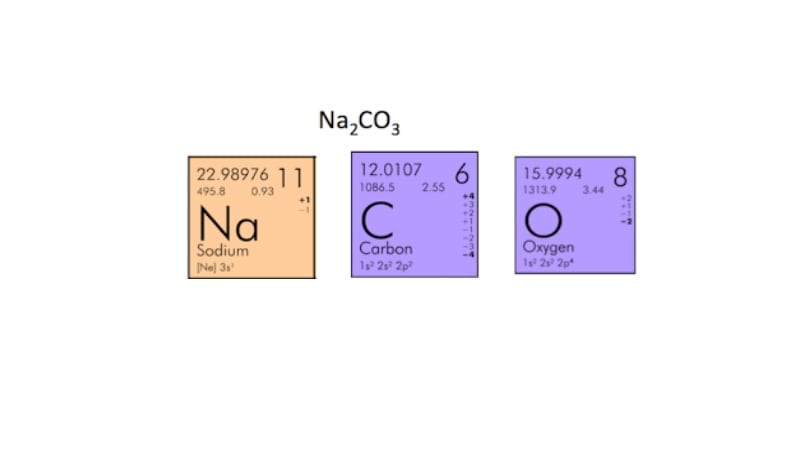
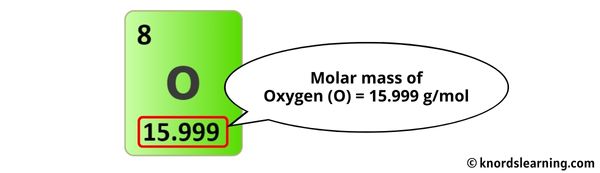
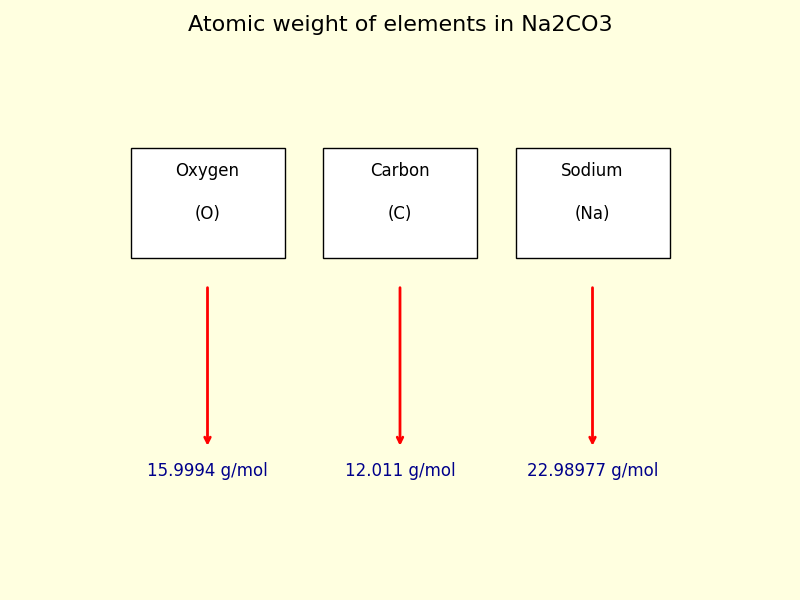
Chemiker haben diese atomaren Gewichte fein säuberlich in einer Tabelle festgehalten, dem Periodensystem. Dort finden wir, dass Natrium (Na) etwa 23 atomare Masseneinheiten (u) wiegt, Kohlenstoff (C) ungefähr 12 u und Sauerstoff (O) rund 16 u. Diese Zahlen sind wie kleine Geheimcodes, die uns verraten, wie schwer jedes Atom im Vergleich zu anderen ist.
Jetzt kommt der Clou! Na2CO3 hat zwei Natriumatome (Na2), ein Kohlenstoffatom (C) und drei Sauerstoffatome (O3). Um die gesamte Masse von Na2CO3 zu berechnen, müssen wir also die Gewichte der einzelnen Atome addieren, aber nicht vergessen, die Anzahl jedes Atoms zu berücksichtigen:
(2 x Gewicht von Na) + (1 x Gewicht von C) + (3 x Gewicht von O)
Setzen wir die Zahlen ein:
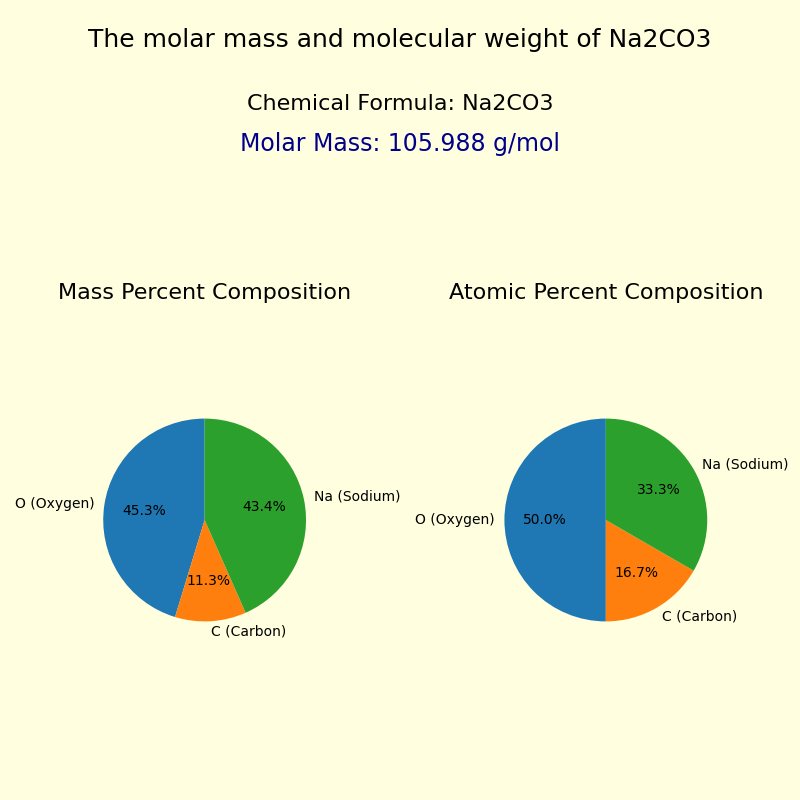
(2 x 23 u) + (1 x 12 u) + (3 x 16 u) = 46 u + 12 u + 48 u = 106 u
Tada! Die molekulare Masse von Na2CO3 beträgt 106 u. Das bedeutet, dass ein einzelnes Molekül Na2CO3 im Vergleich zu einem Standard-Atom (zum Beispiel Kohlenstoff-12) 106-mal schwerer ist.
Mehr als nur eine Zahl
Okay, 106 u – das klingt jetzt vielleicht nicht nach dem spannenden Höhepunkt der Chemiegeschichte. Aber diese Zahl ist unglaublich nützlich! Sie ist wie eine Art Bauplan, der uns hilft zu verstehen, wie viel von Na2CO3 wir für bestimmte Reaktionen oder Anwendungen brauchen. Stellt euch vor, ihr müsst eine riesige Menge Waschmittel herstellen, das Na2CO3 enthält (denn das ist eine seiner vielen Anwendungen). Dank dieser molekularen Masse könnt ihr genau berechnen, wie viel ihr davon benötigt, um das perfekte Reinigungsergebnis zu erzielen. Keine Überraschungen, keine Reinigungs-Katastrophen!
Na2CO3, auch bekannt als Soda, ist ein echter Alltagsheld. Es findet sich in Waschmitteln, Glas, Papier und sogar in einigen Lebensmitteln. Es ist wie ein stiller Mitspieler in unserem Leben, der uns oft gar nicht bewusst ist. Und die molekulare Masse von 106 u ist der Schlüssel, um seine Geheimnisse zu entschlüsseln.
Die kleine Geschichte hinter dem Code
Es ist fast wie bei einem alten Familienrezept. Die molekulare Masse ist wie die Mengenangaben, die dafür sorgen, dass der Kuchen perfekt gelingt. Und so wie ein Familienrezept über Generationen weitergegeben wird, ist auch das Wissen über die molekulare Masse von Na2CO3 ein wertvolles Gut für Chemiker und Wissenschaftler auf der ganzen Welt.
Das nächste Mal, wenn ihr also eine Waschmaschine anstellt oder ein Stück Glas betrachtet, denkt daran: Hinter diesen scheinbar einfachen Dingen steckt eine ganze Welt von Molekülen und Berechnungen. Und die molekulare Masse von Na2CO3, diese unscheinbare Zahl von 106 u, ist ein kleines, aber feines Puzzleteil in diesem faszinierenden Universum der Chemie.
Also, lasst uns die Chemie feiern – nicht nur im Labor, sondern auch in unserem Alltag! Denn auch wenn wir es oft nicht merken, sie ist überall um uns herum, voller Überraschungen und kleiner, bedeutungsvoller Geheimnisse.
"Die Chemie ist die Lehre von den Stoffen, ihren Eigenschaften und ihrer Zusammensetzung sowie den Veränderungen, denen sie unterliegen." - Ein weiser Chemiker (wahrscheinlich)