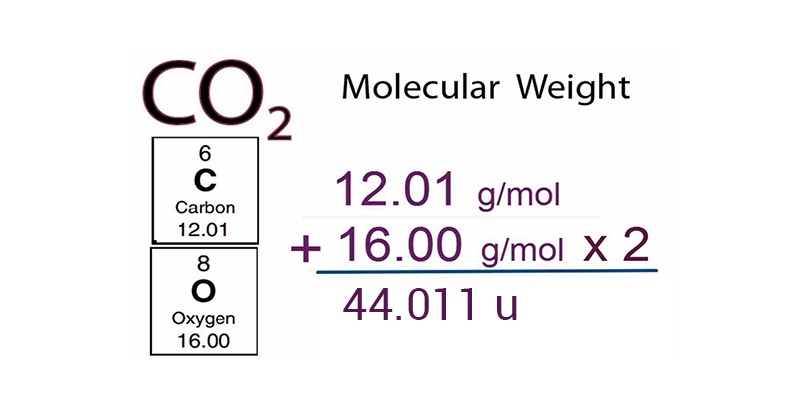
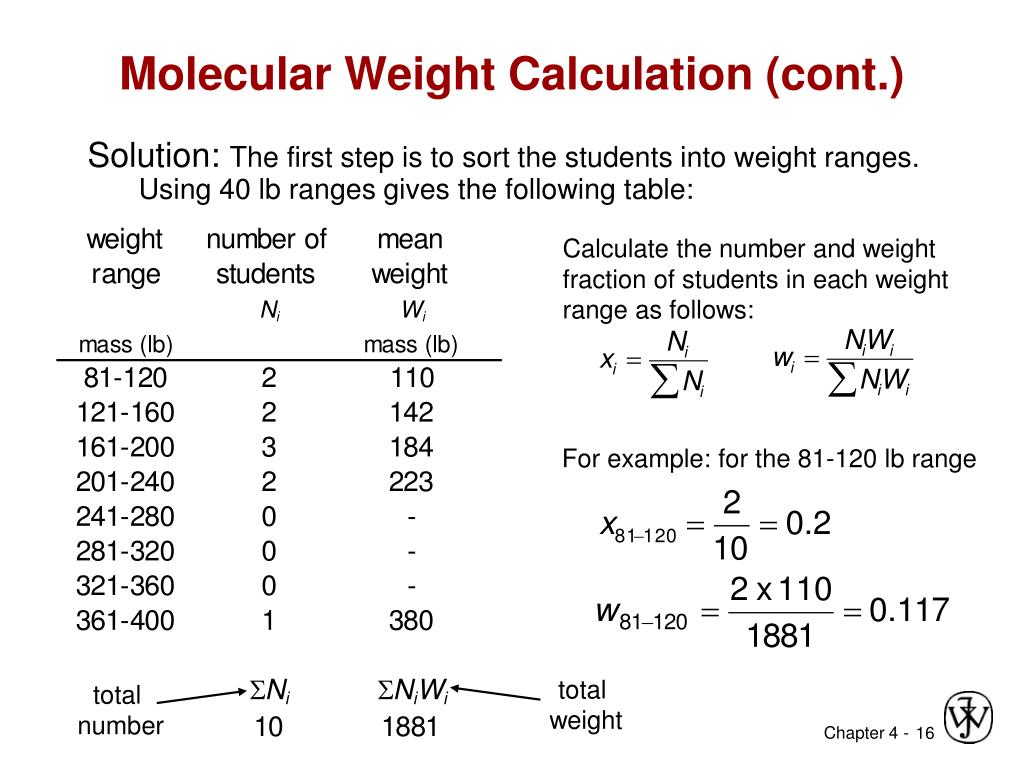
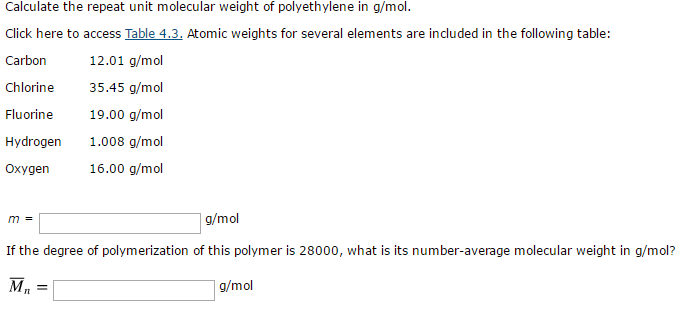Molecular Weight Unit Of Measure
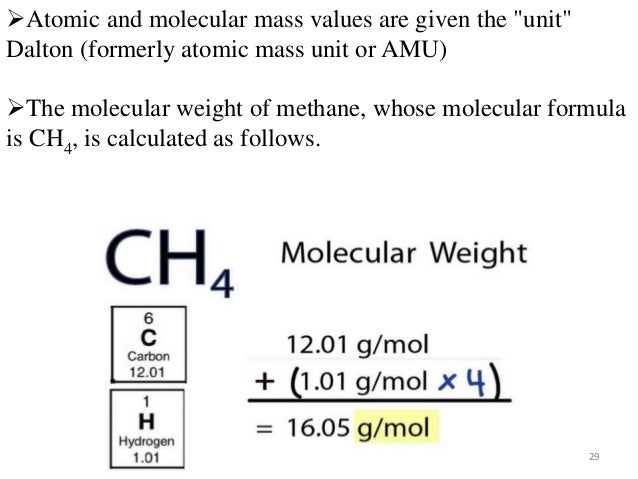
Stell dir vor, du stehst in der Küche und backst deinen Lieblingskuchen. Du nimmst Eier, Mehl, Zucker, Butter... alles nach Rezept, damit er perfekt wird. Im Grunde genommen jonglierst du mit Molekülen, auch wenn du das nicht direkt siehst! Und hier kommt die atomare Masseneinheit ins Spiel, oder wie wir sie liebevoll u nennen.
Was zum Teufel ist 'u'?
Ganz einfach: 'u' ist wie ein Super-Mini-Messlöffel für Atome und Moleküle. Atome sind winzig, wirklich winzig. So winzig, dass normale Gewichte wie Gramm oder Kilogramm völlig ungeeignet wären, um sie zu wiegen. Stell dir vor, du willst einzelne Sandkörner mit einer LKW-Waage wiegen! Lächerlich, oder? Genau deshalb brauchen wir 'u'.
Die atomare Masseneinheit ist definiert als 1/12 der Masse eines Kohlenstoff-12-Atoms. Warum gerade Kohlenstoff-12? Nun, Kohlenstoff ist ein nettes, stabiles Atom, das in allem vorkommt, von Diamanten bis zu deinem Bleistift. Es ist sozusagen der Star unter den Atomen. Also haben sich die Wissenschaftler geeinigt: "Hey, lasst uns Kohlenstoff-12 als Standard nehmen!"
Denk an 'u' als eine Art universelles Atom-Geld. Damit können wir die "Kosten" verschiedener Atome vergleichen. Ein Wasserstoffatom zum Beispiel hat eine Masse von ungefähr 1 u. Ein Sauerstoffatom wiegt etwa 16 u. Und so weiter. Mit diesen "Atom-Geldern" können wir dann Moleküle "kaufen".
Moleküle, die Stars der Chemie
Moleküle sind, im Grunde, Atome, die sich zusammengetan haben, um eine Band zu gründen. Ein Wassermolekül (H2O) besteht aus zwei Wasserstoffatomen und einem Sauerstoffatom. Um herauszufinden, wie viel ein Wassermolekül "wiegt", addieren wir einfach die Massen der einzelnen Atome: 1 u + 1 u + 16 u = 18 u. Das nennt man Molekulargewicht.
Und warum ist das Molekulargewicht wichtig? Denk an dein Kuchenrezept. Wenn du weißt, wie schwer jedes Molekül (z.B. Zucker, Mehl) ist, kannst du genau die richtige Menge abwiegen, um den perfekten Kuchen zu backen. Im Labor verwenden Chemiker das Molekulargewicht, um genau zu berechnen, wie viel von jeder Substanz sie für eine bestimmte Reaktion benötigen.
Ein bisschen Humor muss sein
Stell dir vor, du bist ein Atom, das ein Date mit einem anderen Atom hat. Du fragst: "Hey, wie viel wiegst du?" Und das andere Atom antwortet: "Oh, ich bin so um die 32 u." Ein bisschen nerdy, aber hey, jedes Atom verdient Liebe!
Und manchmal fragt man sich, ob Moleküle auch Eitelkeit besitzen. "Spiegel, Spiegel an der Wand, wer hat das größte Molekulargewicht im ganzen Land?" Wahrscheinlich irgendein riesiges Protein, das in deinem Körper herumschwirrt und dafür sorgt, dass alles reibungslos funktioniert.
'u' im Alltag: Mehr als nur Chemie
Obwohl 'u' vielleicht nach einem abstrakten Konzept klingt, beeinflusst es unser Leben auf vielfältige Weise. Pharmazeutische Unternehmen verwenden das Molekulargewicht, um die richtige Dosierung von Medikamenten zu bestimmen. Lebensmittelhersteller nutzen es, um die Zusammensetzung und Qualität ihrer Produkte zu gewährleisten. Und Wissenschaftler verwenden es, um neue Materialien mit ganz besonderen Eigenschaften zu entwickeln.
"Die Schönheit der Chemie liegt in der Einfachheit ihrer Grundlagen. Atome, Moleküle und das magische 'u', das alles zusammenhält."
Denk beim nächsten Mal, wenn du ein Etikett auf einem Lebensmittelprodukt liest oder eine Tablette einnimmst, an die kleine, aber mächtige atomare Masseneinheit. Sie ist wie ein unsichtbarer Dirigent, der die Welt der Moleküle orchestriert und sicherstellt, dass alles nach Plan verläuft.
Und wer weiß, vielleicht inspiriert dich dieses Wissen sogar, selbst zum Molekül-Dirigenten zu werden und in deiner eigenen Küche zu experimentieren. Aber bitte, verbrenne nicht das Haus! Die Feuerwehrleute haben wahrscheinlich Besseres zu tun, als sich mit Molekulargewichten auseinanderzusetzen. ;)



+A+molecular+weight+is+the+sum+of+the+atomic+weights+of+the+atoms+in+a+molecule..jpg)