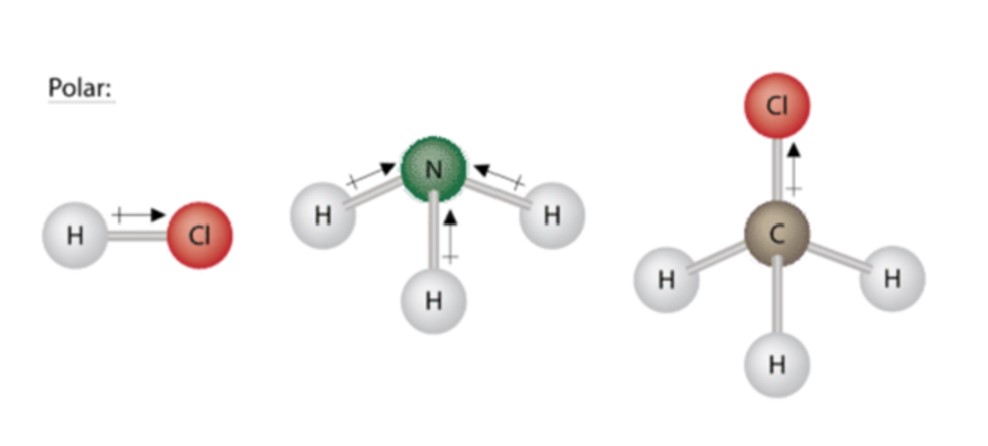
Molecules That Are Polar

Stellt euch vor, ihr seid auf einer Party. Eine Party der Moleküle! Manche Moleküle sind total ausgeglichen, chillen in der Ecke und interagieren kaum mit anderen. Das sind die unpolaren Typen. Aber dann gibt es die polarisierten Moleküle! Die sind ein bisschen wie die Leute, die immer im Mittelpunkt stehen, die eine starke Meinung haben und andere anziehen oder abstoßen. Heute geht es um diese schillernden Persönlichkeiten der molekularen Welt.
Wasser: Der Superstar unter den polaren Molekülen
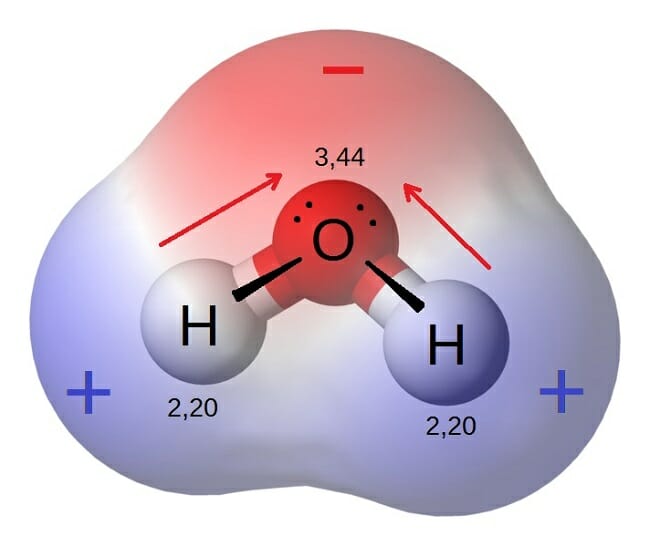
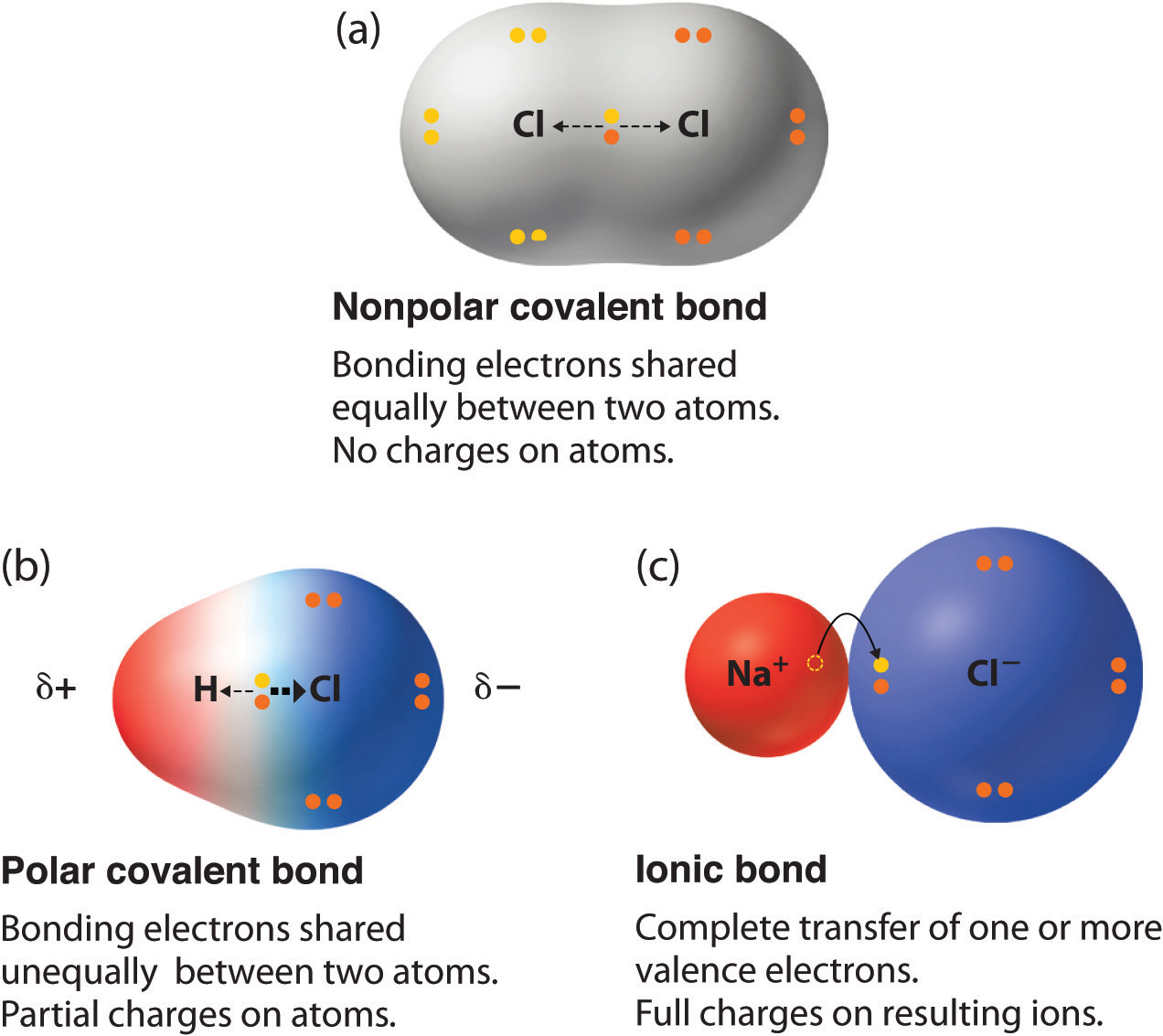
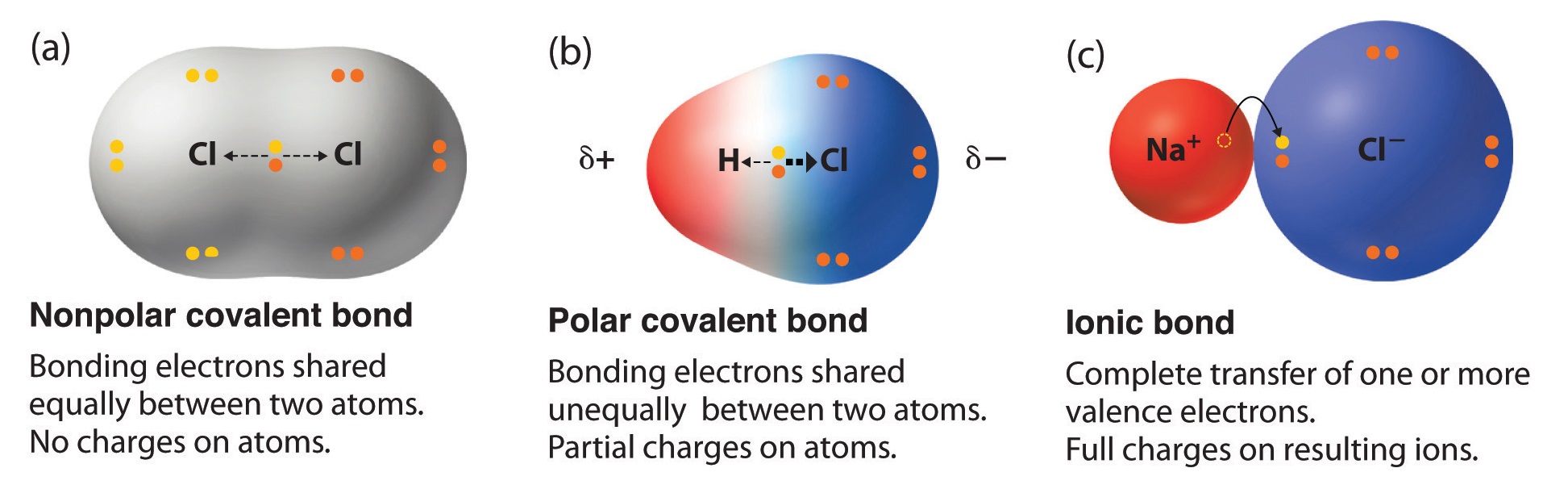
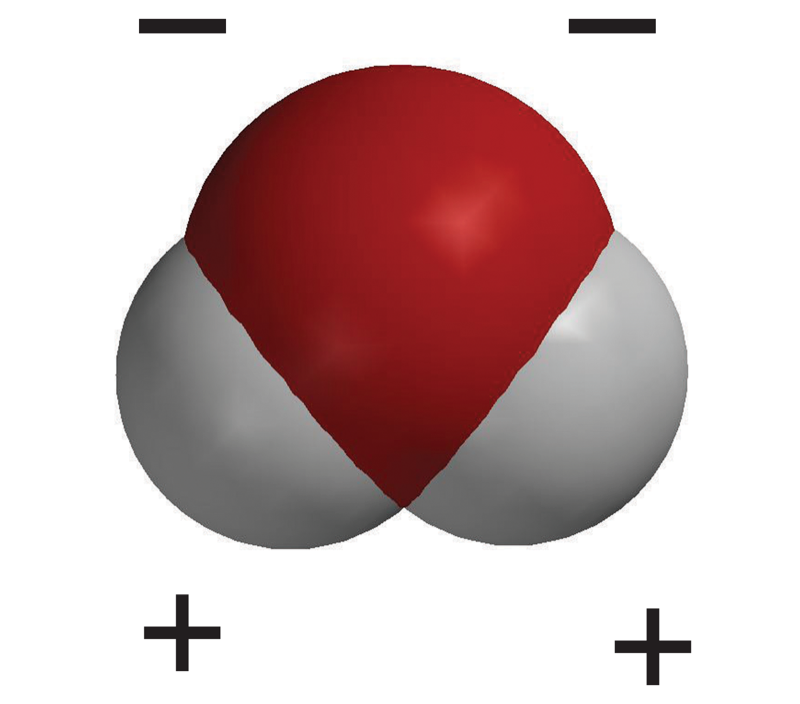
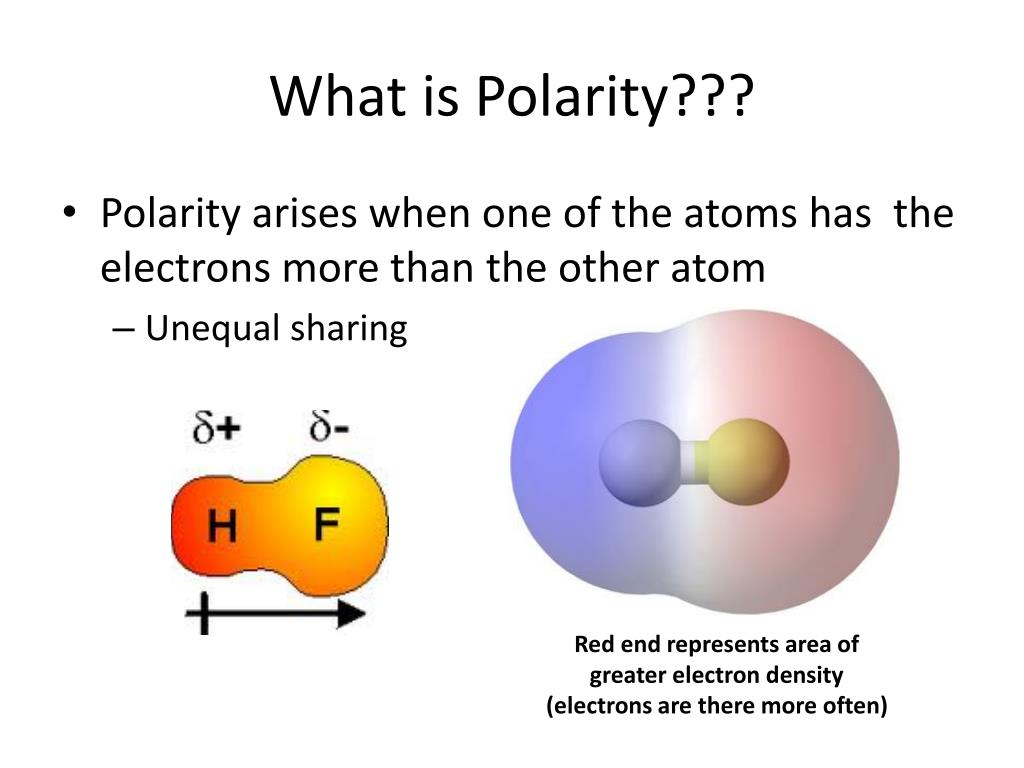
Das berühmteste Beispiel ist natürlich Wasser (H2O). Ja, das Zeug, das wir trinken, mit dem wir uns waschen und ohne das wir nicht leben könnten. Wasser ist nicht einfach nur H2O. Es ist ein kleines, elektrisches Kraftpaket! Das Sauerstoffatom zieht die Elektronen der beiden Wasserstoffatome stärker an sich. Dadurch bekommt der Sauerstoff eine leicht negative Ladung (δ-), und die Wasserstoffatome eine leicht positive Ladung (δ+). Das klingt kompliziert, ist aber wie ein kleiner Magnet. Und diese kleinen Magnete machen Wasser zu etwas Besonderem.
Denkt mal darüber nach: Wegen dieser Polarität kann Wasser so viele andere Stoffe lösen. Zucker, Salz, all das verschwindet im Wasser, weil die polaren Wassermoleküle sich an die positiv und negativ geladenen Teile dieser Stoffe klammern und sie auseinanderziehen. Wäre Wasser unpolar, wäre das Leben, wie wir es kennen, unmöglich. Kein Meer, kein Regen, keine leckere Limonade. Schreckliche Vorstellung, oder?
Und es wird noch besser! Diese polare Anziehungskraft zwischen Wassermolekülen erzeugt auch die Oberflächenspannung. Das ist der Grund, warum kleine Insekten auf dem Wasser laufen können. Sie nutzen die Anziehungskraft zwischen den Wassermolekülen an der Oberfläche aus. Faszinierend, oder? Quasi ein molekulares Trampolin!
Andere polare Chaoten
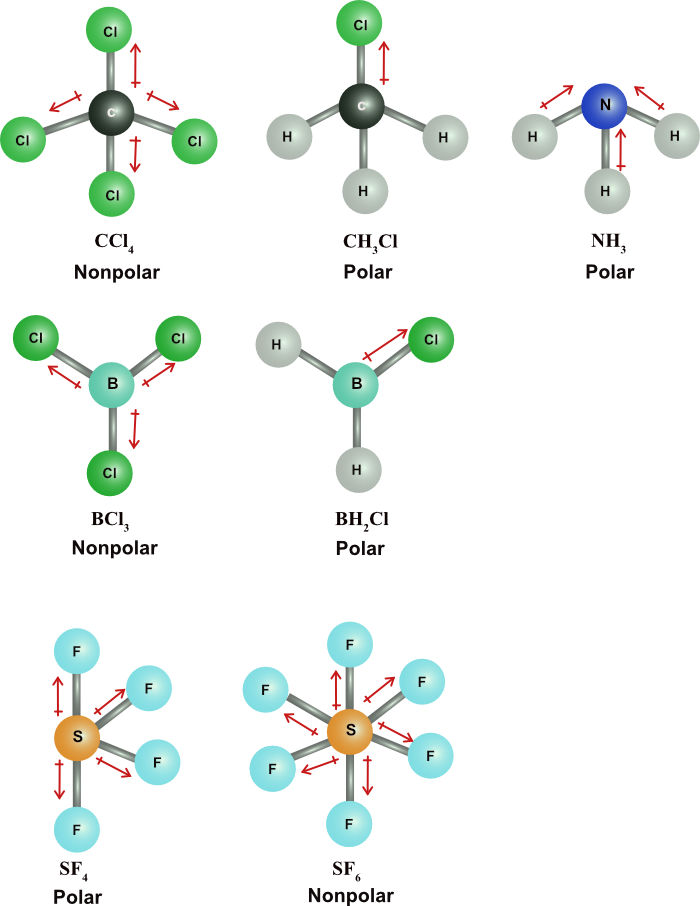
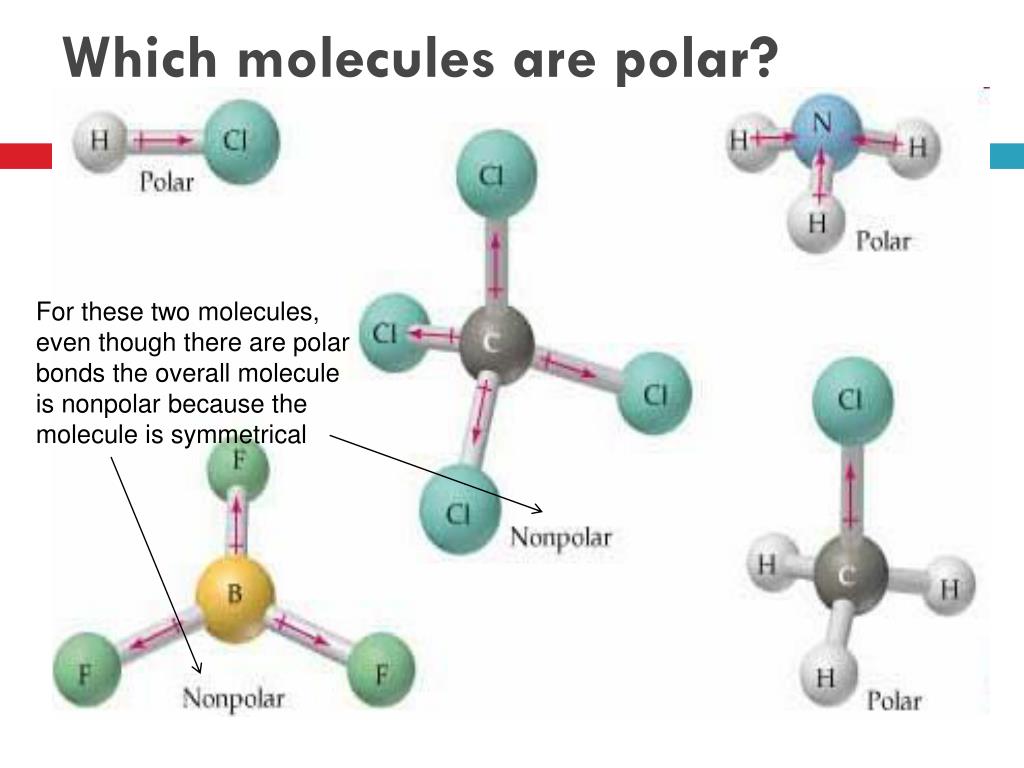
Wasser ist nicht allein. Es gibt eine ganze Reihe anderer polarer Moleküle, die unser Leben beeinflussen. Ammoniak (NH3) zum Beispiel. Das stinkt zwar zum Himmel, aber es ist ein wichtiger Bestandteil von Düngemitteln und Reinigungsmitteln. Auch Ammoniak hat ein Stickstoffatom, das die Elektronen stärker anzieht als die Wasserstoffatome. Deshalb ist auch Ammoniak polar.
Auch viele organische Moleküle sind polar. Alkohol zum Beispiel. Ja, der Alkohol in eurem Lieblingscocktail. Das Sauerstoffatom in der Hydroxylgruppe (-OH) macht auch den Alkohol polar. Deshalb mischt sich Alkohol so gut mit Wasser. Zwei polare Freunde vereint im Glas!
Die humorvolle Seite der Polarität
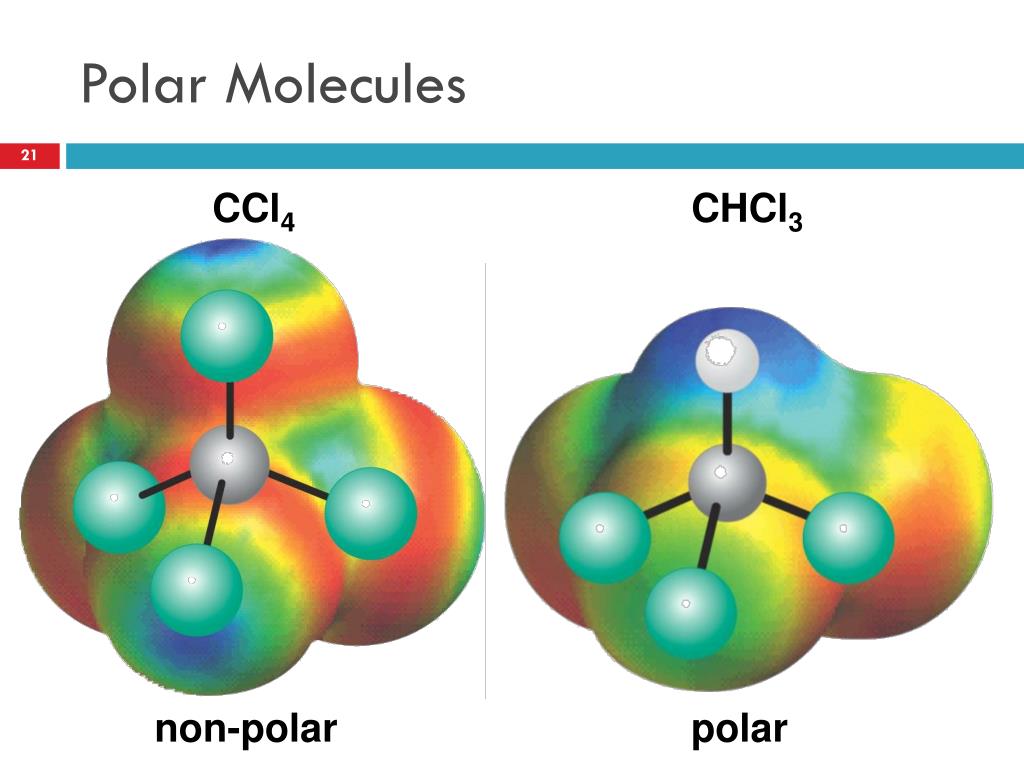
Die Polarität von Molekülen kann auch zu lustigen Situationen führen. Habt ihr euch schon mal gefragt, warum Öl und Wasser sich nicht mischen? Weil Öl hauptsächlich aus unpolaren Kohlenwasserstoffen besteht. Die unpolaren Ölmoleküle wollen nichts mit den polaren Wassermolekülen zu tun haben. Sie ziehen sich gegenseitig nicht an und trennen sich lieber. Das ist wie auf einer Party, wo die einen Leute nur mit Leuten reden, die die gleiche Musik hören, und die anderen Leute sich lieber mit anderen unterhalten.
"Polar mag polar, und unpolar mag unpolar!" könnte das Motto dieser molekularen Party lauten.
Polarität im Alltag
Wir begegnen der Polarität von Molekülen jeden Tag, oft ohne es zu merken. Zum Beispiel beim Kochen. Wenn wir Gemüse in Wasser kochen, lösen sich viele wasserlösliche Vitamine und Nährstoffe im Wasser auf, weil sie polar sind. Deshalb ist es wichtig, das Kochwasser nicht einfach wegzuschütten, sondern es für Saucen oder Suppen zu verwenden, damit man diese wertvollen Nährstoffe nicht verliert.
Auch beim Reinigen spielen polare Moleküle eine wichtige Rolle. Seife und Waschmittel enthalten Moleküle, die sowohl einen polaren als auch einen unpolaren Teil haben. Der unpolare Teil bindet an Fett und Schmutz, der polare Teil bindet an Wasser. So werden Fett und Schmutz vom Wasser weggespült. Genial, oder?
Zucker (C12H22O11) ist ein weiteres gutes Beispiel für Polarität. Dank der vielen OH-Gruppen ist Zucker sehr polar und löst sich daher sehr gut in Wasser. Das ist auch der Grund, warum wir Zucker in Kaffee oder Tee rühren können.
Eine Welt voller Anziehung und Abstoßung
Die Polarität von Molekülen ist ein faszinierendes Phänomen, das unser Leben in vielerlei Hinsicht beeinflusst. Von der Art und Weise, wie Wasser Stoffe löst, bis hin zur Reinigung unserer Kleidung. Die kleinen elektrischen Ladungen in Molekülen bestimmen, wie sie miteinander interagieren und welche Eigenschaften sie haben. Es ist eine Welt voller Anziehung und Abstoßung, die uns jeden Tag umgibt.
Denkt beim nächsten Mal, wenn ihr ein Glas Wasser trinkt oder euch die Hände wascht, daran: Ihr interagiert mit kleinen, polarisierten Magneten, die das Leben, wie wir es kennen, erst möglich machen. Die unsichtbare Welt der Moleküle ist voller Überraschungen und Wunder. Und das ist doch wirklich etwas, worüber man sich freuen kann!