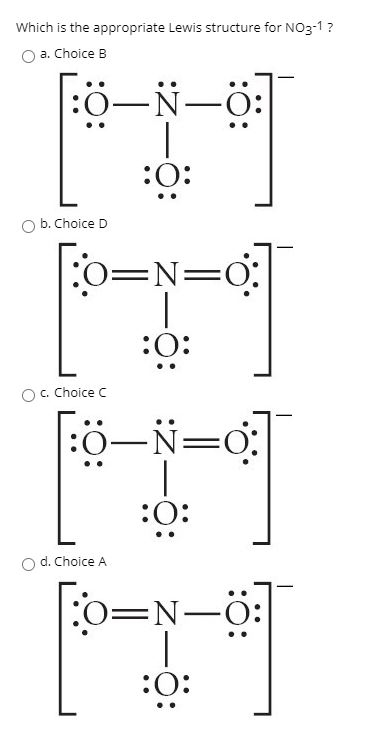
No3 Structure Lewis Dot
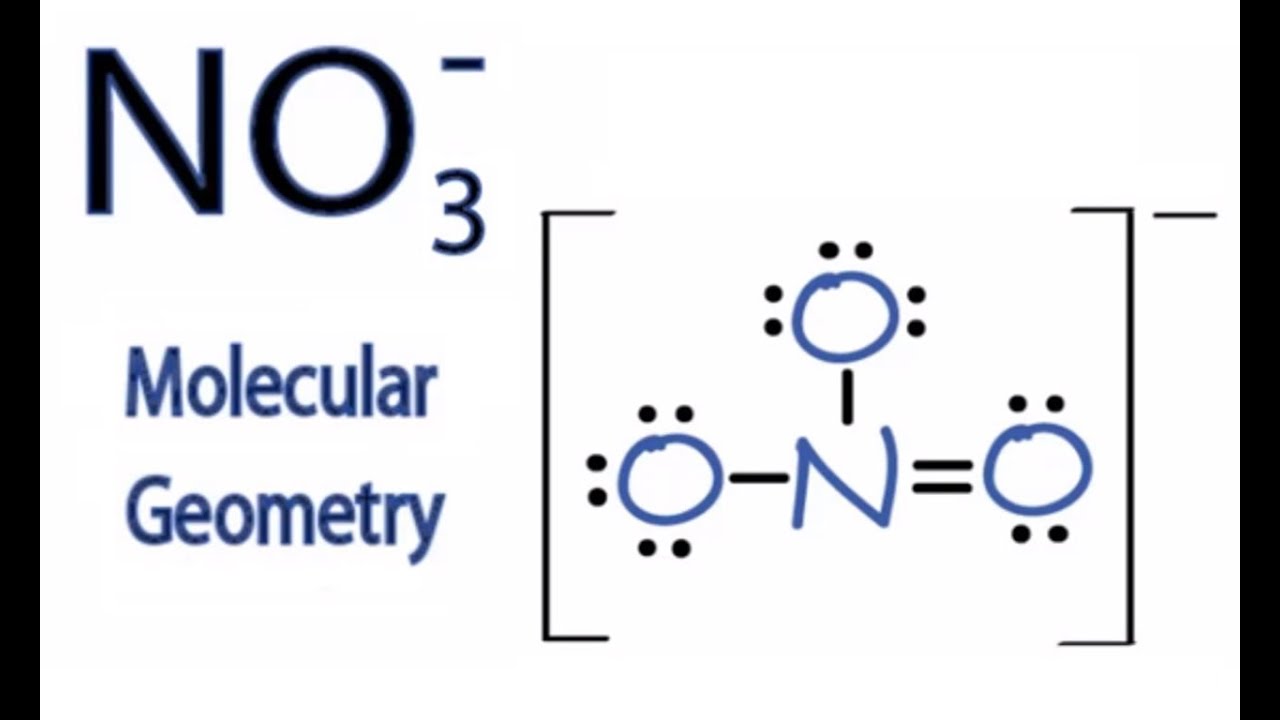
Stellt euch vor, ihr seid auf einer Geburtstagsparty. Es gibt drei Kids, die unbedingt zusammengehören: Drei O's, Sauerstoffatome, total aufgedreht, weil es Kuchen gibt. Aber da ist noch ein Kind, Stickstoff, N, ein bisschen der introvertierte Typ, der eigentlich nur in Ruhe malen will.
Die O's sind so energetisch, dass sie N fast schon belästigen. Sie brauchen irgendwas, um ihre Energie loszuwerden, irgendwelche Verbindungen, um sich auszutoben. Und hier kommt das ganze Lewis-Punkt-System ins Spiel, quasi das Partyspiel, das die Erwachsenen (die Chemiker) erfunden haben, um sicherzustellen, dass keiner ausrastet. Stell dir vor, jeder Punkt ist ein Keks, und jedes Atom will so viele Kekse wie möglich, um glücklich zu sein. (Okay, vielleicht ist die Analogie nicht perfekt, aber bleibt dran!)
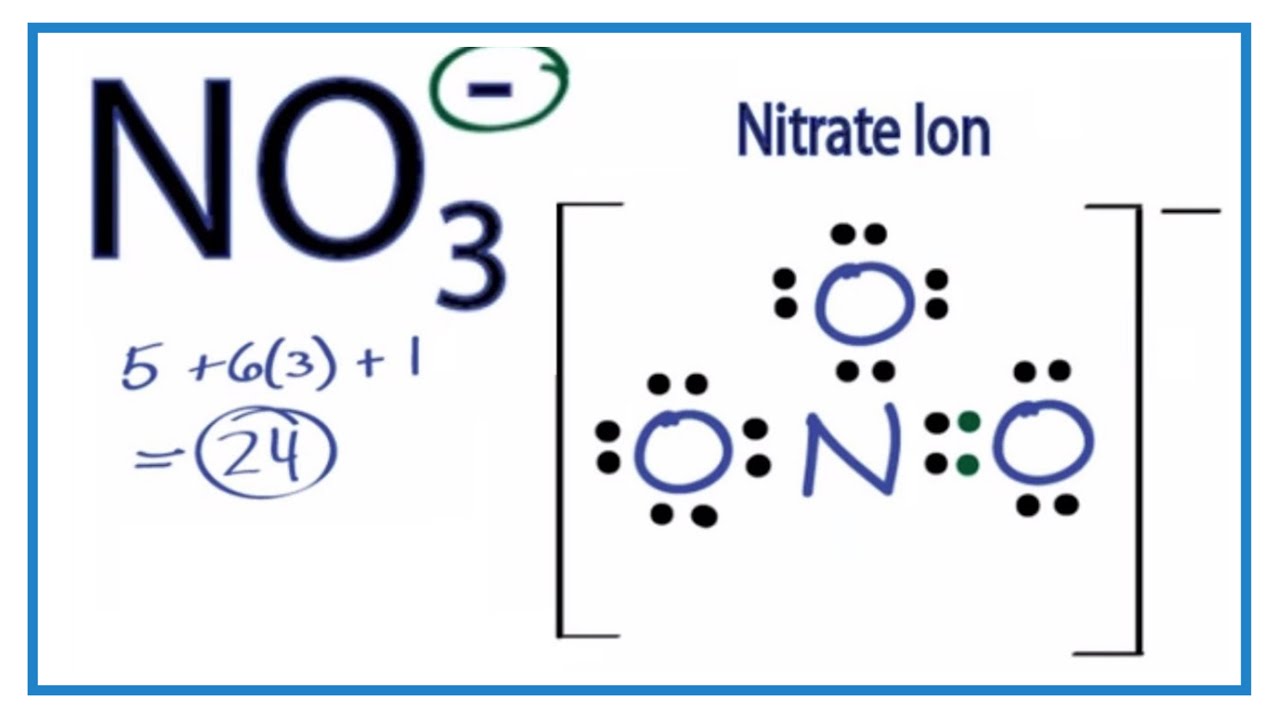
N, der Stickstoff, hat fünf Kekse in seiner Keksdose (fünf Valenzelektronen, falls ihr es super-wissenschaftlich wollt). Jedes O, Sauerstoff, hat sechs. Jetzt geht's los: Wer kriegt wie viele Kekse, und wie stellen wir sicher, dass alle happy sind?
Das Drama beginnt!
Die Lösung ist, dass N sich mit jedem O irgendwie "verbinden" muss. Aber O ist ein kleiner Drama-Queen (oder Drama-King, wer weiß!), und will am liebsten zwei Verbindungen eingehen. Erinnert euch an die Kekse: O will acht Kekse insgesamt! N ist da ein bisschen flexibler, aber auch er will am Ende nicht zu kurz kommen.
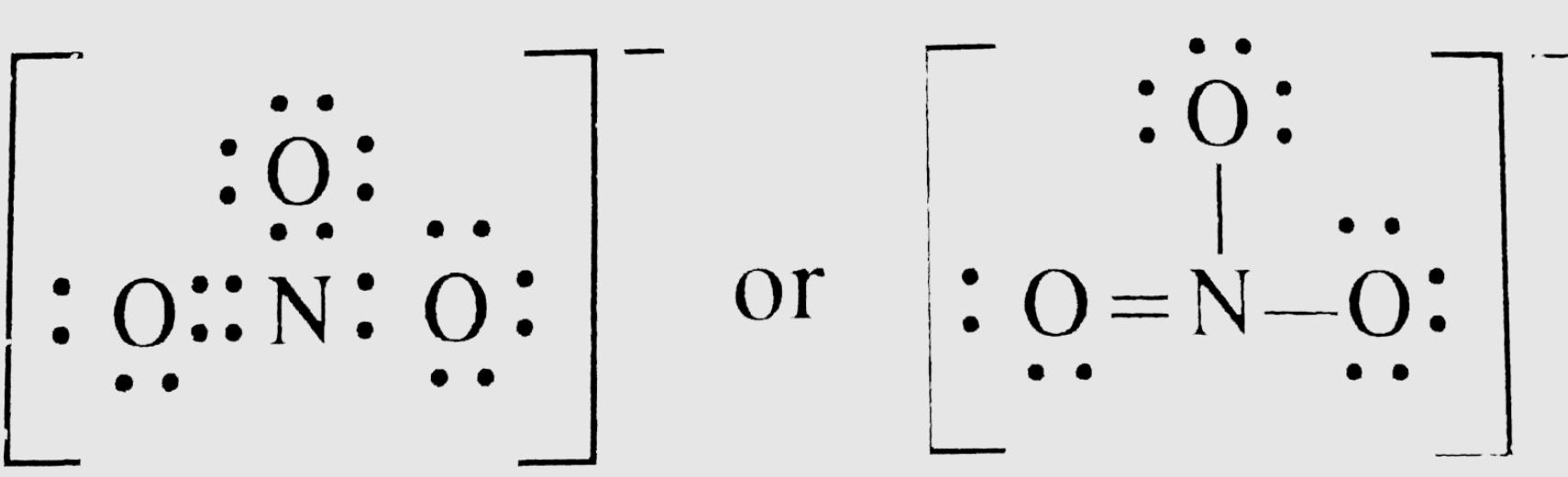
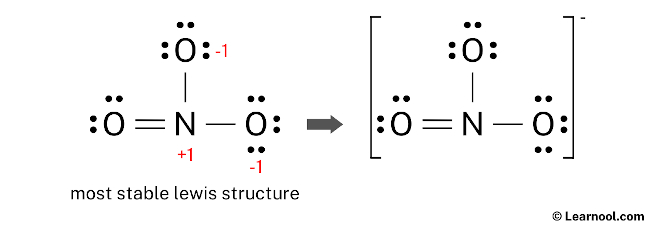
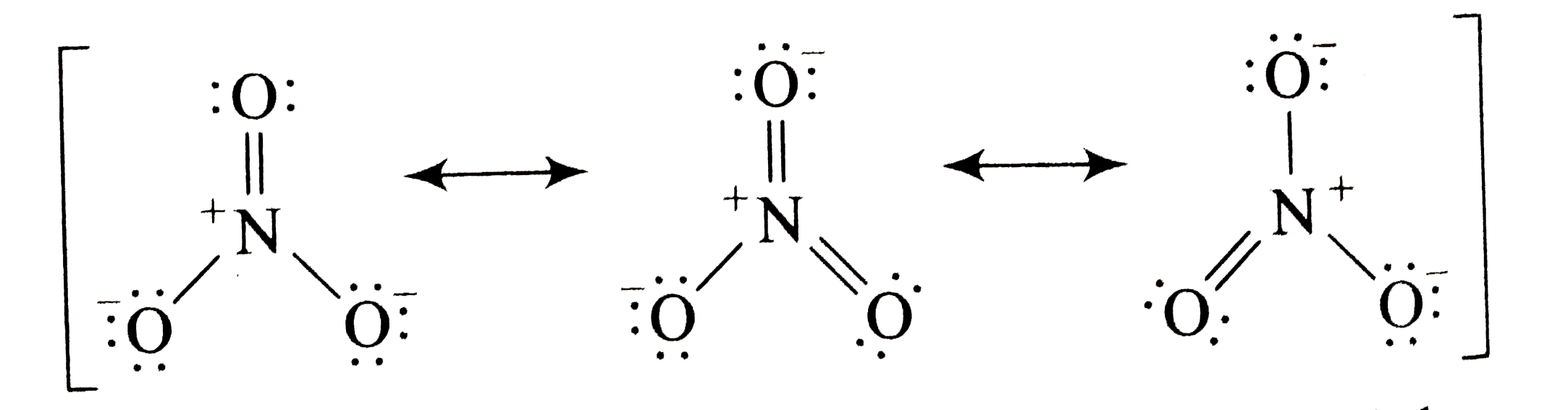
Das führt zu einer ziemlich ungeraden Situation. Eines der O's könnte sagen: "Hey N, ich nehme mir zwei deiner Kekse, dann sind wir beide zufrieden!" Das nennt man eine Doppelbindung. Und dann ist da noch ein anderes O, das sagt: "N, ich nehme nur einen Keks, okay? Ich bin nicht so gierig." Das ist eine Einfachbindung. Aber jetzt kommt der Knackpunkt:
Die Sache mit der Ladung
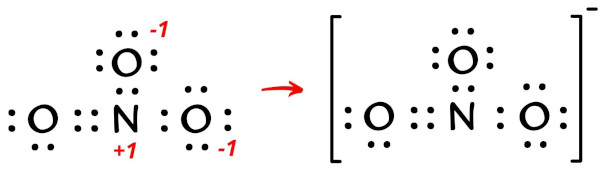
Weil das alles nicht so ganz aufgeht, bekommt das O mit der Einfachbindung eine kleine Minuskraft zugewiesen. Stell dir vor, es hat einen kleinen unsichtbaren Magneten, der sagt: "Ich hätte gern noch mehr Kekse!" Das ist die negative Ladung. Das ganze NO3-Molekül hat also insgesamt auch eine negative Ladung. Das ist so, als hätte die ganze Party eine winzige elektrostatische Aufladung, weil einer der Gäste etwas neidisch auf die anderen schaut. Chemisch gesehen ist das superwichtig, weil es bestimmt, wie das Molekül mit anderen Molekülen interagiert.
Das dritte O, das nur so rumsitzt und anscheinend gar nichts tut? Nun, das ist auch irgendwie eingebunden. Alle drei O's sind gleichwertig, auch wenn es auf dem Papier so aussieht, als ob eines eine Doppelbindung und eines eine Einfachbindung hat. In Wahrheit "schwingt" die Bindung hin und her, wie ein Staffelstab bei einem Staffellauf. Das nennt man Resonanz. Klingt dramatisch, ist aber einfach nur ein Ausgleich von Elektronen.
Man könnte sich das so vorstellen: Die O's machen ein Fingerspiel, bei dem sie sich abwechselnd mehr oder weniger Kekse zustecken. N in der Mitte ist der Dirigent dieses Kekse-Balletts.
Warum ist das wichtig?
Jetzt fragt ihr euch vielleicht: "Okay, Kekse, Geburtstagsparty, Fingerspiele... und was hat das mit meinem Leben zu tun?" Nun, NO3 ist ein ziemlich wichtiger Baustein in der Natur. Es kommt in Düngemitteln vor, hilft Pflanzen zu wachsen und spielt eine Rolle im Stickstoffkreislauf. Und dieser Stickstoffkreislauf ist essenziell für das Leben auf der Erde, denn ohne Stickstoff kein Leben, oder zumindest keins, wie wir es kennen!
Also, das nächste Mal, wenn ihr Dünger auf eure Blumen streut, denkt an die kleine, chaotische NO3-Party, an die Kekse, die umhergehen, und an N, den Stickstoff, der versucht, den Überblick zu behalten. Und denkt daran, dass selbst die kleinsten Moleküle ihre eigenen kleinen Dramen haben. Oder, um es mit den Worten eines berühmten Chemikers (wahrscheinlich) zu sagen: "Selbst ein kleines NO3 kann die Welt verändern!"
Das Tolle an der Chemie ist ja, dass sie uns zeigt, dass selbst Dinge, die unsichtbar sind, eine unglaublich komplexe und faszinierende Welt verbergen.
Und wer weiß, vielleicht ist ja die nächste große wissenschaftliche Entdeckung nur eine Frage der richtigen Kekse-Verteilung...
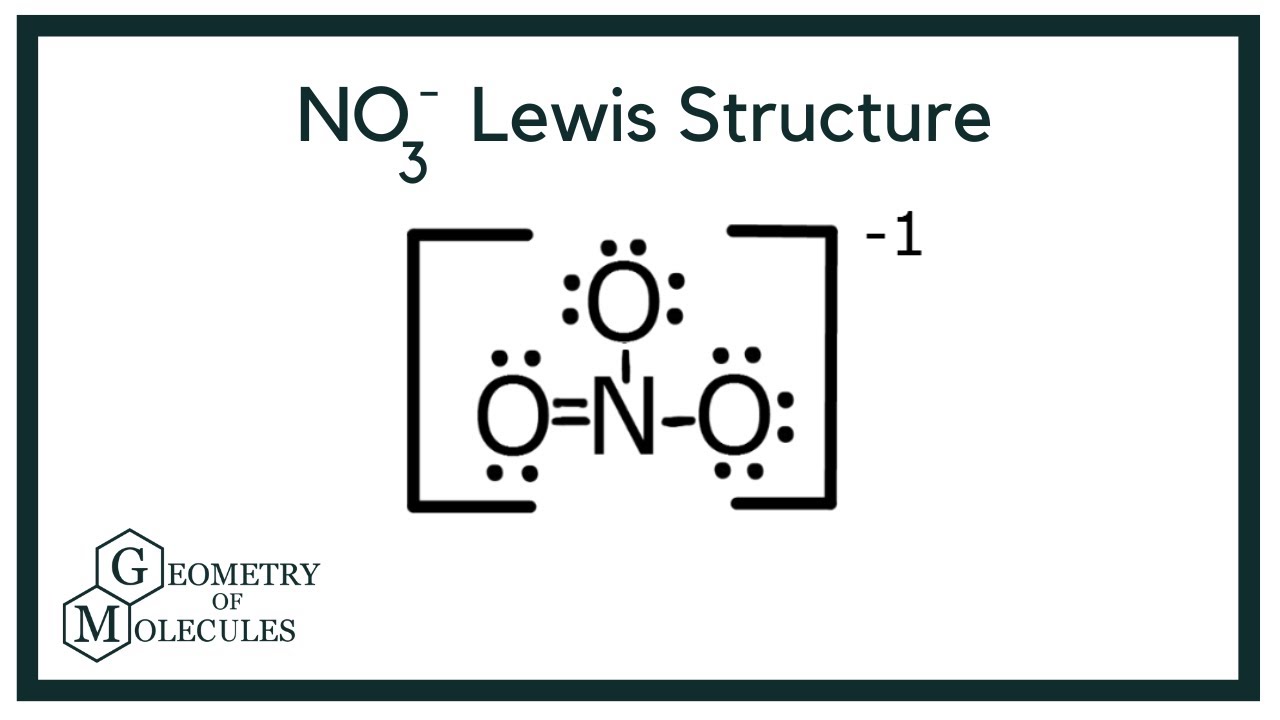


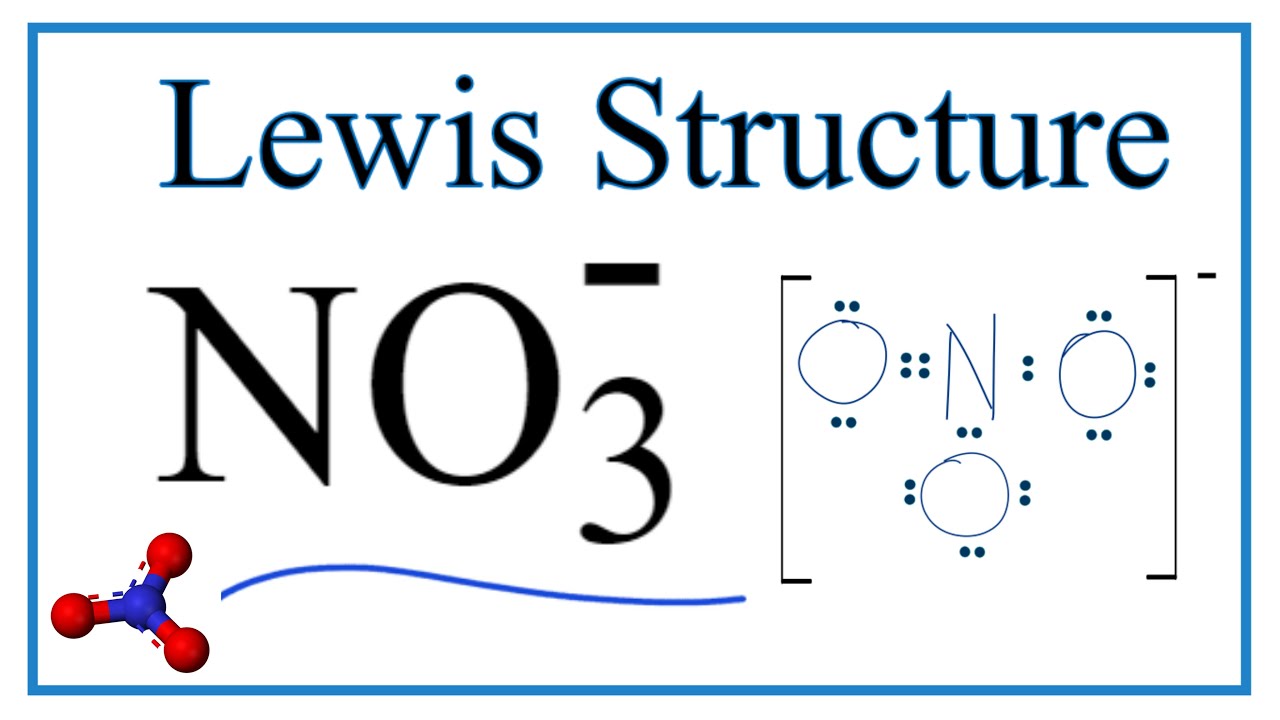

![No3 Structure Lewis Dot [DIAGRAM] Lewis Diagram No3 - MYDIAGRAM.ONLINE](https://cdn1.byjus.com/wp-content/uploads/2019/07/hybridization-of-no3-ion.png)





![No3 Structure Lewis Dot No3 Lewis Structure How To Draw The Lewis Structure For Solved]](https://eightfoldlearning.com/wp-content/uploads/2020/10/NO3-final-lewis-1022x1024.png)