Reaktionsgleichung Salzsäure Und Magnesium

Habt ihr euch jemals gefragt, was passiert, wenn man etwas wirklich Sprudelndes mit etwas Metallischem vermischt? Ich rede hier nicht von einer Cola mit Löffel (das gibt höchstens eine klebrige Sauerei), sondern von etwas... Wissenschaftlicherem! Und zwar von der legendären Reaktionsgleichung Salzsäure und Magnesium. Klingt kompliziert? Keine Sorge, wir machen das Ganze zu einem spaßigen Chemie-Happening!
Die Zutaten: Salzsäure und Magnesium – Ein ungleiches Paar
Stellt euch vor: Wir haben da Salzsäure (HCl). Die kennen manche vielleicht aus dem Chemieunterricht oder vom Entfernen von Kalkablagerungen – Achtung, ist ätzend, also Finger weg, wenn ihr nicht wisst, was ihr tut! Salzsäure ist quasi die Diva unter den Säuren, immer bereit, etwas aufzumischen. Und dann haben wir Magnesium (Mg), ein silbrig-weißes Metall, das in vielen Dingen vorkommt, sogar in manchen Nahrungsergänzungsmitteln. Magnesium ist eher der ruhige Typ, aber lasst euch nicht täuschen, der hat es faustdick hinter den Ohren!
Das Knistern und Zischen: Die Reaktion in Aktion
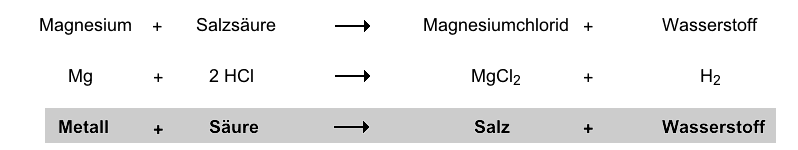
Was passiert also, wenn diese beiden aufeinandertreffen? Nun, dann geht die Post ab! Stellt euch vor, ihr werft einen Eiswürfel in eine heiße Pfanne – es zischt, knistert und dampft. So ähnlich ist das auch hier, nur eben auf chemisch! Das Magnesium-Metall wird von der Salzsäure angegriffen. Die Salzsäure ist wie ein hyperaktiver Staubsauger, der die Magnesiumatome förmlich aus dem Metall herauszieht. Dabei entstehen zwei Dinge: Magnesiumchlorid (MgCl2) und – jetzt kommt der Clou – Wasserstoffgas (H2)!
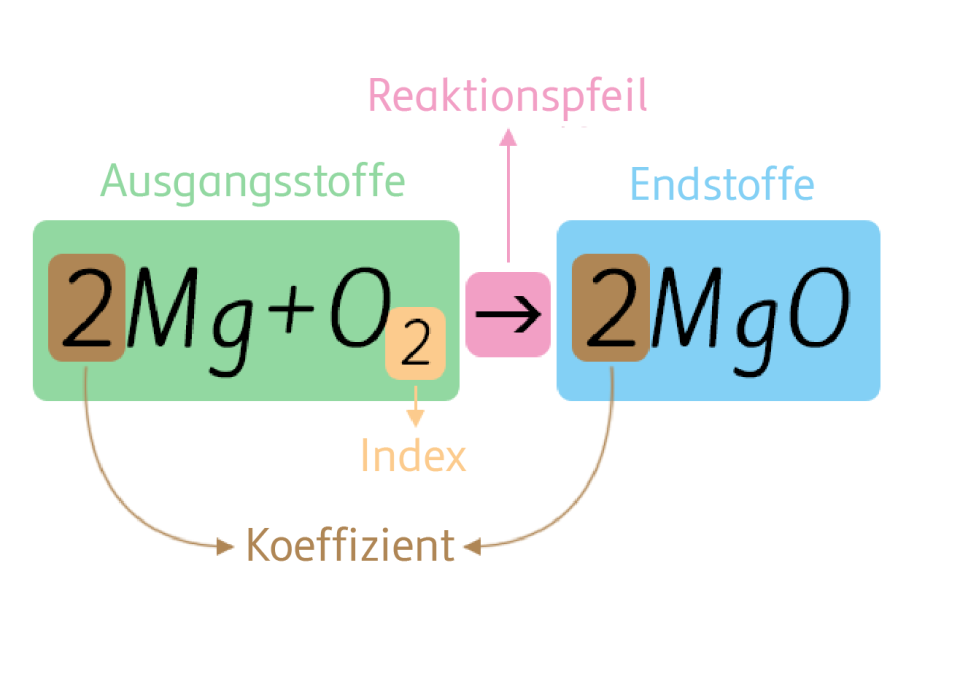
Die eigentliche Reaktionsgleichung lautet: Mg + 2 HCl → MgCl2 + H2. Einfach, oder?
Das Wasserstoffgas ist der Star der Show! Es ist nämlich brennbar. Wenn man also eine kleine Flamme in die Nähe des entstehenden Gases hält (Vorsicht! Nur unter Aufsicht von Erwachsenen und mit den nötigen Sicherheitsvorkehrungen!), gibt es einen kleinen Knall – ein sogenanntes "Knallgasprobe". Das ist der Beweis, dass Wasserstoff entstanden ist! Stell dir vor, du bist ein kleiner Chemiker und hast gerade eine Mini-Explosion verursacht! (Aber bitte, bitte, seid vorsichtig damit!)
Magnesiumchlorid: Der unscheinbare Held
Und was ist mit dem Magnesiumchlorid? Das ist sozusagen der unscheinbare Held dieser Geschichte. Es löst sich im Wasser und ist farblos. Im Prinzip ist es nichts anderes als ein Salz, ähnlich wie Kochsalz, nur eben mit Magnesium statt Natrium. Es ist nicht so spektakulär wie das Wasserstoffgas, aber es ist ein wichtiger Teil der Reaktion.
Alltagstaugliche Analogien: Chemie ist überall!
Okay, Salzsäure und Magnesium klingen jetzt vielleicht immer noch nach Labor und Reagenzgläsern. Aber Chemie ist überall um uns herum! Denkt mal an Folgendes: Wenn ihr eine Brausetablette in Wasser werft, sprudelt es auch. Das ist auch eine chemische Reaktion, nur eben eine andere. Oder wenn ihr Backpulver und Essig mischt, gibt es auch ein Zischen und Schäumen. Chemie ist wie Magie, nur eben mit Regeln und Formeln! Und die Reaktionsgleichung Salzsäure und Magnesium ist nur eine von unzähligen spannenden chemischen Reaktionen, die jeden Tag um uns herum stattfinden.
Warum das Ganze so faszinierend ist
Das Faszinierende an dieser Reaktion ist, dass man mit bloßem Auge sehen kann, wie sich etwas verändert. Man sieht, wie das Metall verschwindet, wie Gasbläschen aufsteigen und man kann sogar den Wasserstoff "testen". Es ist wie ein kleines Experiment, das man zu Hause machen kann (aber eben nur unter Aufsicht und mit den nötigen Sicherheitsvorkehrungen!). Und es zeigt uns, dass die Welt um uns herum voller Überraschungen steckt. Chemie ist nicht nur etwas für Nerds im Labor, sondern etwas, das uns alle betrifft und faszinieren kann!
Also, das nächste Mal, wenn ihr etwas Sprudelndes seht oder ein Metallstück in der Hand haltet, denkt an die Reaktionsgleichung Salzsäure und Magnesium! Vielleicht entdeckt ihr ja eure eigene Begeisterung für die Welt der Chemie!