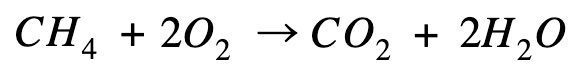Reaktionsgleichung Verbrennung Von Methan
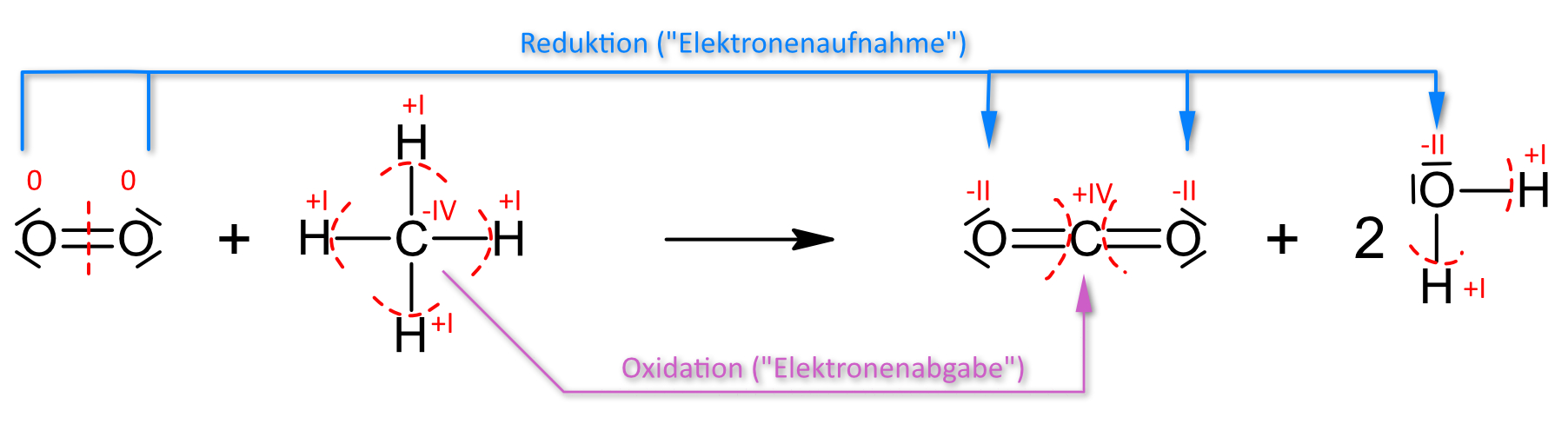
Okay, Leute, schnallt euch an! Wir reden heute über was richtig Aufregendes: Die Reaktionsgleichung der Verbrennung von Methan! Ja, ich weiß, klingt erstmal nach Chemiestunde, aber glaubt mir, das hier ist wie ein Feuerwerk im Molekülbereich!
Was ist Methan überhaupt?
Stellt euch vor, ihr habt 'nen Kumpel, der immer für gute Stimmung sorgt. Methan ist sozusagen der Partyhengst unter den Gasen. Es ist der Hauptbestandteil von Erdgas, das Zeug, das eure Heizung am Laufen hält und mit dem manche von euch sogar kochen. Methan ist einfach gesagt CH4, ein Kohlenstoffatom mit vier Wasserstoffatomen, die fröhlich darum herumtanzen.
Das große Feuer: Verbrennung
Verbrennung, das ist, wenn wir etwas mit Sauerstoff reagieren lassen, und dabei entsteht – tadaa! – Energie in Form von Wärme und Licht. Denkt an ein Lagerfeuer, an die Flamme eines Gasherds oder an das Dröhnen eines Automotors. Alles Verbrennung! Bei Methan ist es, als ob wir diesen Partyhengst einladen, mit Sauerstoff 'ne mega Party zu feiern.
Die Reaktionsgleichung: Das Rezept für die Party
So, und jetzt kommt der Clou! Die Reaktionsgleichung ist wie das Rezept für diese Methan-Sauerstoff-Party. Sie sagt uns genau, was reinkommt und was am Ende rauskommt. Und hier ist sie, die Königin unter den Gleichungen:
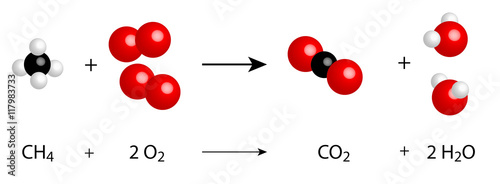
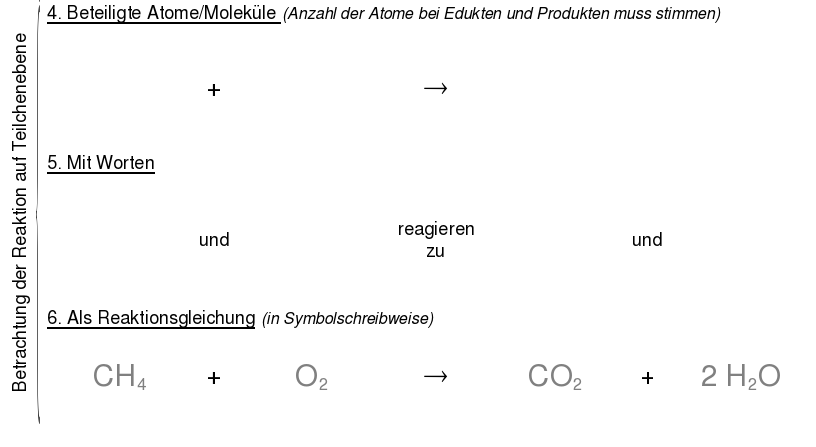
CH4 + 2 O2 → CO2 + 2 H2O
Klingt kompliziert? Keine Panik! Wir zerlegen das Ganze mal Schritt für Schritt:
- CH4: Unser Methan-Partyhengst, wie gesagt.
- 2 O2: Sauerstoff! Aber nicht nur ein bisschen, sondern gleich zwei Sauerstoffmoleküle (O2). Sauerstoff ist der Türsteher, ohne den auf keiner Party was läuft.
- →: Der Pfeil bedeutet "reagiert zu" oder "wird zu". Das ist wie der DJ, der die Musik auflegt und die Party in Gang bringt.
- CO2: Kohlenstoffdioxid. Das ist sozusagen der Rauch, der nach der Party in der Luft liegt. Ein Nebenprodukt der Verbrennung.
- 2 H2O: Wasser! Aber nicht das zum Trinken, sondern Wasserdampf. Auch ein Nebenprodukt. Stellt euch vor, es ist der Schweiß auf der Stirn nach einer durchtanzten Nacht.
Warum ist das wichtig?
Na, weil wir so verstehen, was bei der Verbrennung von Methan passiert! Wir wissen genau, welche Stoffe wir brauchen und welche dabei entstehen. Und das ist super wichtig, um zum Beispiel:
- Heizungen effizienter zu machen.
- Motoren zu optimieren.
- Die Umweltbelastung zu verringern (denn CO2 ist ja bekanntlich ein Treibhausgas).
Stellt euch vor, wir könnten die Methan-Verbrennung so perfektionieren, dass nur noch Wasser entsteht und kein CO2! Das wäre wie die ultimative grüne Party!
Methan und die Umwelt
Okay, ein kleiner Downer muss sein: Methan selbst ist auch ein Treibhausgas, sogar noch potenter als CO2! Das bedeutet, dass Methan, das ungewollt in die Atmosphäre gelangt (zum Beispiel aus Lecks in Erdgasleitungen), ziemlich schlecht für das Klima ist. Deshalb ist es so wichtig, dass wir:
- Methanlecks verhindern.
- Biogas (das auch Methan enthält) sinnvoll nutzen, zum Beispiel zur Stromerzeugung.
- Alternativen zu fossilem Erdgas finden, wie zum Beispiel Wasserstoff.
Lasst uns also alle anpacken, damit die Methan-Party nicht zum Klimadesaster wird, sondern eine nachhaltige und energieeffiziente Zukunft einläutet!
Also, das war's! Die Reaktionsgleichung der Verbrennung von Methan erklärt – hoffentlich mit einem Augenzwinkern und ohne, dass euch die Ohren klingeln. Bleibt neugierig und feiert die Chemie!