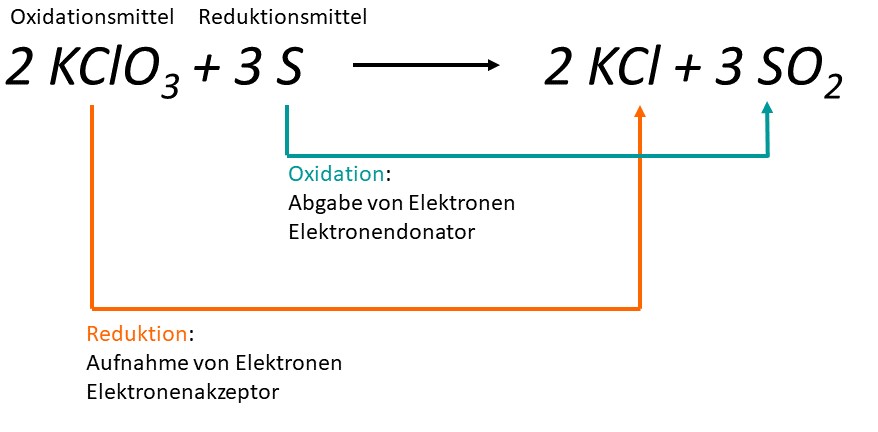
Redoxreaktion Magnesium Und Sauerstoff
Habt ihr euch jemals gefragt, was passiert, wenn man ein Stück Magnesium anzündet? Also, nicht wirklich angezündet im Sinne von "Ups, die Küche brennt!", sondern eher so im kontrollierten, wissenschaftlichen "Oooh, das ist ja cool!"-Sinn. Ich rede von dieser strahlenden, blendenden Helligkeit, die fast schon magisch wirkt. Dahinter steckt eine verdammt coole Geschichte, und die hat mit Redoxreaktionen zu tun!
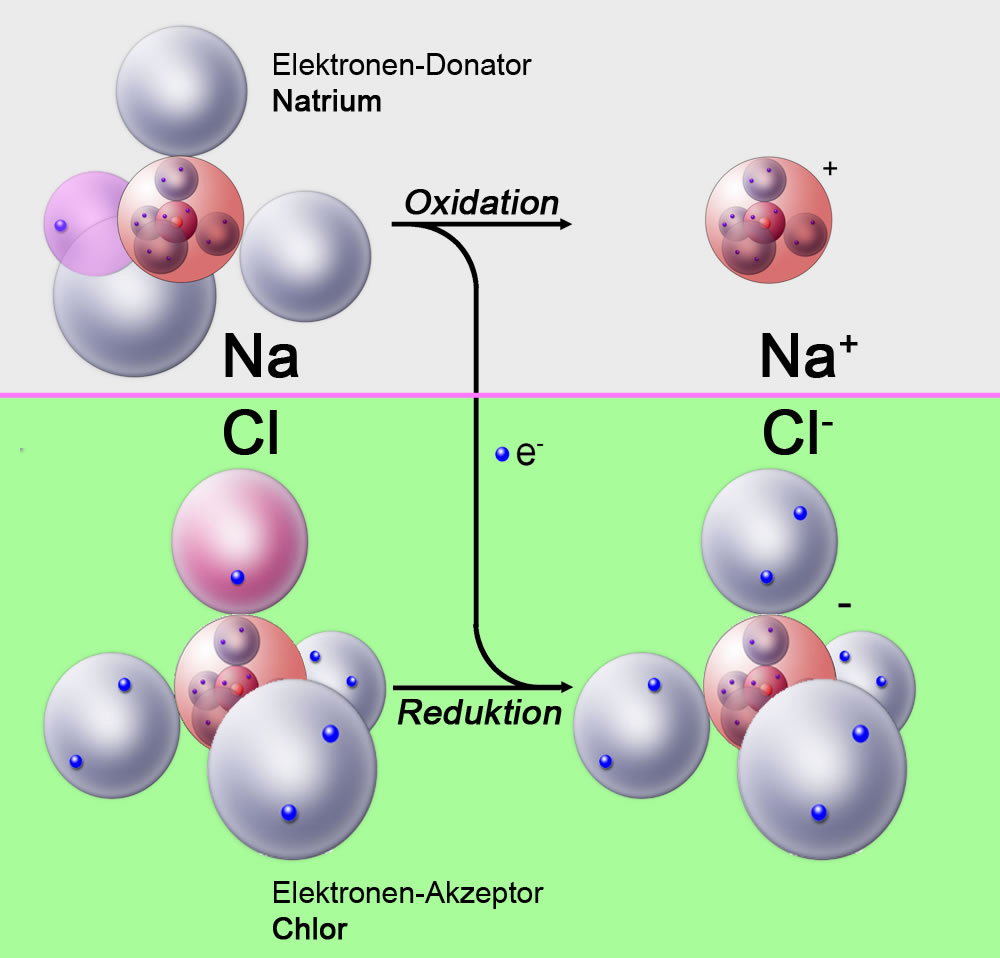
Klingt kompliziert? Keine Sorge, wir machen’s zum Kinderspiel. Stellt euch vor, Magnesium ist ein Typ, der total gerne Sachen verschenkt. In diesem Fall sind die "Sachen" Elektronen. Und Sauerstoff? Der ist ein bisschen wie ein Sammler. Er liebt es, Elektronen zu bekommen. Das ist die perfekte Chemie, oder?
Das große Geschenk: Magnesium gibt Elektronen ab
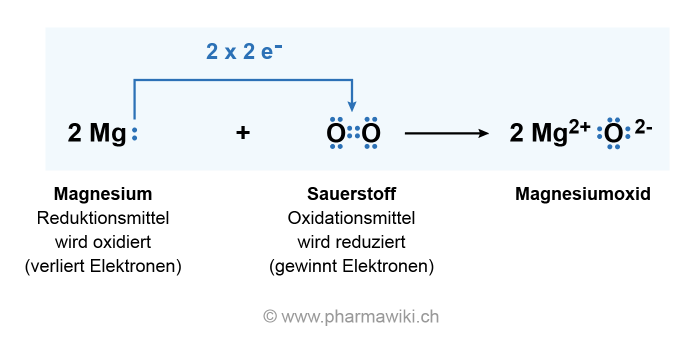
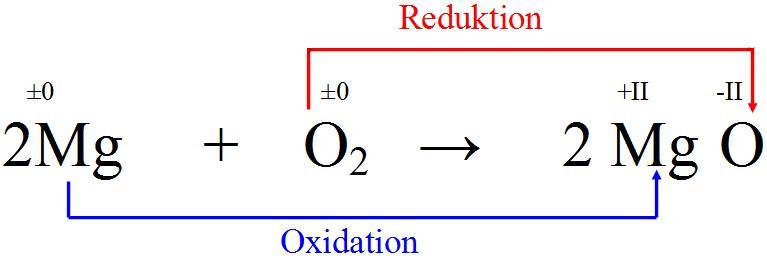
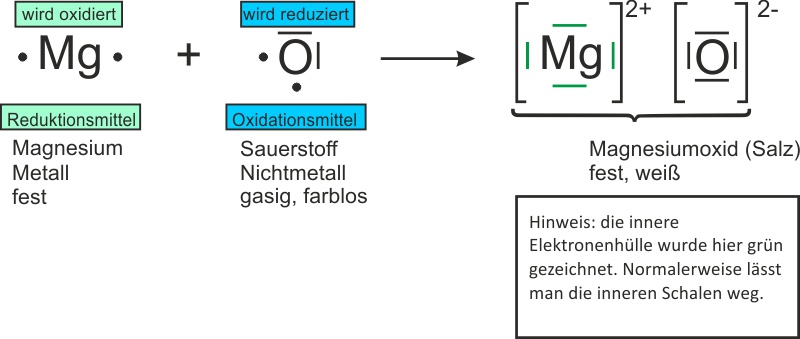
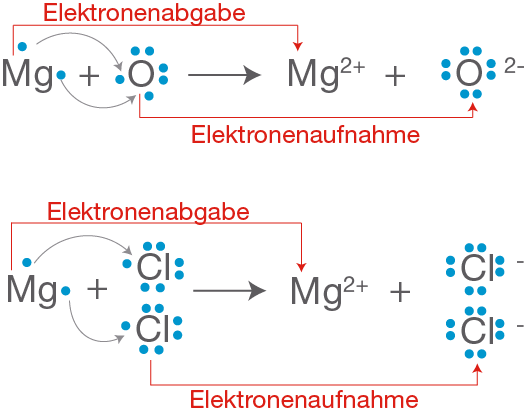
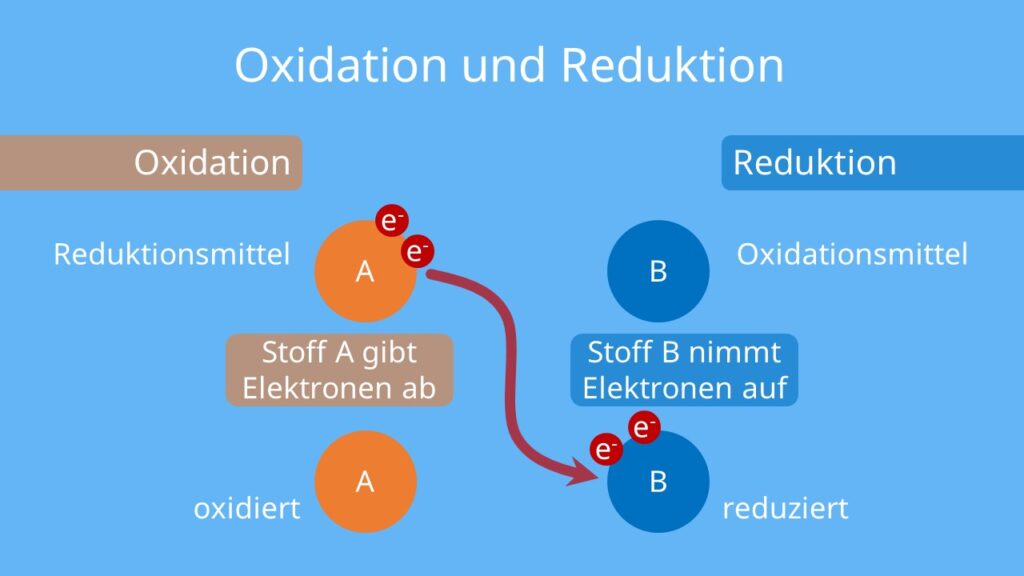
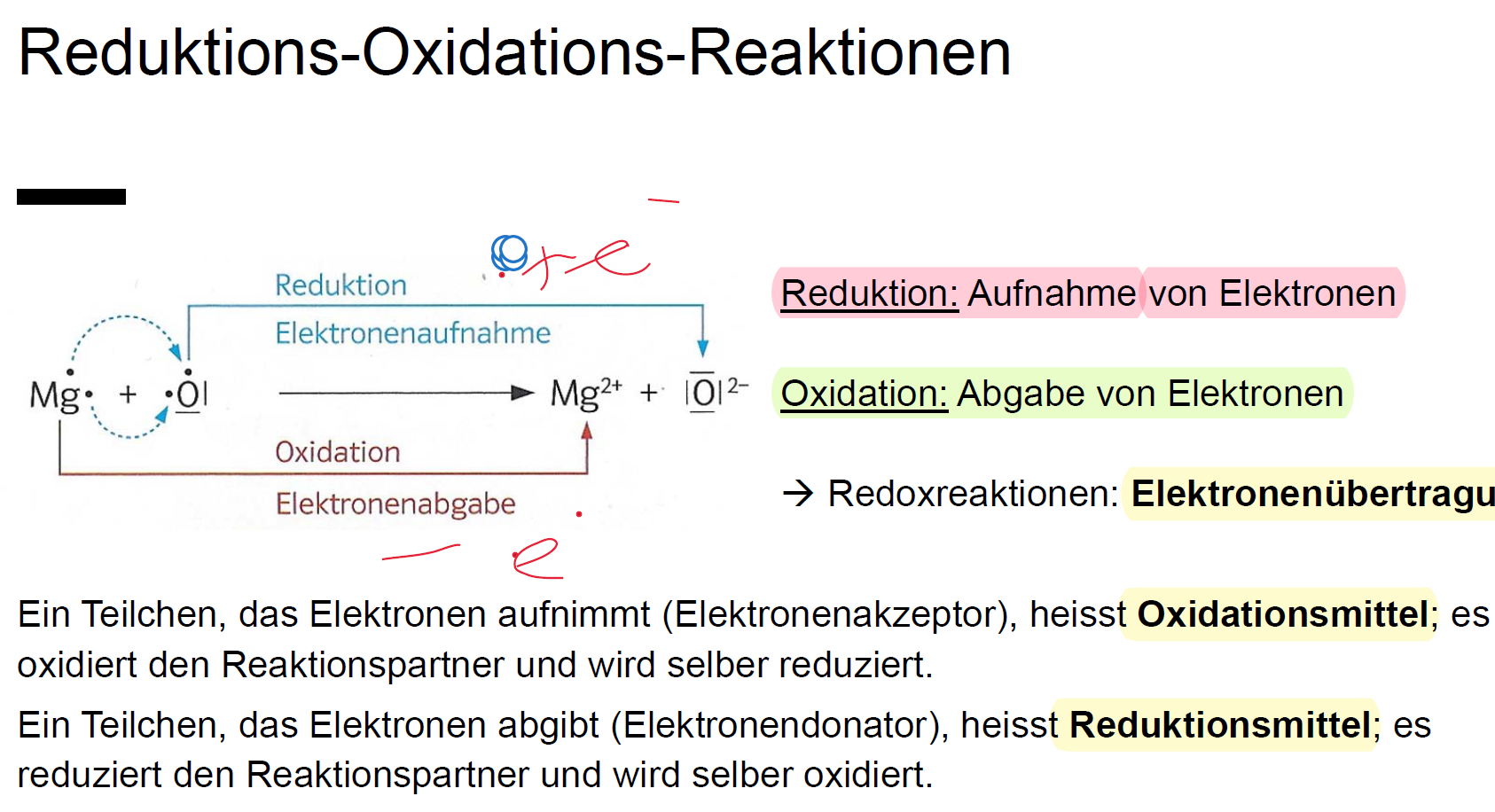
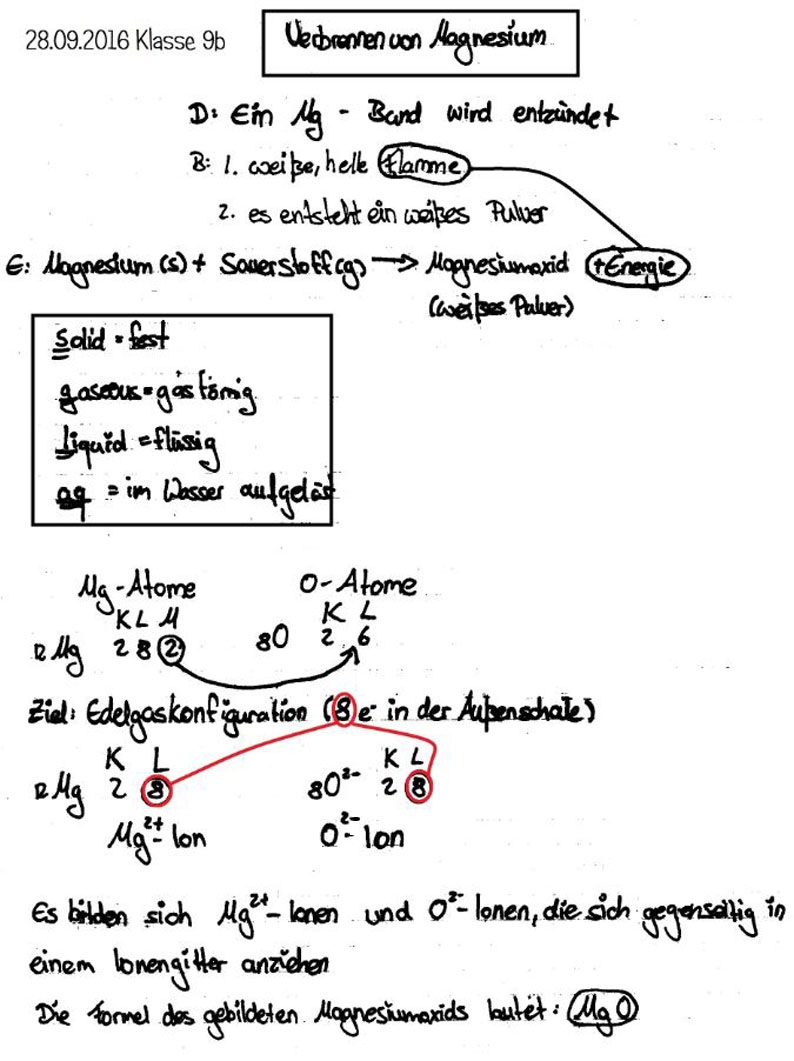
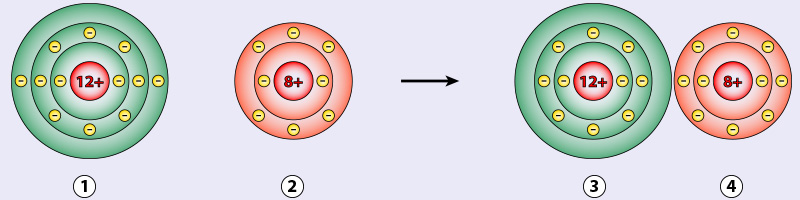
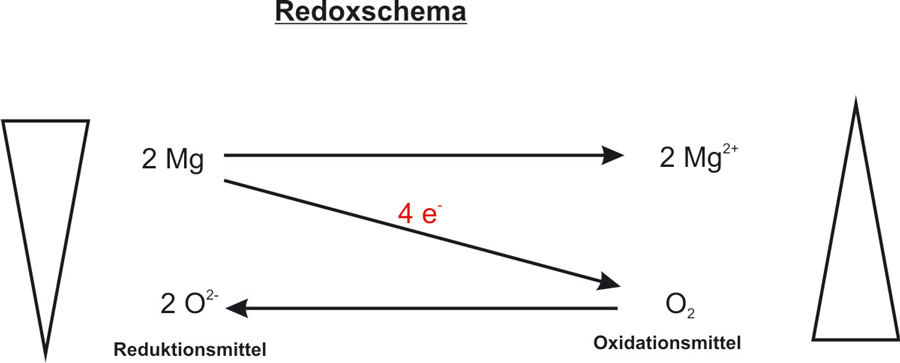
Wenn wir Magnesium (Mg) in die Nähe von Sauerstoff (O2) bringen und ihm einen kleinen Schubs geben – in Form von Hitze, also dem Anzünden – dann passiert’s: Magnesium gibt seine Elektronen an den Sauerstoff ab. Dieser Prozess ist wie eine super freundliche Geste, aber mit ein bisschen mehr Feuerwerk. Das Magnesium wird oxidiert, das heißt, es verliert Elektronen. Stell dir vor, es ist wie ein Gewichtheber, der die Hantel loslässt – erleichtert, aber vielleicht ein bisschen weniger beeindruckend.
Aber was passiert mit dem Sauerstoff? Nun, er nimmt die Elektronen dankend an. Das nennt man Reduktion. Er gewinnt Elektronen und wird dadurch ein bisschen "mächtiger". Denk an einen Schwamm, der Wasser aufsaugt. Er wird größer und schwerer, weil er etwas aufgenommen hat.
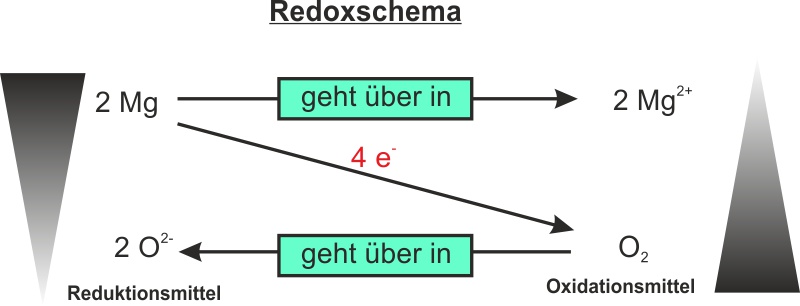
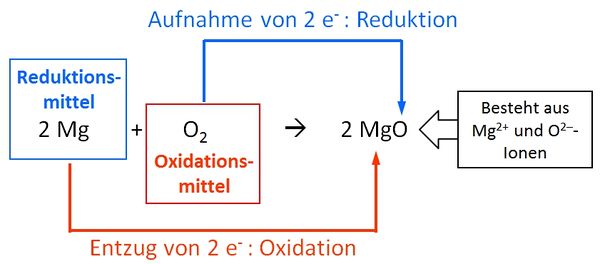
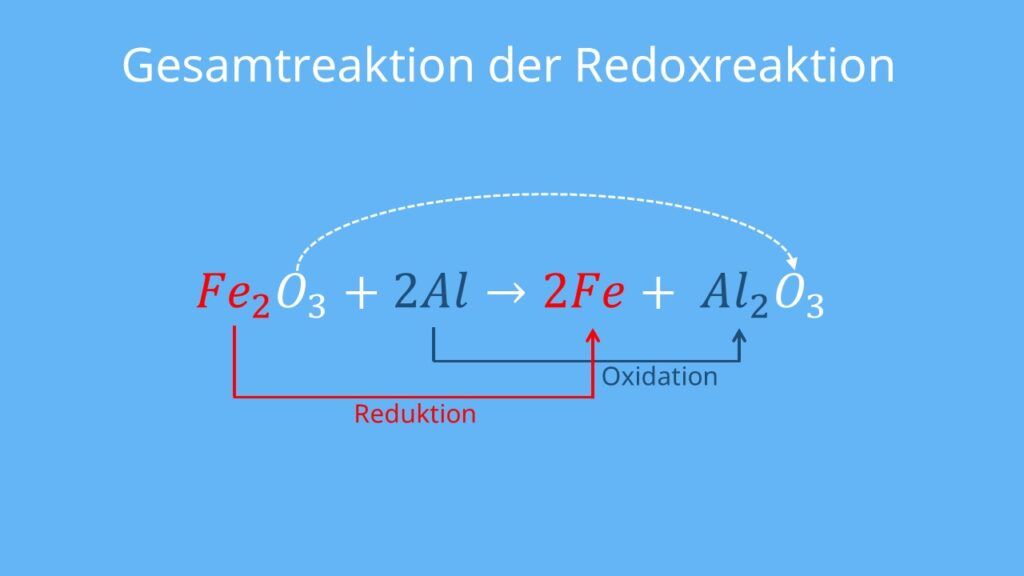
Zusammen bilden Oxidation und Reduktion die Redoxreaktion. Das ist wie ein Tanz, bei dem Magnesium den ersten Schritt macht (Elektronen abgeben) und Sauerstoff den zweiten (Elektronen annehmen). Und das Ergebnis? Magnesiumoxid (MgO), ein weißes Pulver. Simpel, oder?
Warum ist das so hell?
Das Leuchten, das wir sehen, ist die freigesetzte Energie. Die Elektronen, die von Magnesium zu Sauerstoff wandern, machen das nicht still und heimlich. Sie veranstalten eine richtige Party! Sie setzen Energie in Form von Licht und Wärme frei. Stell dir vor, du wirfst einen Stein in einen Teich. Es gibt einen lauten Platsch und Wellen entstehen. So ähnlich ist es auch mit den Elektronen – nur mit viel, viel mehr Licht!
Und dieses Licht ist wirklich hell. Sehr, sehr hell. So hell, dass man nicht direkt hineinschauen sollte! Es ist, als würde die Sonne in Miniaturform auf deinem Tisch tanzen (aber bitte ohne deinen Tisch abzufackeln!).
Redoxreaktionen überall!
Das Coole ist, dass diese Redoxreaktionen nicht nur im Labor passieren. Sie sind überall um uns herum! Das Rosten von Eisen ist eine Redoxreaktion (Eisen gibt Elektronen an Sauerstoff ab). Die Photosynthese in Pflanzen ist eine Redoxreaktion (Wasser gibt Elektronen ab, um Zucker zu bilden). Sogar das Atmen ist eine Redoxreaktion (wir nehmen Sauerstoff auf, der Elektronen von unserer Nahrung annimmt). Unglaublich, oder?
"Redoxreaktionen sind wie die heimlichen Architekten des Universums. Sie stecken hinter so vielen Prozessen, die unser Leben ermöglichen!"
Also, das nächste Mal, wenn ihr ein Feuerwerk seht (natürlich aus sicherer Entfernung!), denkt daran, dass da eine Redoxreaktion am Werk ist. Oder wenn ihr ein Stück Eisen seht, das rostet. Oder wenn ihr einfach nur atmet. Die unsichtbare Welt der Elektronen, die hin und her wandern, ist faszinierend!
Und wer weiß, vielleicht inspiriert euch die Magnesium-Sauerstoff-Redoxreaktion ja dazu, selbst zum "Elektronen-Spender" zu werden – im übertragenen Sinne natürlich. Seid großzügig mit eurem Wissen, eurer Freundlichkeit und eurer positiven Energie. Denn auch das ist eine Art von Chemie, die die Welt ein bisschen heller macht!
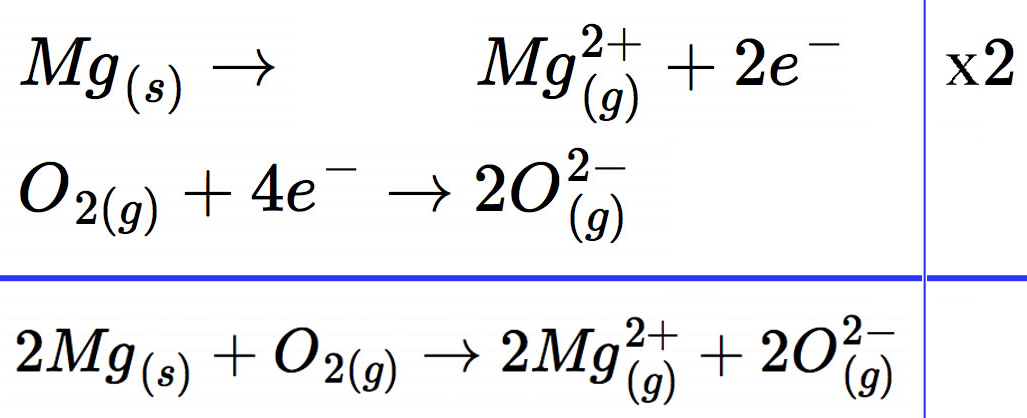
![Redoxreaktion Magnesium Und Sauerstoff Redoxreaktion einfach erklärt • Oxidation & Reduktion · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2021/12/03_Redoxreaktion-als-Elektronenübertragung-1-1024x576.jpg)

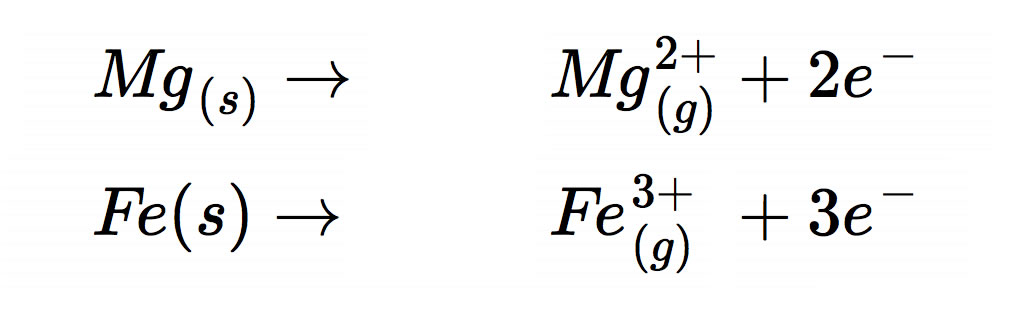
![Redoxreaktion Magnesium Und Sauerstoff Was sind Redoxreaktionen? [Erläuterung & Beispiele]](https://images.cdn.sofatutor.net/videos/pictures/27012/normal/27012_Thumbnail.jpg?1686650070)