Sn1 Und Sn2 Reaktionen
Stell dir vor, du bist auf einer Party. Es gibt da zwei verschiedene Arten, wie du dich von deinem alten Date (sagen wir, einem *Bromatom*) trennen und mit jemand Neuem (einem super coolen *Hydroxid-Ion*) anbandeln kannst. Diese beiden Arten sind wie die *Sn1* und *Sn2* Reaktionen in der Chemie – nur viel weniger peinlich, weil es hier keine gebrochenen Herzen gibt, sondern nur neue Bindungen!
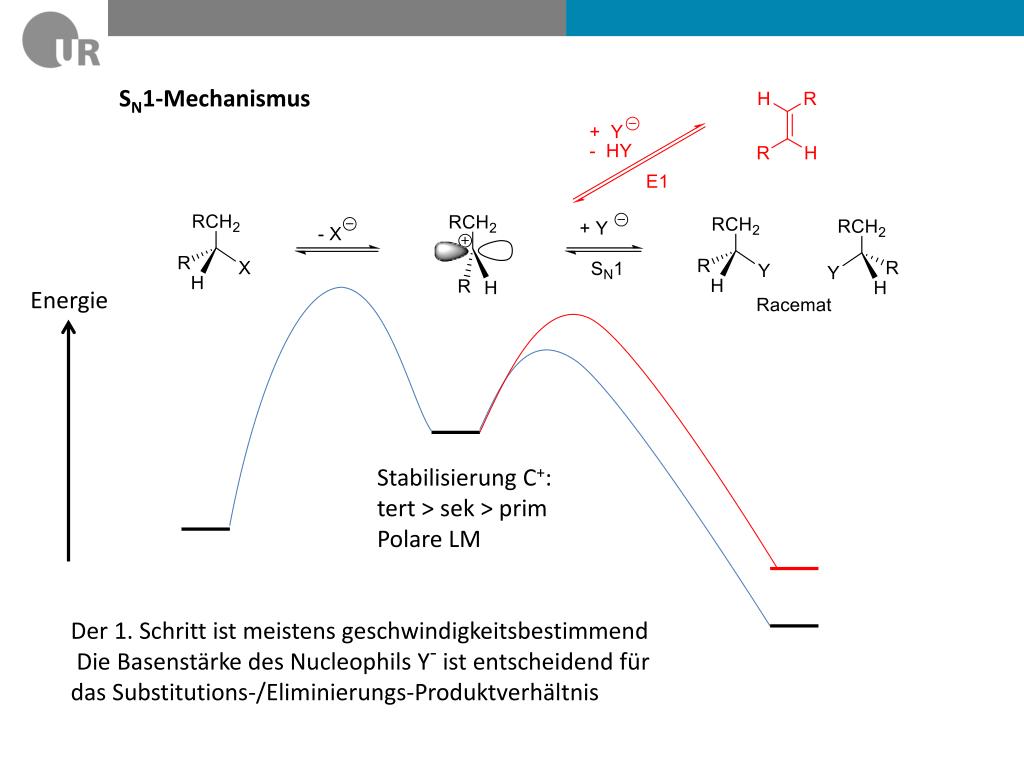
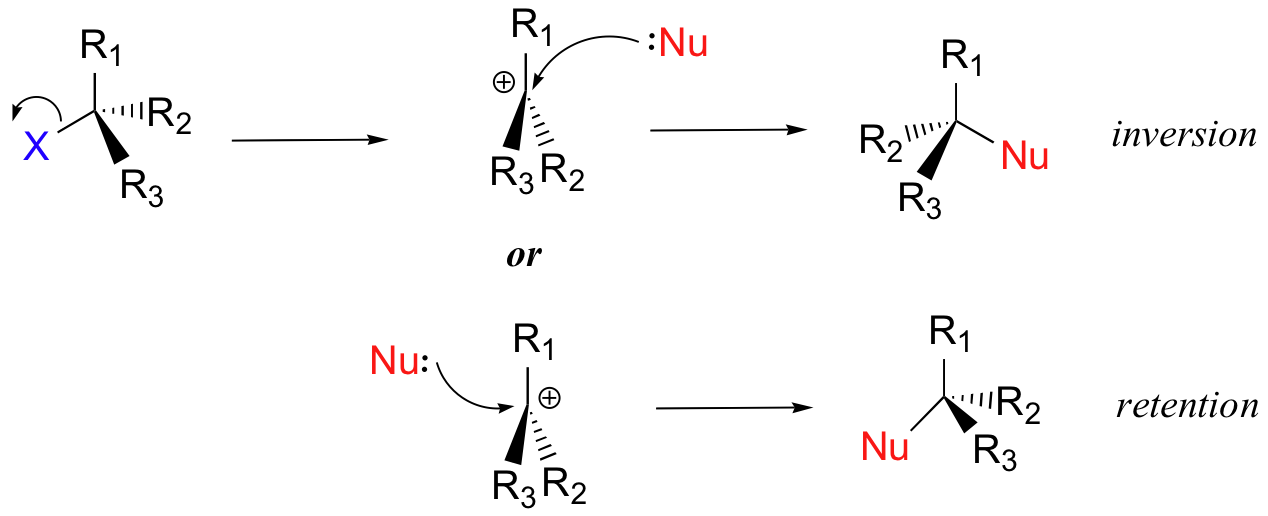
Sn1: Der einsame Wolf
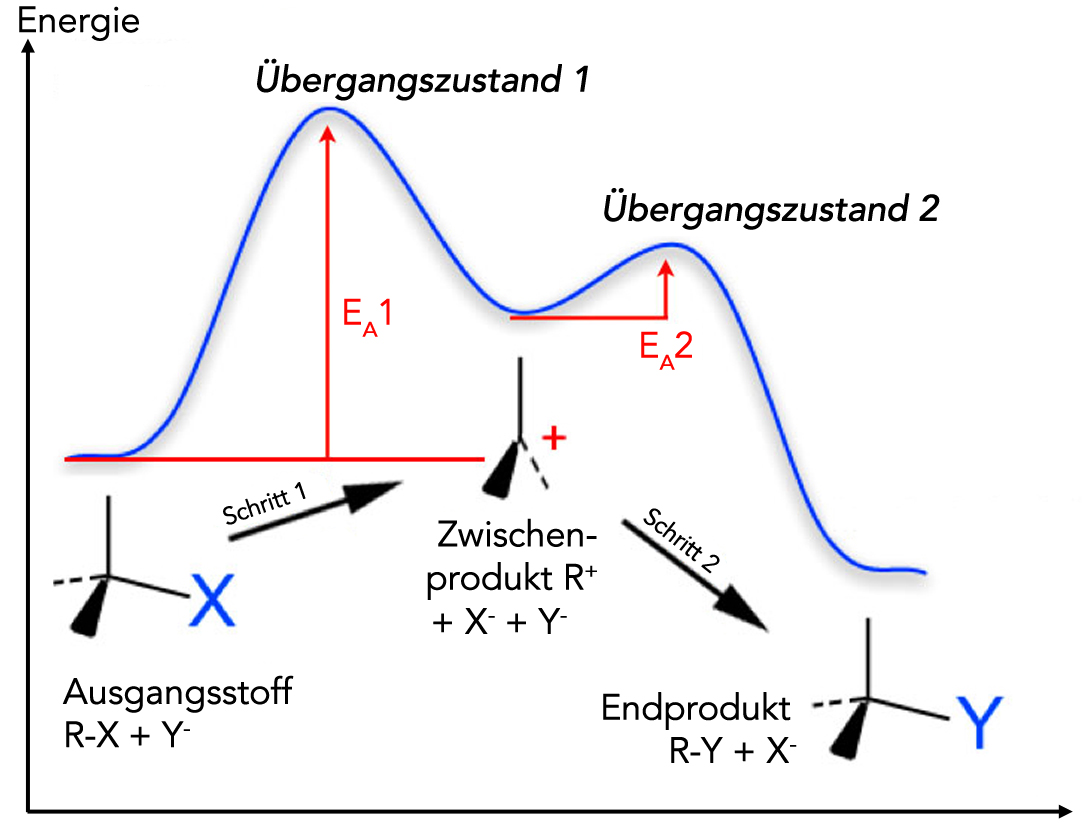
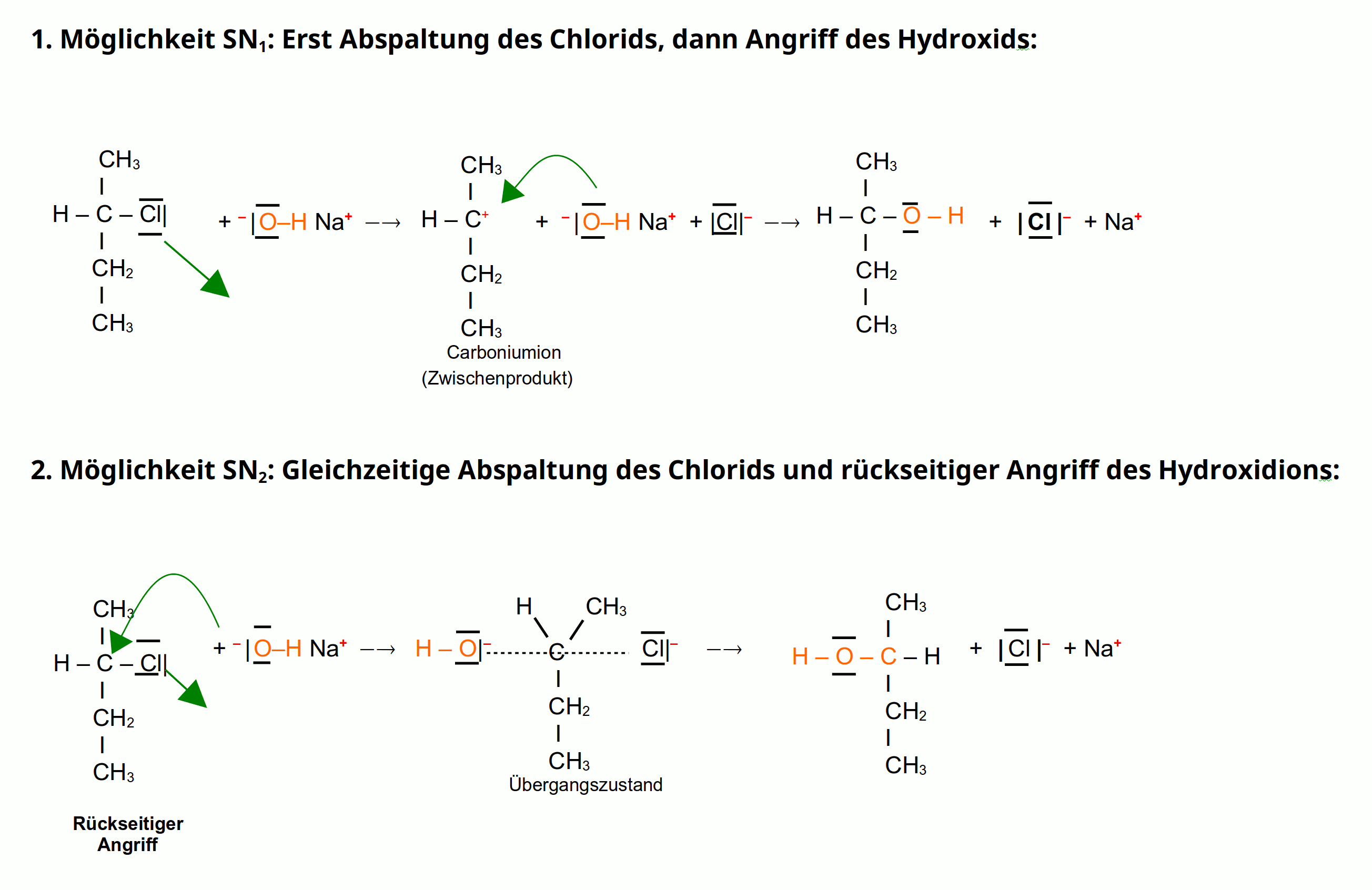
Die *Sn1* Reaktion, lass sie uns den einsamen Wolf unter den chemischen Reaktionen nennen, ist super entspannt. Stell dir vor, dein Bromatom ist so langweilig, dass es einfach *spontan* abhaut. Es sagt quasi: "Tschüss, ich geh mal eben!", ohne sich großartig darum zu kümmern, wer danach kommt. Das Ergebnis? Ein sogenanntes *Carbokation*. Stell dir das wie einen einsamen Partygast vor, der kurz davor ist, einen Anruf von Mama zu bekommen, weil er ganz alleine rumsteht. Dieses Carbokation ist super unglücklich und will SOFORT Gesellschaft.
Jetzt kommt unser cooles Hydroxid-Ion ins Spiel! Es sieht den einsamen Partygast und denkt: "Hey, der sieht ja ganz verlassen aus, da muss ich helfen!". Und *schwupps*, bindet es sich an das Carbokation. Fertig! Eine neue Beziehung, ganz ohne großes Tamtam. Das Tolle an der *Sn1* Reaktion ist, dass es ihr egal ist, von welcher Seite das Hydroxid-Ion kommt. Es ist wie bei einer offenen Tür – wer zuerst kommt, mahlt zuerst. Das führt oft zu einem Gemisch aus verschiedenen Produkten. Es ist ein bisschen chaotisch, aber hey, Hauptsache, es knistert wieder!
Die Sache mit der Stabilität
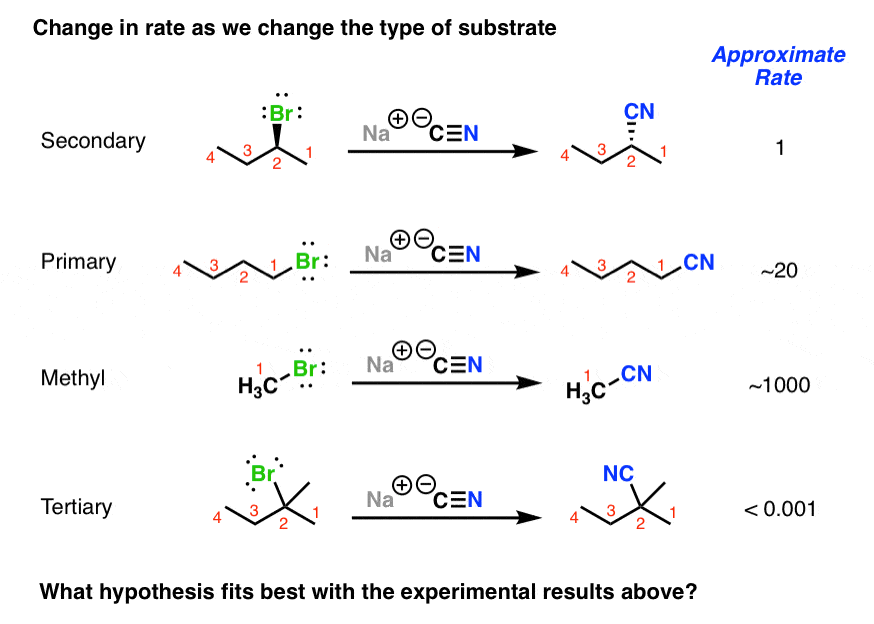
Je stabiler das Carbokation, desto leichter geht die *Sn1* Reaktion vonstatten. Denk an den einsamen Partygast – je cooler er ist, desto schneller findet er einen neuen Tanzpartner. *Tertiäre Carbokationen* (drei Freunde, die ihm Gesellschaft leisten – quasi drei Alkylgruppen) sind viel stabiler als *primäre* (nur ein Freund). Ein primäres Carbokation wäre wie ein kleines Kind, das seine Mama vermisst und gleich anfängt zu weinen. Das will keiner daten!
Sn2: Der Tanz auf der Rasierklinge
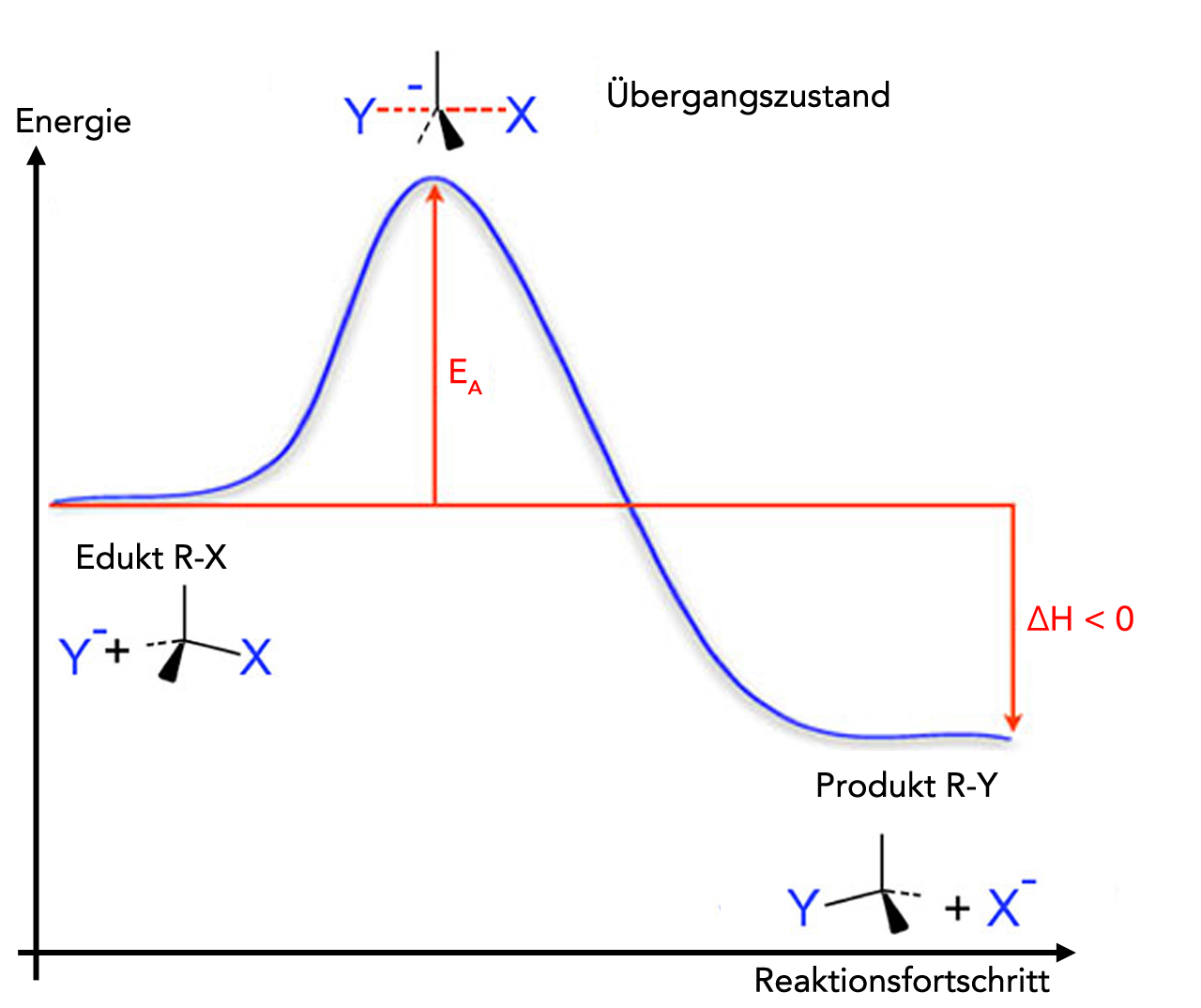
Die *Sn2* Reaktion ist ganz anders. Sie ist wie ein Tanz auf der Rasierklinge, super präzise und koordiniert. Hier gibt es kein einsames Carbokation, das jämmerlich herumsteht. Nein, hier passiert alles gleichzeitig! Unser Hydroxid-Ion ist ungeduldig und sagt: "Bromatom, du bist raus! Ich übernehme jetzt!". Es schleicht sich quasi von hinten an das Bromatom heran und drängt es gleichzeitig raus. Das ist wie bei einem Stau – einer drängelt, und der Vordermann muss Platz machen.
Das Ergebnis? Eine *Inversion der Konfiguration*! Stell dir vor, du drehst einen Regenschirm um. Das Hydroxid-Ion kommt von der entgegengesetzten Seite des Bromatoms. Die *Sn2* Reaktion ist super wählerisch. Sie braucht Platz! Wenn das Molekül zu voll ist (viele Alkylgruppen rund um das Kohlenstoffatom), dann kommt das Hydroxid-Ion nicht durch. Es ist wie versuchen, in einem überfüllten Bus einen Sitzplatz zu finden – unmöglich!
Sterische Hinderung – der Party-Crasher
*Sterische Hinderung* ist das Stichwort! Wenn viele große Gruppen rund um das Kohlenstoffatom sitzen, dann ist es für das Hydroxid-Ion unmöglich, anzugreifen. Es ist wie bei einer Tür, die von innen verbarrikadiert ist. Da kommt keiner rein! Deshalb funktionieren *Sn2* Reaktionen am besten mit *primären Alkylhalogeniden*, wo wenig Platzmangel herrscht.
Also, merk dir: *Sn1* ist der entspannte, zweistufige Prozess, der über ein Carbokation läuft und keine Angst vor Chaos hat. *Sn2* ist der präzise, einstufige Tanz, der Platz braucht und zur Inversion führt. Beide Reaktionen sind wie unterschiedliche Wege, zum gleichen Ziel zu gelangen: Ein neues Molekül und ein zufriedenstellendes chemisches Ergebnis. Und hey, wer weiß, vielleicht lernst du ja auf der nächsten Party, ob du eher ein *Sn1* oder ein *Sn2* Typ bist! Viel Spaß beim Reagieren!