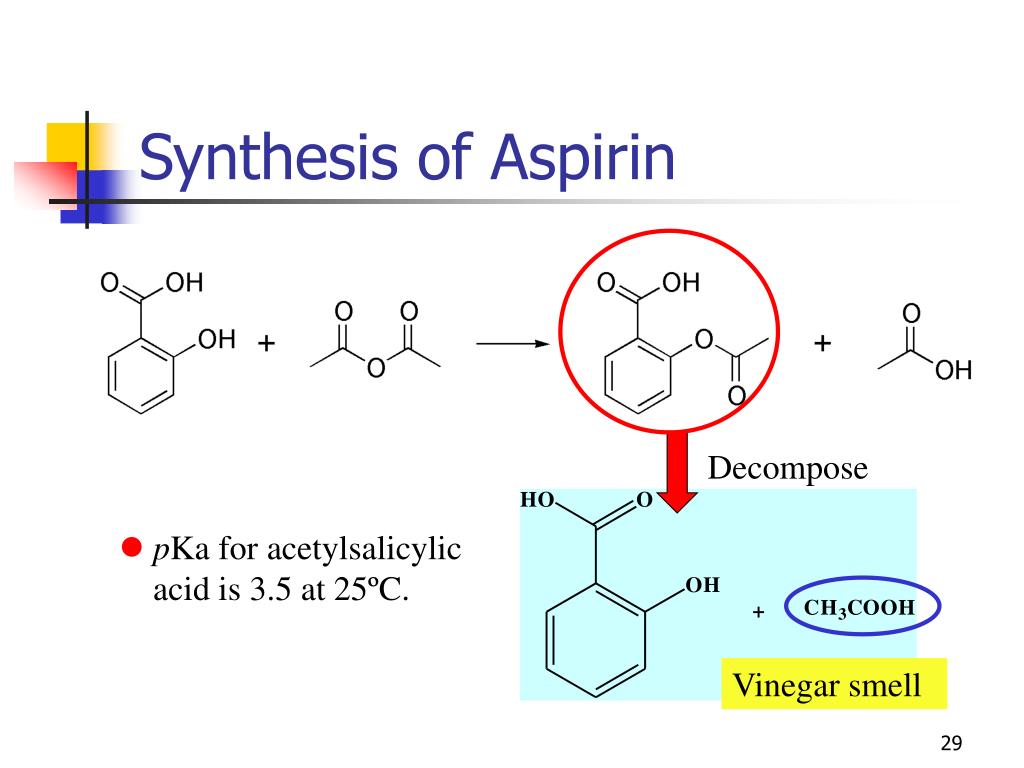
Synthesis Of Aspirin Procedure

Hast du dich jemals gefragt, wie man Aspirin herstellt? Es ist kein Hexenwerk, sondern faszinierende Chemie! Denk an einen kleinen Zaubertrank, den du in deinem eigenen (sicheren!) Labor zusammenbrauen könntest. Klingt cool, oder?
Was du brauchst: Die Zutaten für dein eigenes Schmerzmittel!
Zuerst brauchst du Salicylsäure. Stell dir vor, das ist die Hauptfigur in unserem chemischen Theaterstück. Dann kommt Essigsäureanhydrid ins Spiel – der mysteriöse Helfer, der die Verwandlung möglich macht. Ein paar Tropfen Schwefelsäure wirken als Katalysator, ein chemischer Speed-Booster, der alles beschleunigt. Und natürlich brauchst du Wasser, um die Reaktion zu stoppen und dein fertiges Produkt zu waschen.
Die Ausrüstung: Dein Mini-Labor
Okay, du brauchst keine High-Tech-Ausrüstung. Ein Becherglas, ein Erlenmeyerkolben (was für ein Wort!), ein Rührwerk (oder einfach ein Glasstab zum Umrühren), ein Heizbad (ein Wasserbad tut's auch) und Filterpapier sind deine wichtigsten Werkzeuge. Vergiss nicht: Sicherheit geht vor! Schutzbrille und Handschuhe sind Pflicht, denn wir wollen ja keinen Chemie-Unfall verursachen.
Die Magie beginnt: Schritt für Schritt zum Aspirin
Los geht's! Zuerst wiegst du die Salicylsäure ab. Genauigkeit ist wichtig, also sei pingelig. Dann gibst du sie in dein Becherglas oder deinen Erlenmeyerkolben. Jetzt kommt das Essigsäureanhydrid dazu. Vorsicht, das Zeug ist ätzend! Rühre alles gut um, sodass sich die Salicylsäure schön auflöst.
Der Katalysator: Der chemische Beschleuniger
Jetzt kommt der spannende Teil: Gib ein paar Tropfen Schwefelsäure hinzu. Beobachte, was passiert! Du wirst vielleicht sehen, wie die Mischung warm wird. Das ist ein Zeichen, dass die Reaktion in vollem Gange ist. Rühre weiter und sorge dafür, dass alles gut vermischt ist.
Das Heizbad: Wärme für die Verwandlung
Stell dein Gefäß in das Heizbad. Die Wärme hilft der Reaktion, schneller abzulaufen. Lass alles für etwa 15 Minuten im warmen Bad köcheln. Achte darauf, dass die Temperatur nicht zu hoch wird, sonst kann es zu unerwünschten Nebenreaktionen kommen. Geduld ist eine Tugend, besonders in der Chemie!
Abkühlen und Ausfällen: Das Aspirin kristallisiert
Nimm dein Gefäß aus dem Heizbad und lass es abkühlen. Jetzt kommt der Moment, auf den du gewartet hast: Gib vorsichtig kaltes Wasser hinzu. Du wirst sehen, wie sich kleine Kristalle bilden. Das ist dein rohes Aspirin! Ein bisschen wie Schnee in deinem Becherglas.
Filtern und Waschen: Das Rohprodukt wird rein
Jetzt musst du die Kristalle vom restlichen Wasser trennen. Das machst du mit dem Filterpapier. Gieß die Mischung durch den Filter und spüle die Kristalle mit kaltem Wasser nach. So entfernst du alle unerwünschten Rückstände.
Trocknen und Wiegen: Dein selbstgemachtes Aspirin
Lass die Kristalle gut trocknen. Am besten legst du sie auf ein sauberes Tuch oder Filterpapier und lässt sie an der Luft trocknen. Wenn sie trocken sind, kannst du sie wiegen. Jetzt weißt du, wie viel Aspirin du hergestellt hast!
Das Ergebnis: Ein Erfolgserlebnis mit Chemie
Denk dran: Dieses Experiment ist vor allem dazu da, um die Chemie zu verstehen. Bitte nimm dein selbstgemachtes Aspirin nicht ein! Es ist nicht rein genug und könnte schädliche Verunreinigungen enthalten. Aber hey, du hast gerade bewiesen, dass du ein echter Chemiker bist! Du hast Salicylsäure in Acetylsalicylsäure, also Aspirin, verwandelt. Wie cool ist das denn?
Das ist doch spannender als jeder Krimi, oder? Die Synthese von Aspirin ist ein faszinierendes Beispiel dafür, wie Chemie unser Leben beeinflusst. Es zeigt, dass die Welt der Moleküle und Reaktionen voller Überraschungen und Möglichkeiten steckt. Und wer weiß, vielleicht inspiriert dich das ja zu weiteren chemischen Abenteuern!
Also, worauf wartest du noch? Schnapp dir deine Schutzbrille, finde ein paar Chemikalien und tauche ein in die faszinierende Welt der organischen Chemie. Vielleicht entdeckst du ja dein eigenes Aspirin-Rezept – natürlich nur für wissenschaftliche Zwecke! 😉
Wichtig: Führe solche Experimente nur unter Aufsicht von erfahrenen Chemikern oder im Rahmen eines geeigneten Kurses durch. Sicherheit geht immer vor!
Die Synthese von Aspirin ist ein klassisches Beispiel für eine Veresterung, eine chemische Reaktion, bei der eine Säure und ein Alkohol zu einem Ester reagieren. In diesem Fall reagiert die Hydroxylgruppe (-OH) der Salicylsäure mit dem Essigsäureanhydrid, um die Acetylgruppe (-COCH3) anzufügen und Acetylsalicylsäure (Aspirin) zu bilden.



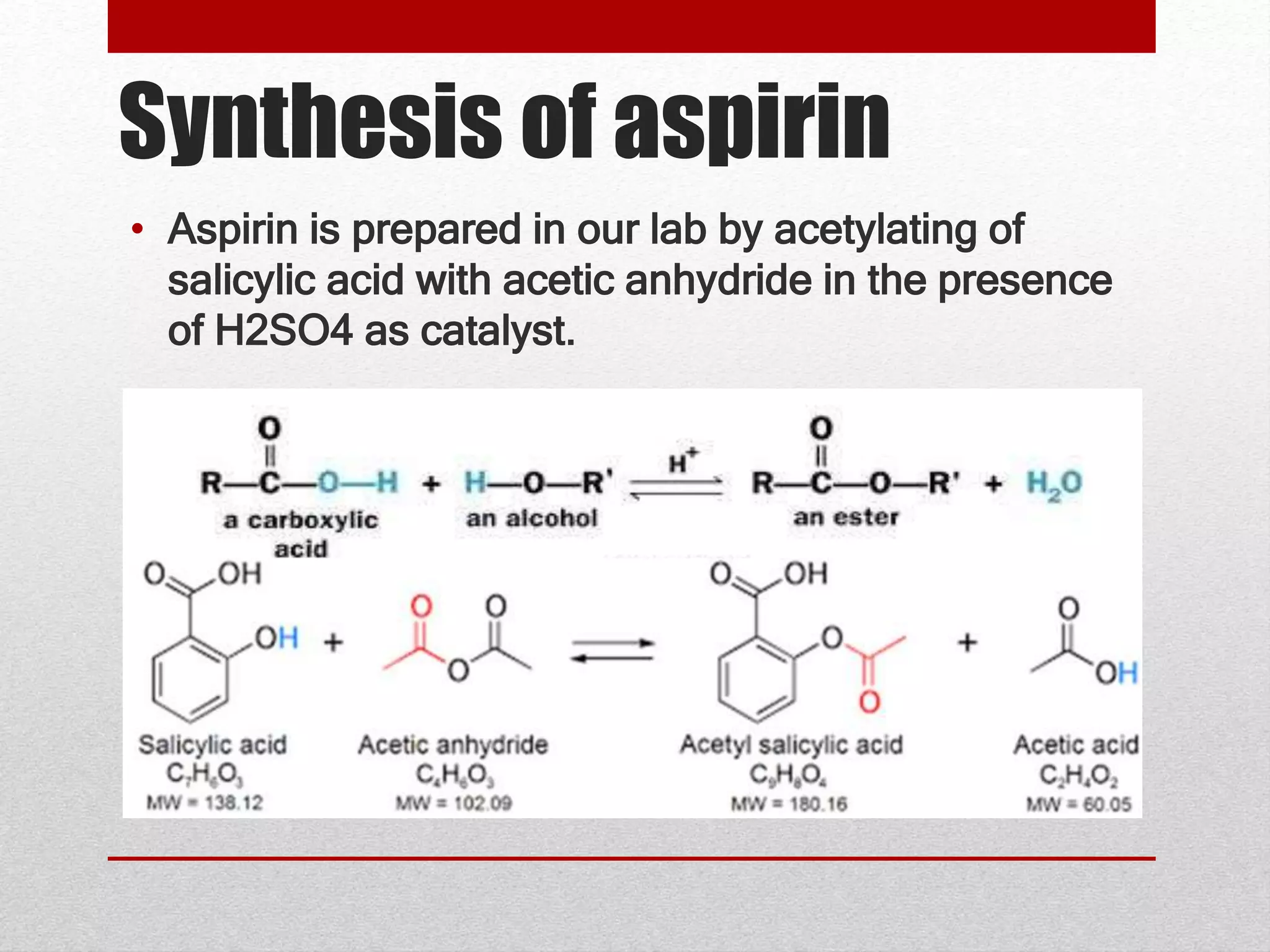





![Synthesis Of Aspirin Procedure Process Flow Diagram Of Aspirin [diagram] Process Flow Diagr](https://d2vlcm61l7u1fs.cloudfront.net/media/42d/42d4e503-fcaa-4db3-ae25-55c300b3a288/phpHfD8By.png)