Titration Schwache Säure Starke Base
Eine Titration einer schwachen Säure mit einer starken Base ist ein faszinierendes Experiment, das weit mehr als nur die Bestimmung der Konzentration einer Säure offenbart. Sie bietet eine tiefe Einsicht in chemische Gleichgewichte, die Pufferwirkung und die Bedeutung von Indikatoren. Betrachten wir dieses Experiment aus der Perspektive einer Ausstellung, in der Bildung, Erlebnis und die Vermittlung komplexer Zusammenhänge im Vordergrund stehen.
Die Ausstellung: Ein interaktiver Lernpfad
Stellen wir uns eine Ausstellung vor, die den Besucher durch die verschiedenen Aspekte der Titration einer schwachen Säure mit einer starken Base führt. Der Schwerpunkt liegt nicht nur auf der Durchführung des Experiments, sondern vielmehr auf dem Verständnis der zugrunde liegenden Prinzipien.
Station 1: Was ist eine schwache Säure?
Diese Station beginnt mit einer Einführung in den Unterschied zwischen starken und schwachen Säuren. Exponate könnten Modelle von Säuremolekülen zeigen, die in Wasser gelöst sind. Eine starke Säure dissoziiert vollständig in ihre Ionen, während eine schwache Säure nur teilweise dissoziiert. Dies wird durch Animationen visualisiert, die den Gleichgewichtszustand der Dissoziation einer schwachen Säure wie Essigsäure (CH3COOH) zeigen. Besucher können interaktiv die Konzentration der Säure verändern und beobachten, wie sich das Gleichgewicht verschiebt. Eine interaktive Simulation ermöglicht es, die Dissoziationskonstante (Ka) zu verändern und deren Einfluss auf den pH-Wert zu beobachten. Die Botschaft ist klar: Schwache Säuren sind nicht einfach "weniger stark", sondern unterliegen einem komplexen Gleichgewicht.
Station 2: Die starke Base – Ein kraftvoller Gegenspieler
Hier wird die starke Base, typischerweise Natriumhydroxid (NaOH), vorgestellt. Ihre vollständige Dissoziation in Natriumionen (Na+) und Hydroxidionen (OH-) wird demonstriert. Der kontrastierende Charakter zur schwachen Säure wird durch farbliche Gestaltung hervorgehoben. Ein interaktives Element könnte das Mischen von NaOH mit verschiedenen Stoffen simulieren, um die stark basische Natur und ihre potenziellen Gefahren zu verdeutlichen. Sicherheitsaspekte, wie das Tragen von Schutzbrillen und Handschuhen im Labor, werden betont.
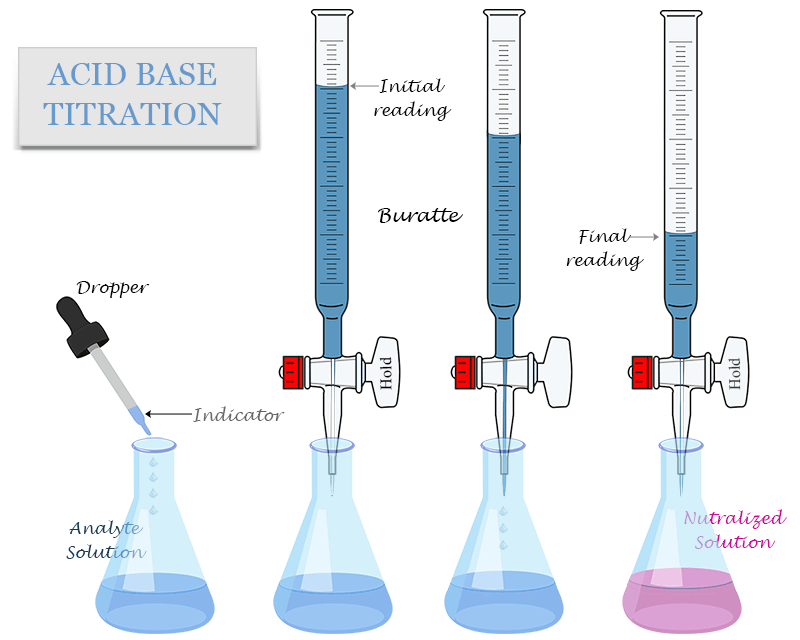
Station 3: Der Titrationsaufbau – Präzision und Kontrolle
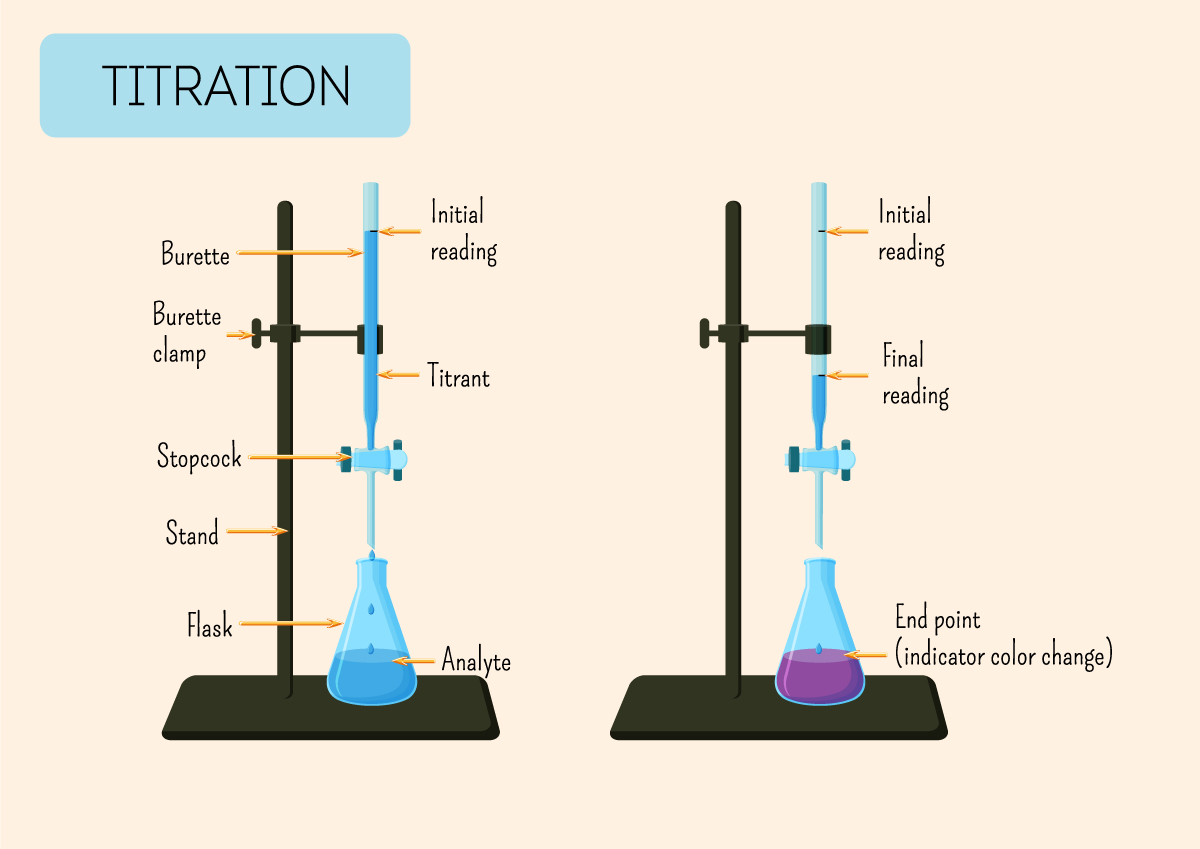
An dieser Station wird der Titrationsaufbau detailliert erklärt. Eine Bürette, ein Erlenmeyerkolben, ein Magnetrührer – jedes Element wird in seiner Funktion erläutert. Ein dreidimensionales Modell des Aufbaus ermöglicht es den Besuchern, die einzelnen Teile virtuell zu demontieren und wieder zusammenzusetzen. Ein kurzer Film zeigt, wie man eine Titration korrekt durchführt, wobei auf die Bedeutung des langsamen Zutropfens der Base und des kontinuierlichen Rührens hingewiesen wird. Hier wird auch der Begriff der "Äquivalenzpunkt" eingeführt, der Punkt, an dem die Säure vollständig neutralisiert ist.
Station 4: Der Indikator – Ein Farbwechsel mit Bedeutung
Die Rolle des Indikators ist zentral für die Titration. Verschiedene Indikatoren, wie Phenolphthalein oder Methylrot, werden vorgestellt. Ihre unterschiedlichen Farbumschläge in Abhängigkeit vom pH-Wert werden demonstriert. Ein interaktives Exponat zeigt, wie sich die Farbe des Indikators ändert, wenn man virtuell Säure oder Base hinzufügt. Der Begriff des "Endpunkts" wird erklärt, der nicht exakt mit dem Äquivalenzpunkt übereinstimmt, aber in der Praxis als Näherung dient. Die Auswahl des richtigen Indikators, dessen Umschlagsbereich möglichst nah am Äquivalenzpunkt liegt, wird thematisiert.
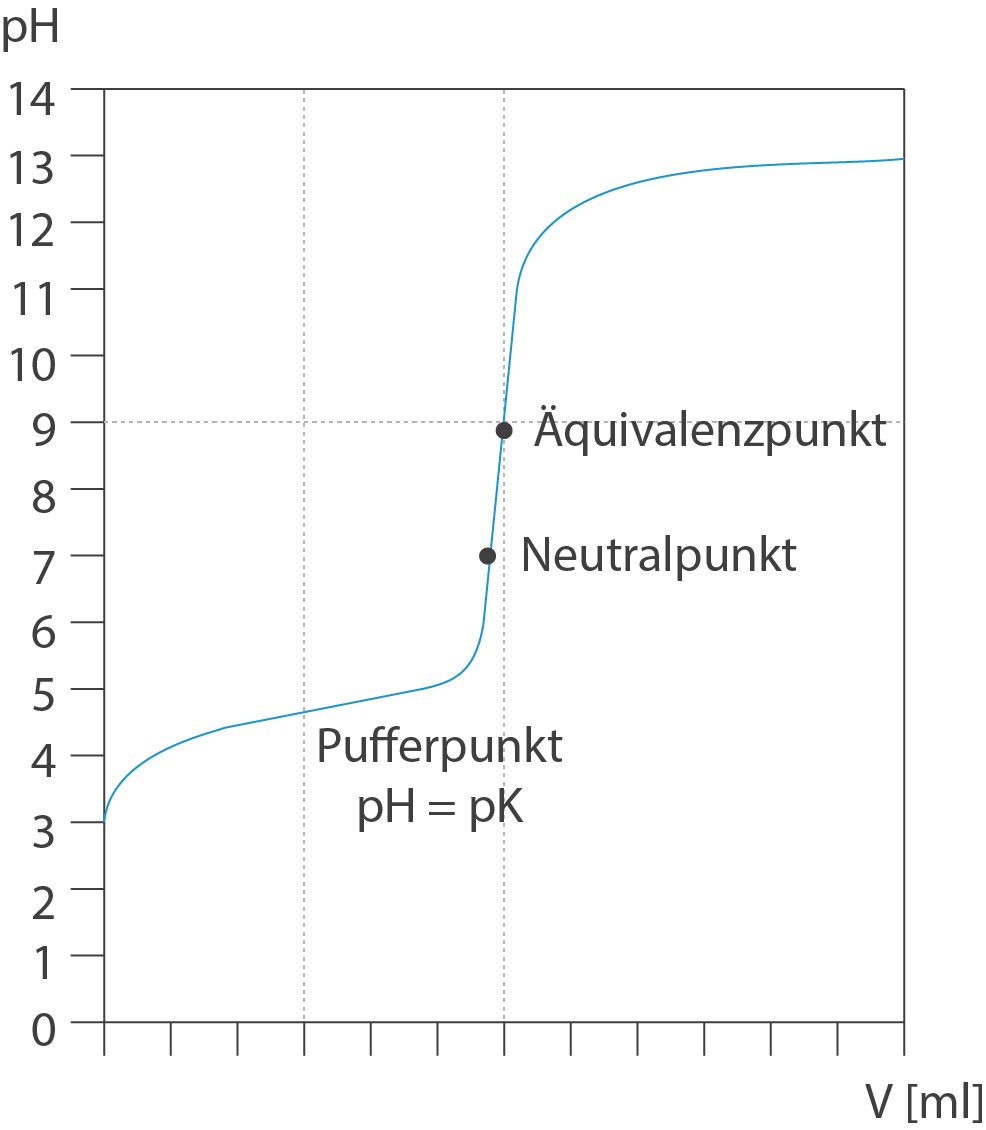
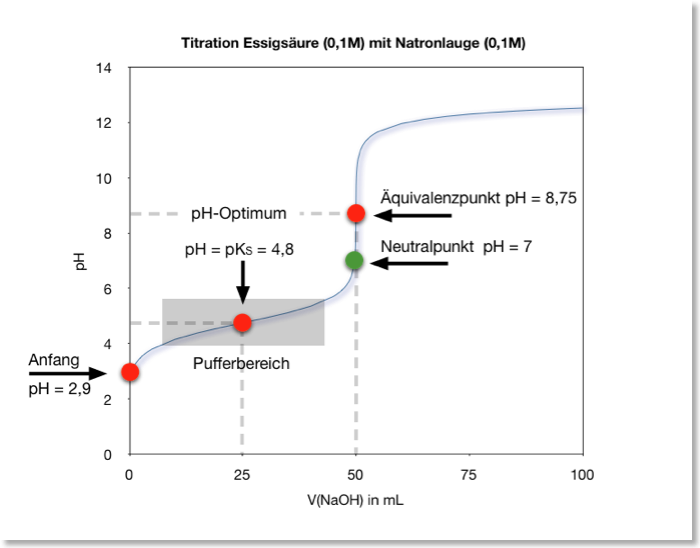
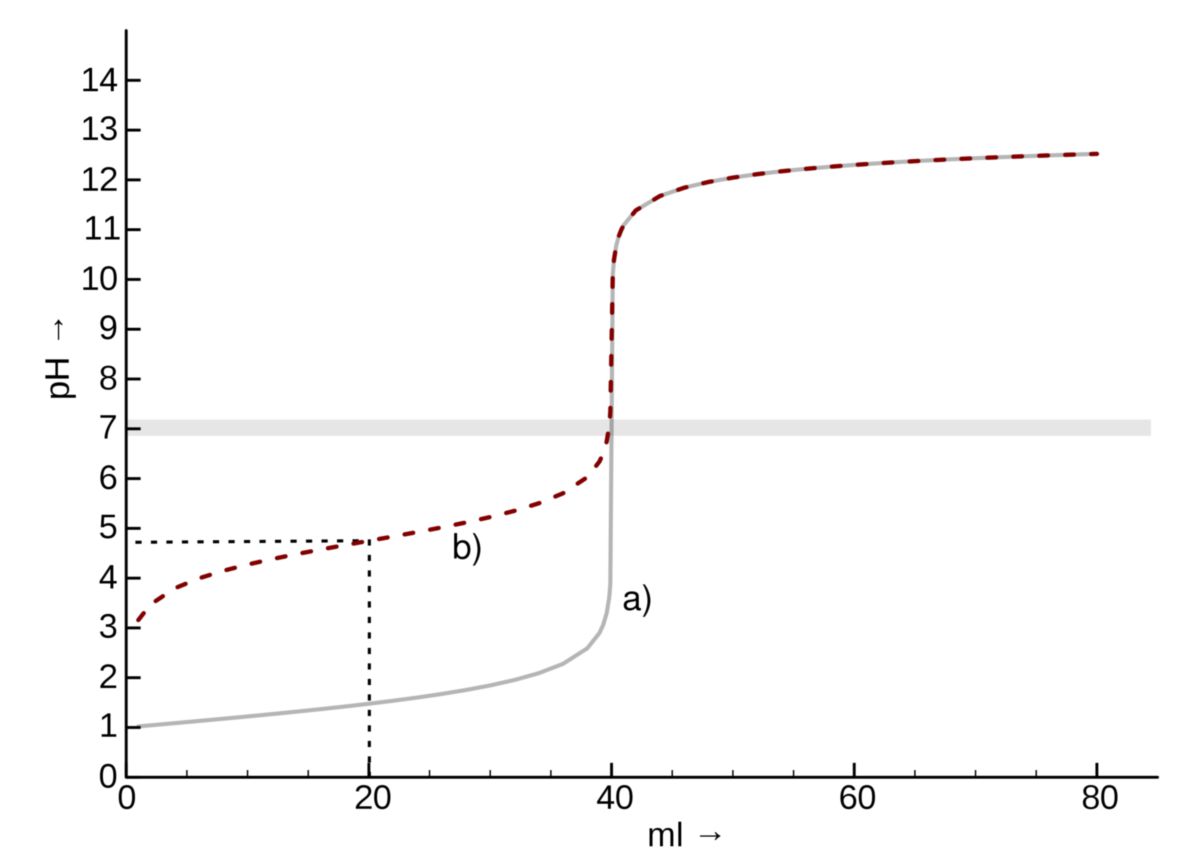
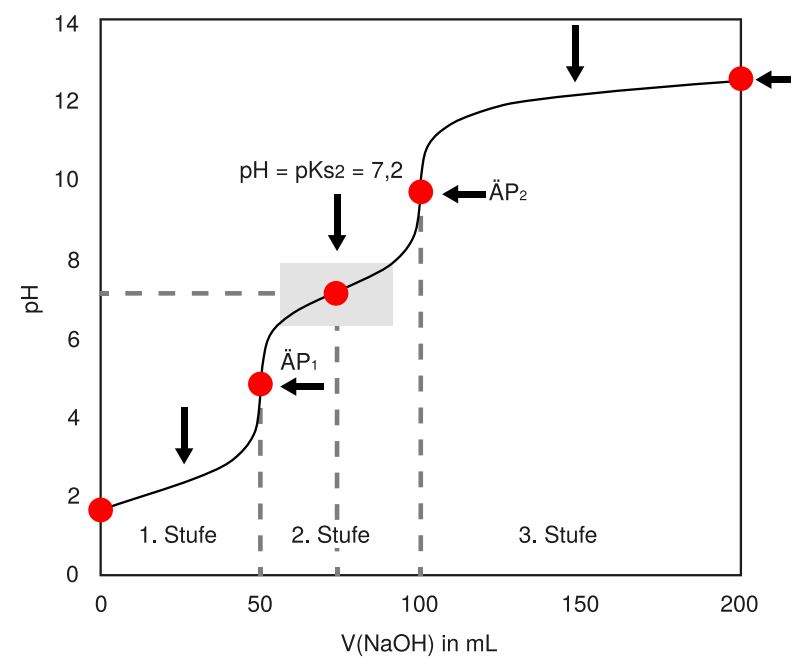
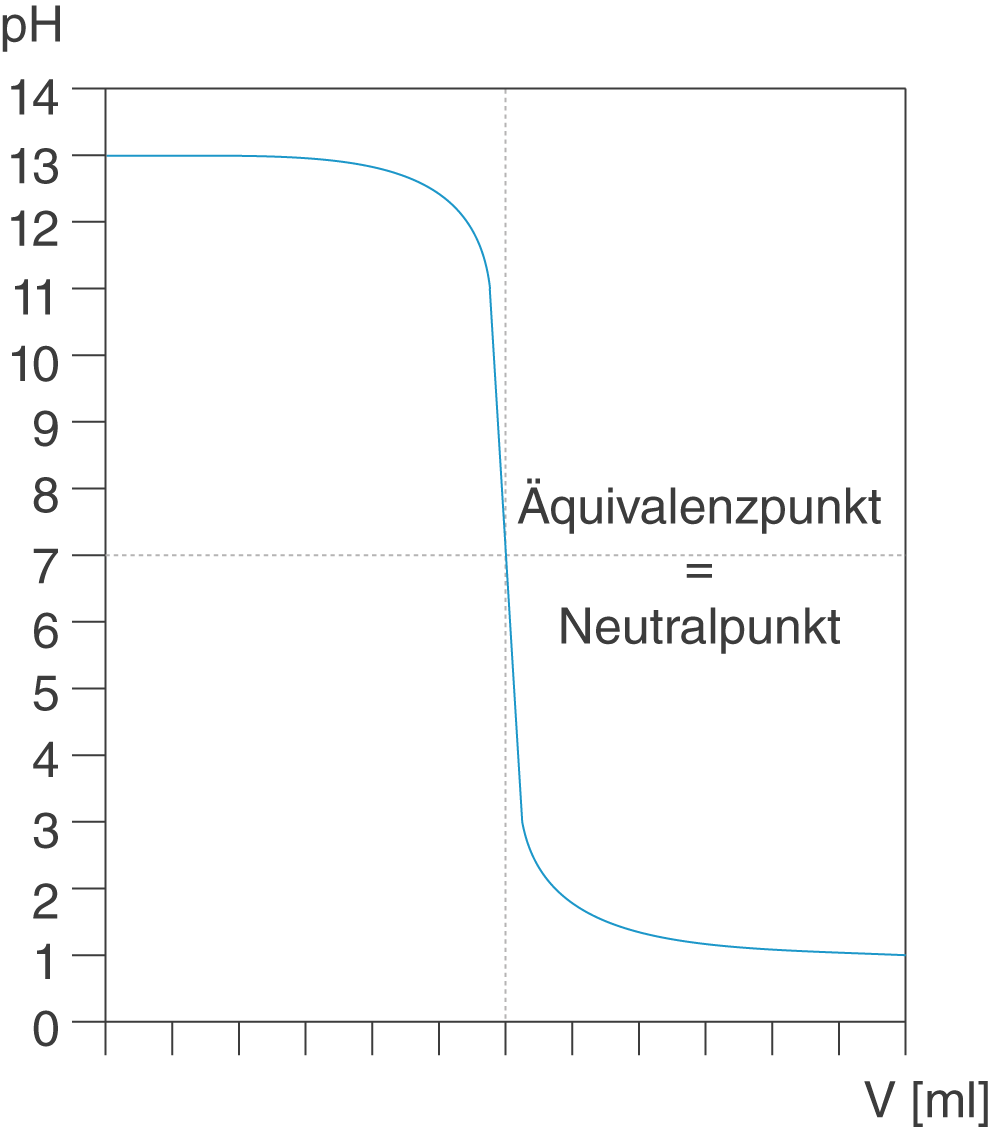
Station 5: Die Titrationskurve – Eine grafische Darstellung der Neutralisation
Diese Station ist das Herzstück der Ausstellung. Hier wird die Titrationskurve, eine grafische Darstellung des pH-Wertes in Abhängigkeit von der zugegebenen Menge an Base, detailliert analysiert. Der charakteristische Verlauf der Kurve, mit dem anfänglich langsamen Anstieg des pH-Wertes, dem steilen Anstieg in der Nähe des Äquivalenzpunktes und dem anschließenden langsamen Anstieg, wird erläutert. Die Bedeutung des Halbäquivalenzpunktes, an dem der pH-Wert gleich dem pKa-Wert der schwachen Säure ist, wird hervorgehoben. Eine interaktive Simulation ermöglicht es den Besuchern, die Konzentration der Säure und der Base zu verändern und zu beobachten, wie sich die Titrationskurve verändert. Dies vermittelt ein intuitives Verständnis für die Pufferwirkung.
Station 6: Die Pufferwirkung – Stabilität in einem sich ändernden Umfeld
Die Pufferwirkung ist eine der wichtigsten Anwendungen von schwachen Säuren und ihren konjugierten Basen. Diese Station erklärt, wie ein Puffersystem, bestehend aus einer schwachen Säure und ihrem Salz, den pH-Wert stabilisiert, wenn Säure oder Base hinzugefügt wird. Alltagsbeispiele für Puffer, wie das Blut, das den pH-Wert in einem engen Bereich hält, werden angeführt. Ein interaktives Exponat simuliert die Zugabe von Säure oder Base zu einem Puffersystem und zeigt, wie der pH-Wert relativ konstant bleibt. Die Henderson-Hasselbalch-Gleichung, die den Zusammenhang zwischen pH-Wert, pKa-Wert und den Konzentrationen von Säure und Base beschreibt, wird vorgestellt. Die Bedeutung der Pufferwirkung für biologische Systeme und chemische Prozesse wird betont.
Station 7: Anwendungen – Titration im Alltag
Die letzte Station zeigt die vielfältigen Anwendungen der Titration im Alltag. Beispiele sind die Bestimmung des Säuregehalts von Lebensmitteln, die Überwachung der Wasserqualität und die Analyse von Medikamenten. Ein kurzes Video zeigt, wie Titration in verschiedenen industriellen Prozessen eingesetzt wird. Die Besucher werden ermutigt, über die Bedeutung der chemischen Analyse und die Rolle der Titration für die Qualitätssicherung nachzudenken.
Die Besucherperspektive: Ein Aha-Erlebnis nach dem anderen
Das Ziel der Ausstellung ist es, den Besuchern ein tiefes Verständnis für die Titration einer schwachen Säure mit einer starken Base zu vermitteln. Dies wird durch eine Kombination aus interaktiven Exponaten, visuellen Darstellungen und praktischen Demonstrationen erreicht. Die Ausstellung ist so konzipiert, dass sie für Besucher unterschiedlicher Altersgruppen und Wissensstände zugänglich ist. Wichtig ist, dass die Besucher nicht nur Fakten lernen, sondern auch die wissenschaftliche Denkweise entwickeln. Sie sollen in der Lage sein, Fragen zu stellen, Hypothesen aufzustellen und Schlussfolgerungen zu ziehen.
Die Ausstellung soll kein trockener Frontalunterricht sein, sondern ein erlebnisorientiertes Lernen ermöglichen. Durch das interaktive Experimentieren können die Besucher die chemischen Prinzipien selbst entdecken und verinnerlichen. Die Ausstellung soll neugierig machen und die Besucher dazu anregen, sich weiter mit dem Thema Chemie auseinanderzusetzen. Eine begleitende Broschüre mit weiterführenden Informationen und Experimentieranleitungen für zu Hause rundet das Angebot ab.
Mehr als nur ein Experiment: Ein Fenster zur Chemie
Die Titration einer schwachen Säure mit einer starken Base ist mehr als nur ein Laborexperiment. Sie ist ein Fenster zur Welt der Chemie, das uns Einblicke in die grundlegenden Prinzipien von Säuren, Basen, Gleichgewichten und Puffern gewährt. Eine Ausstellung zu diesem Thema kann dazu beitragen, das Interesse an der Chemie zu wecken und das Verständnis für die Bedeutung der Chemie in unserem Alltag zu fördern. Durch die Kombination von Bildung und Erlebnis kann die Ausstellung zu einem unvergesslichen Lernerlebnis werden, das die Besucher nachhaltig beeindruckt und inspiriert.
Indem die Ausstellung die komplexen chemischen Prozesse vereinfacht, visualisiert und interaktiv erlebbar macht, wird das Thema zugänglich und verständlich. Die Besucher verlassen die Ausstellung nicht nur mit neuem Wissen, sondern auch mit einer neuen Perspektive auf die Welt um sie herum.





![Titration Schwache Säure Starke Base Säure Base Titration • Aufbau, Titrationskurven, Berechnung · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2022/04/03_Titrationskurve-schwache-Säure-mit-starker-Base-1-1024x576.jpg)


![Titration Schwache Säure Starke Base Säure Base Titration • Aufbau, Titrationskurven, Berechnung · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2022/04/04_Titrationskurve-mehrprotoniger-Säuren-1-1024x576.jpg)

