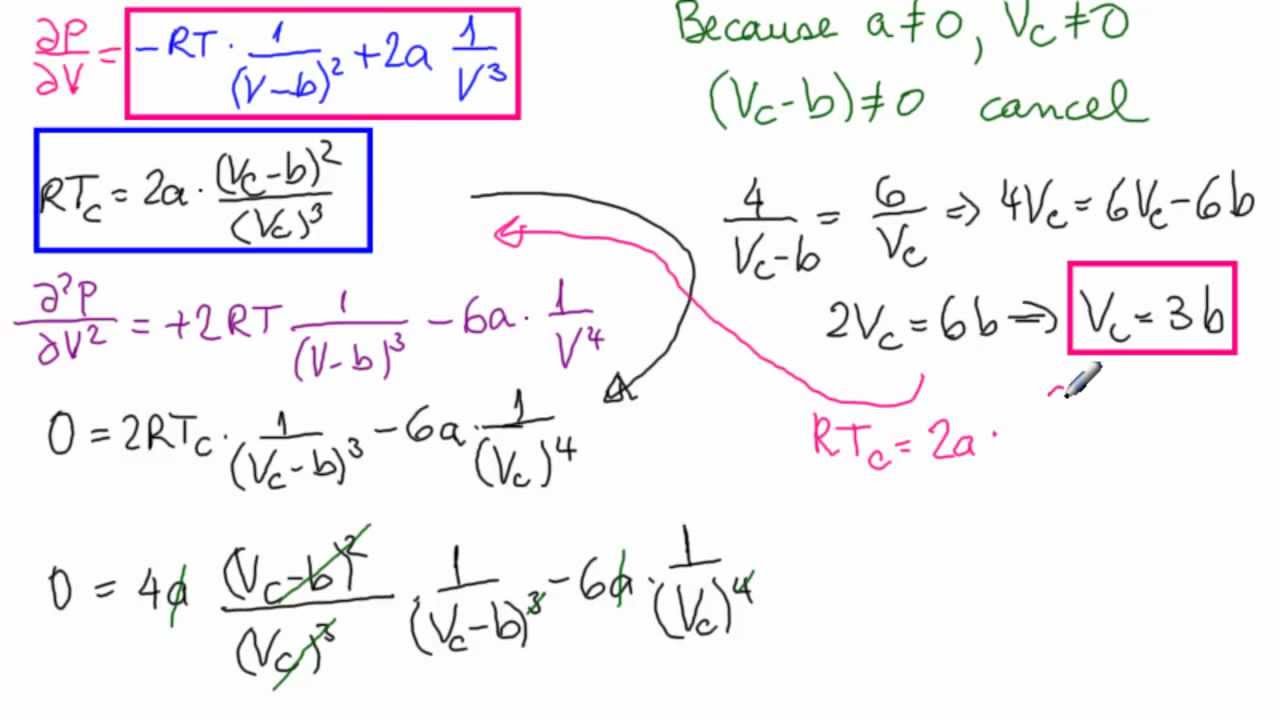
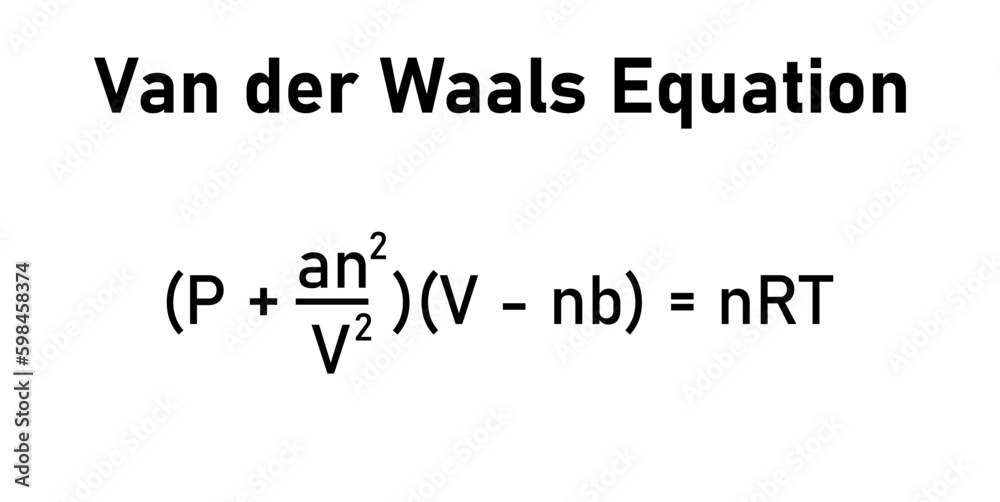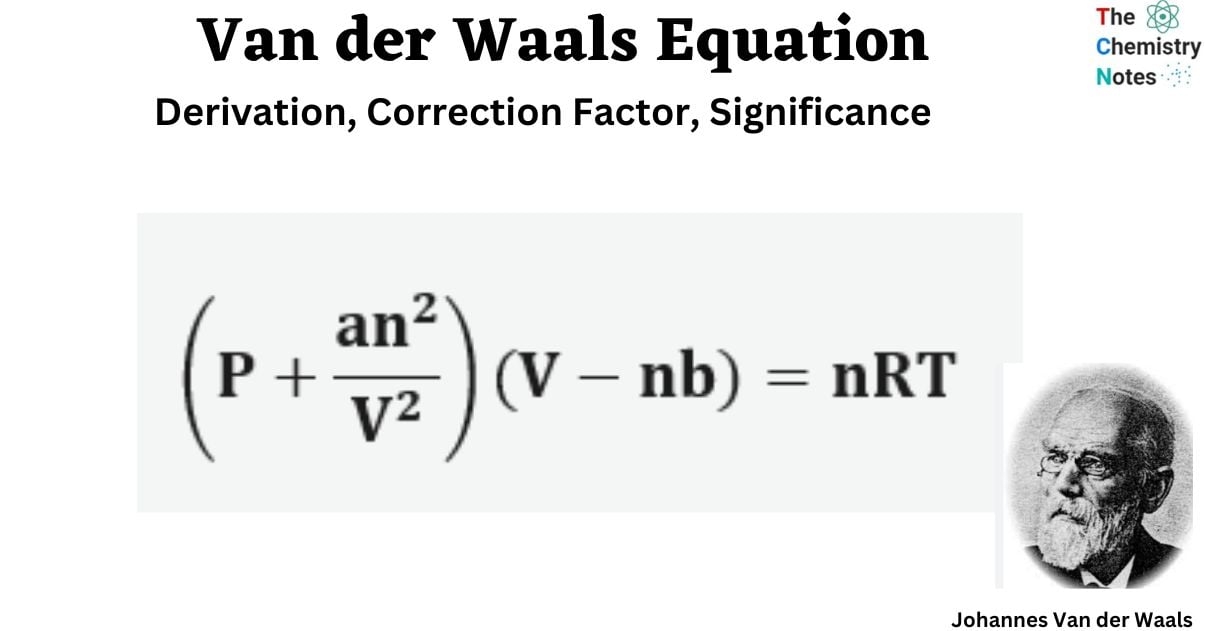Van Der Waals Gleichung
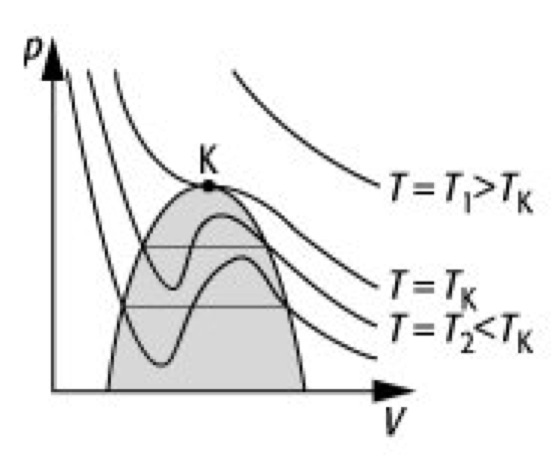
Stell dir vor, du bist auf einer Party. Ein Haufen Leute in einem kleinen Raum. Anfangs ist alles fröhlich, ausgelassen. Jeder tanzt und lacht. Aber je mehr Leute dazukommen, desto enger wird es. Man rempelt sich an, es wird stickig und man merkt: „Ideale Partybedingungen? Fehlanzeige!“
Genauso verhält es sich mit Gasen. Zumindest, wenn wir realistisch sein wollen. In der Schule lernen wir oft vom sogenannten "idealen Gas". Das ist ein theoretisches Konstrukt, bei dem die Gasmoleküle winzig kleine Billardkugeln sind, die sich wild durcheinander bewegen und überhaupt nicht miteinander interagieren. Klingt ja ganz nett, aber die Realität ist...nun ja, etwas chaotischer, wie eine überfüllte Party eben.
Die Sache mit den idealen Gasen: Ein bisschen zu idealistisch
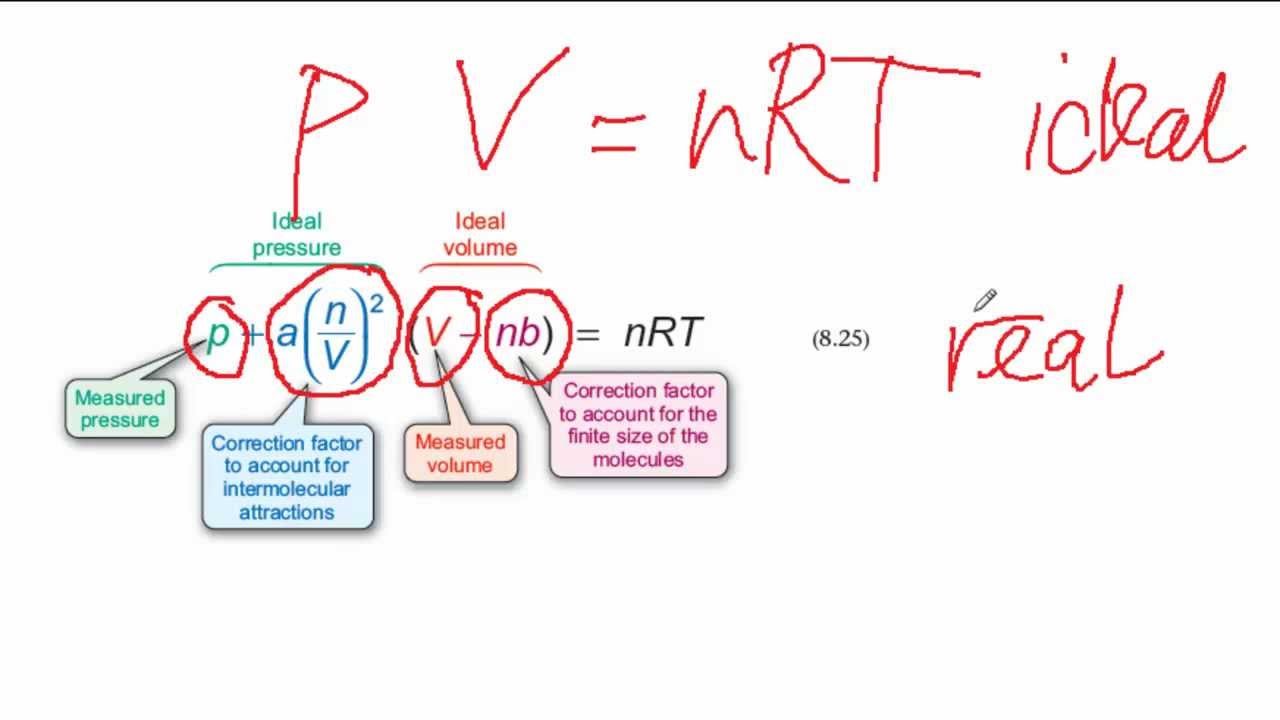
Die Formel, die das Verhalten von idealen Gasen beschreibt (PV = nRT – Druck mal Volumen ist gleich Stoffmenge mal Gaskonstante mal Temperatur), ist zwar super einfach und nützlich, aber sie ignoriert zwei wesentliche Dinge:
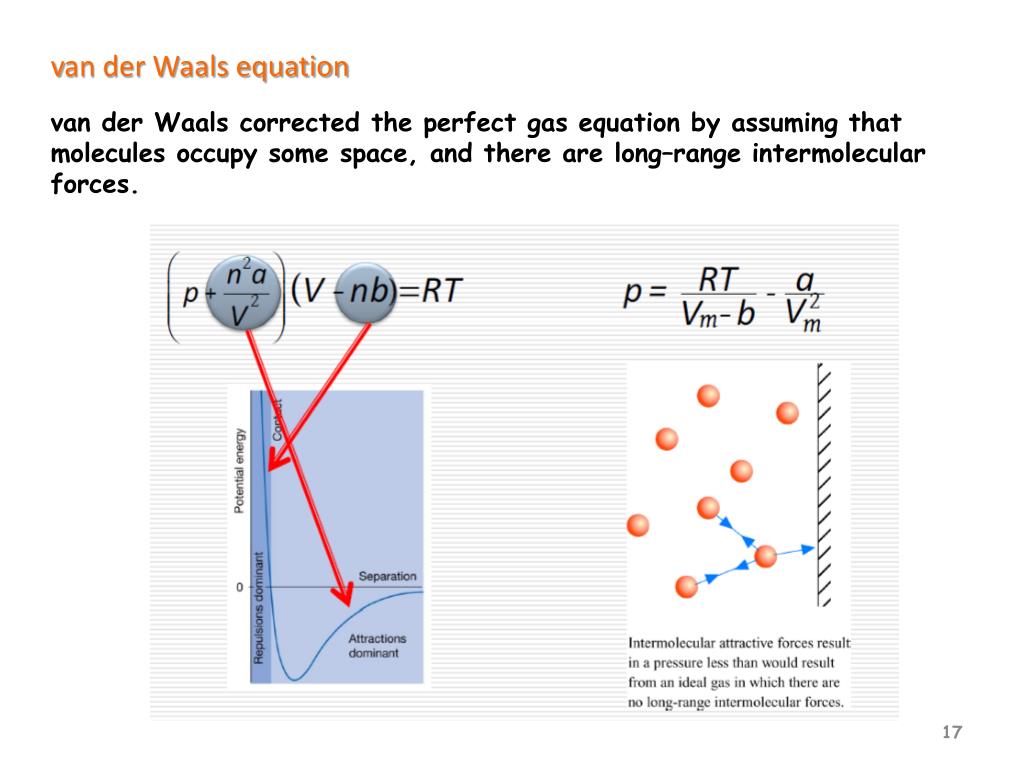
- Volumen der Moleküle: Die Moleküle sind nicht punktförmig! Sie nehmen Platz ein. Je mehr Moleküle, desto weniger Platz zum Herumsausen.
- Anziehungskräfte zwischen den Molekülen: Auch wenn es winzig ist, ziehen sich die Moleküle gegenseitig an. Stell dir vor, die Partygäste würden nicht nur tanzen, sondern sich auch noch leicht an den Händen halten. Das würde die Bewegung auch einschränken.
Und genau hier kommt unser Held ins Spiel: Johannes Diderik van der Waals.
Van der Waals: Der Party-Realist unter den Physikern
Van der Waals, ein niederländischer Physiker, hatte genug von der idealen Party. Er sagte sich: "Leute, das ist doch alles Quatsch! Gase sind nicht ideal! Wir müssen die Realität berücksichtigen!" Und so entwickelte er eine Gleichung, die eben diese Realität mit einbezieht: Die Van-der-Waals-Gleichung.
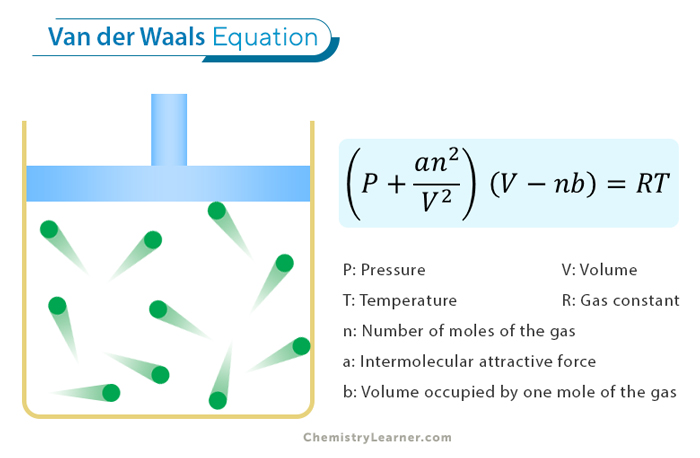
Die Van-der-Waals-Gleichung ist im Grunde genommen die ideale Gasgleichung, aber mit zwei kleinen Korrekturen. Keine Sorge, wir werden sie hier nicht komplett auseinandernehmen. Wichtig ist das Prinzip:
Die erste Korrektur berücksichtigt das Eigenvolumen der Moleküle. Sie subtrahiert von dem Gesamtvolumen des Gases einen Wert, der von der Stoffmenge und einem bestimmten Faktor (oft mit "b" bezeichnet) abhängt. Im Grunde sagt sie: "Hey, die Moleküle nehmen ja Platz weg! Das müssen wir vom Gesamtvolumen abziehen, um das tatsächliche 'freie' Volumen zu bekommen." Denk an die Party: Das freie Volumen zum Tanzen ist kleiner, wenn alle Leute dicker sind!
Die zweite Korrektur berücksichtigt die Anziehungskräfte zwischen den Molekülen. Sie addiert zum Druck einen Wert, der von der Stoffmenge, dem Volumen und einem anderen Faktor (oft mit "a" bezeichnet) abhängt. Hier sagt die Gleichung: "Die Moleküle ziehen sich an! Das verringert den tatsächlichen Druck auf die Gefäßwände, weil sie sich gegenseitig 'festhalten'." Wieder die Party: Wenn alle Leute sich an den Händen halten, ist der Drang zur Tür hin geringer!
Warum ist das Ganze wichtig?
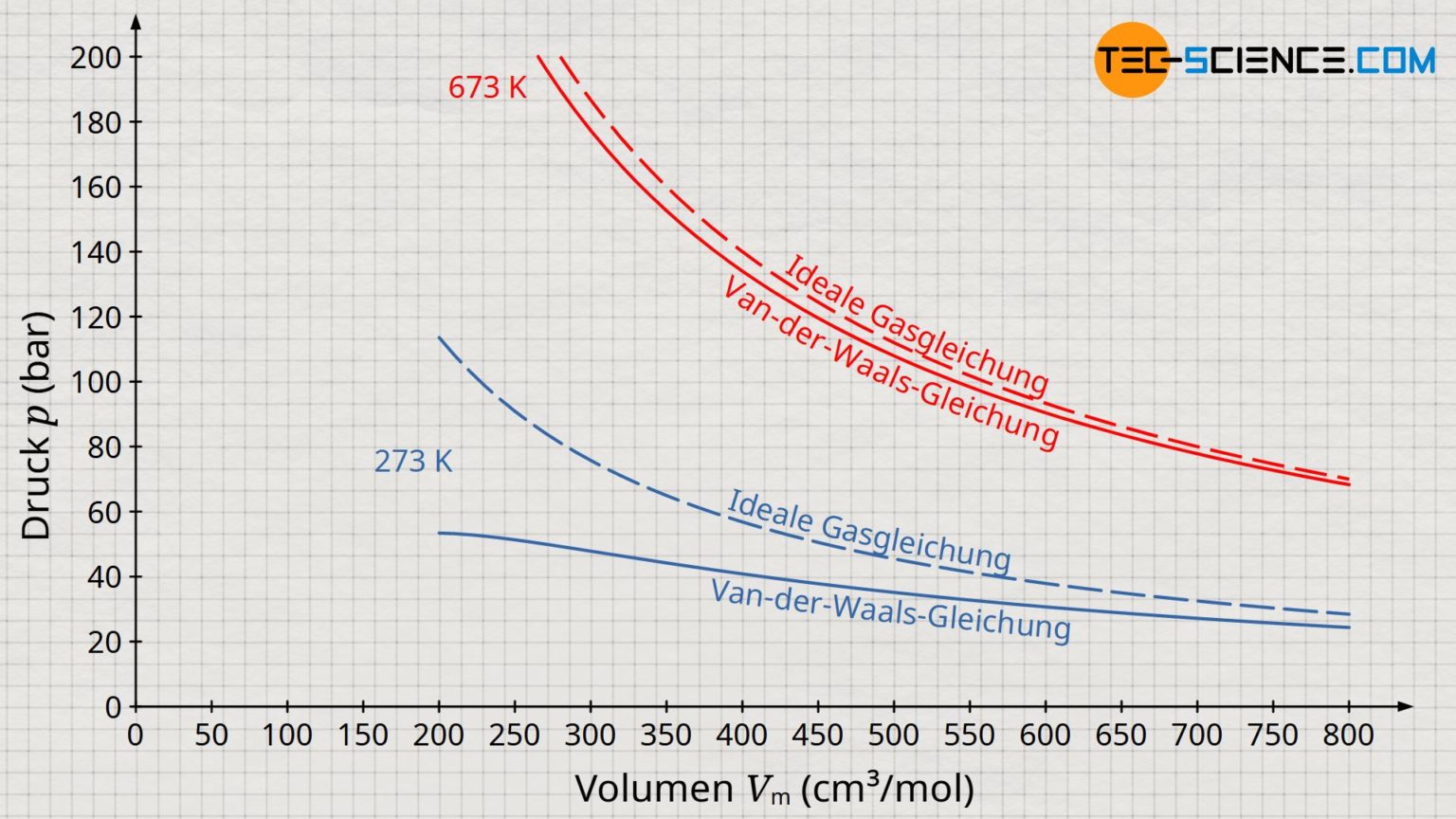
Die Van-der-Waals-Gleichung ist viel genauer als die ideale Gasgleichung, besonders bei hohen Drücken und niedrigen Temperaturen. Das ist wichtig für alle möglichen Anwendungen, von der Entwicklung von Kühlmitteln bis hin zur Herstellung von Kunststoffen. Denn wenn man verstehen will, wie sich Gase und Flüssigkeiten verhalten, muss man eben die Realität berücksichtigen – inklusive der kleinen "Anrempeleien" und "Umarmungen" zwischen den Molekülen.
Denk an die überfüllte Party. Wenn du wissen willst, ob die Klimaanlage ausreicht, um die Luft kühl zu halten, musst du wissen, wie viel Platz wirklich zum Atmen da ist und wie stark die Leute aneinanderkleben. Die ideale Gasgleichung würde dir sagen: "Alles super, genug Platz!" Die Van-der-Waals-Gleichung würde sagen: "Moment mal, da ist es ganz schön stickig, die Leute kleben aneinander, wir brauchen mehr Kühlung!"
Mehr als nur eine Gleichung: Eine Lektion in Realismus
Die Geschichte der Van-der-Waals-Gleichung ist mehr als nur eine Geschichte über Physik. Es ist eine Geschichte darüber, wie wichtig es ist, die Realität anzuerkennen, auch wenn sie komplizierter ist als die Theorie. Van der Waals hat uns gezeigt, dass wir die Welt nicht immer idealisieren können. Manchmal müssen wir die kleinen Fehler und Unvollkommenheiten mit einbeziehen, um ein wirklich gutes Verständnis zu bekommen.
Und vielleicht, ganz vielleicht, können wir von ihm auch lernen, wie wir unsere eigenen "Partys" besser gestalten – sei es im übertragenen oder im wörtlichen Sinne. Denn wer will schon eine überfüllte, stickige Party, wenn man mit ein bisschen Realismus und Planung eine wirklich unvergessliche Feier veranstalten kann?
Und falls du dich das nächste Mal fragst, warum dein Kühlschrank so gut funktioniert, denk an Van der Waals und seine realistischen Moleküle. Er hat uns ein Stück näher daran gebracht, die Welt zu verstehen – eine "Anziehungskraft" nach der anderen.