Van Der Waals Kräfte Alkane
Willkommen! Dieser Artikel erklärt Ihnen die Van-der-Waals-Kräfte im Zusammenhang mit Alkanen. Er soll Ihnen helfen, diese wichtigen chemischen Konzepte einfach zu verstehen, besonders wenn Sie neu in Deutschland sind oder sich mit Chemie befassen.
Was sind Van-der-Waals-Kräfte?
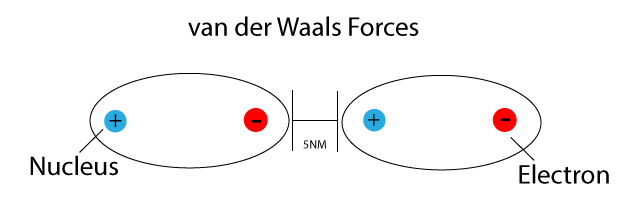
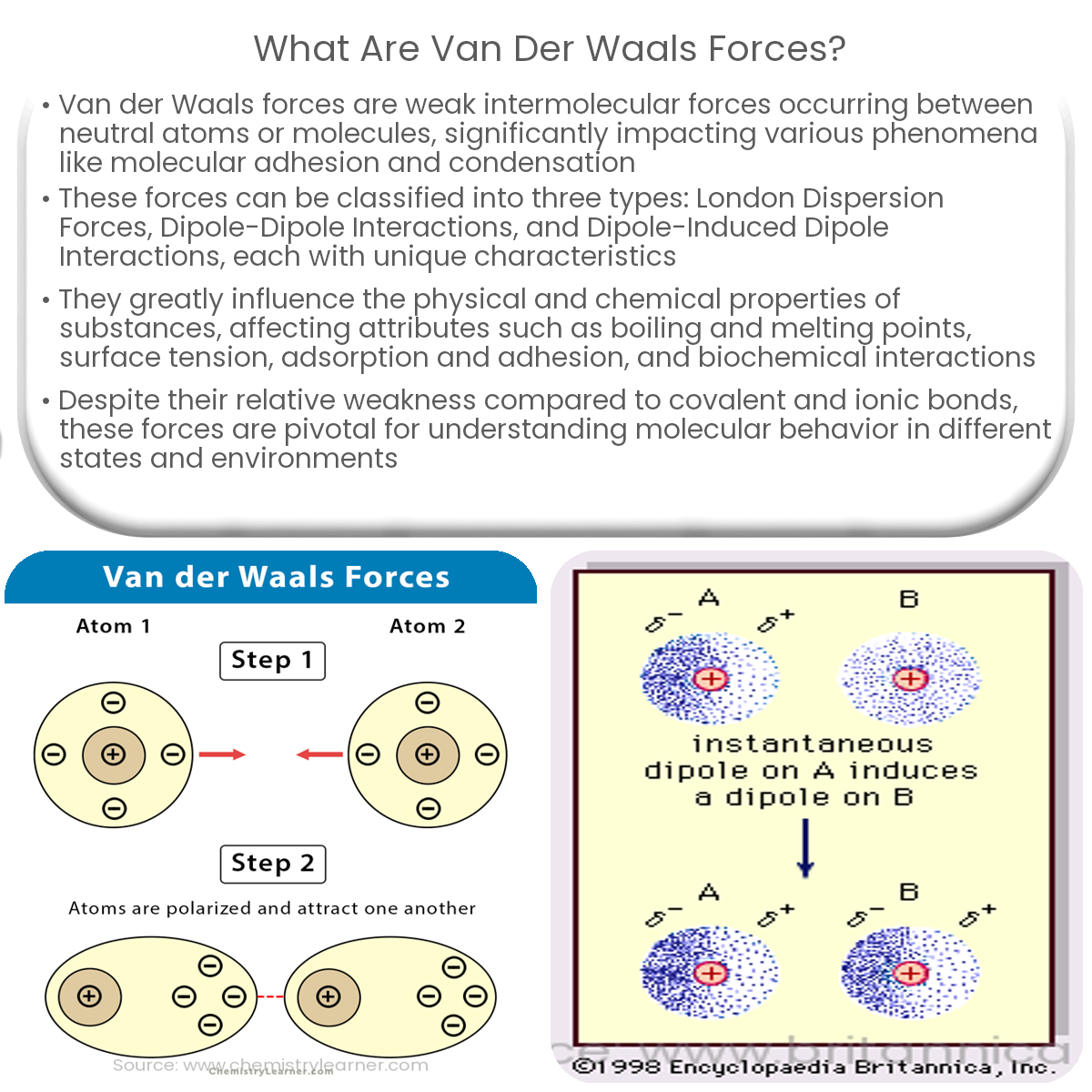
Van-der-Waals-Kräfte sind schwache, zwischenmolekulare Anziehungskräfte, die zwischen allen Atomen und Molekülen auftreten können. Sie sind nach dem niederländischen Physiker Johannes Diderik van der Waals benannt. Diese Kräfte spielen eine entscheidende Rolle bei der Bestimmung der physikalischen Eigenschaften vieler Stoffe, wie z.B. Siedepunkte, Schmelzpunkte und Löslichkeit. Es ist wichtig zu verstehen, dass Van-der-Waals-Kräfte viel schwächer sind als kovalente oder ionische Bindungen, die Atome innerhalb eines Moleküls zusammenhalten. Sie sind jedoch entscheidend für die Wechselwirkungen zwischen Molekülen.
Es gibt drei Haupttypen von Van-der-Waals-Kräften:
1. Dipol-Dipol-Wechselwirkungen
Dipol-Dipol-Wechselwirkungen treten zwischen Molekülen auf, die ein permanentes Dipolmoment besitzen. Ein Dipolmoment entsteht, wenn die Elektronegativität der Atome in einem Molekül unterschiedlich ist, was zu einer ungleichen Verteilung der Ladung führt. Ein Ende des Moleküls wird leicht positiv (δ+) und das andere leicht negativ (δ-). Diese polarisierten Moleküle ziehen sich dann gegenseitig an, wobei der positive Pol eines Moleküls den negativen Pol eines anderen anzieht.
Beispiel: Wasser (H₂O) ist ein polares Molekül aufgrund der unterschiedlichen Elektronegativität von Sauerstoff und Wasserstoff. Die Sauerstoffatome ziehen stärker an den Elektronen als die Wasserstoffatome, was zu einem Dipolmoment führt. Die Dipol-Dipol-Wechselwirkungen zwischen Wassermolekülen tragen wesentlich zu seinen hohen Siedepunkt im Vergleich zu Molekülen ähnlicher Größe bei.
2. Dipol-induzierte Dipol-Wechselwirkungen (Debye-Kräfte)
Dipol-induzierte Dipol-Wechselwirkungen treten zwischen einem polaren Molekül (mit einem permanenten Dipol) und einem unpolaren Molekül auf. Das polare Molekül kann die Elektronenwolke des unpolaren Moleküls verzerren und so einen induzierten Dipol erzeugen. Das polare Molekül und der induzierte Dipol ziehen sich dann gegenseitig an.
Beispiel: Wenn Ammoniak (NH₃), ein polares Molekül, mit Sauerstoff (O₂), einem unpolaren Molekül, in Kontakt kommt, induziert das Ammoniakmolekül einen Dipol im Sauerstoffmolekül. Die daraus resultierende Anziehungskraft ist jedoch schwächer als bei Dipol-Dipol-Wechselwirkungen.
3. London-Dispersionskräfte (auch bekannt als induzierte Dipol-induzierte Dipol-Wechselwirkungen)
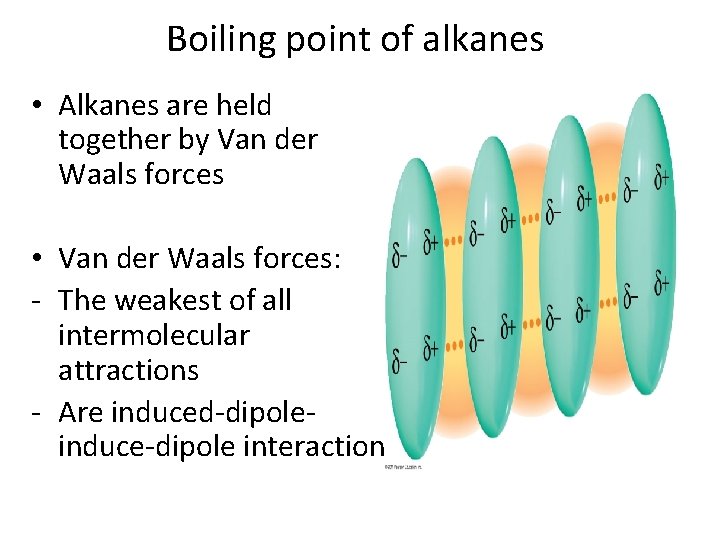
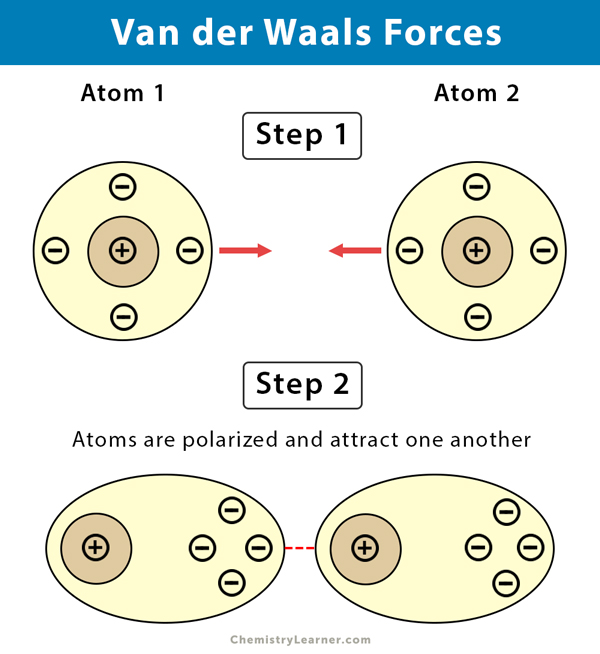
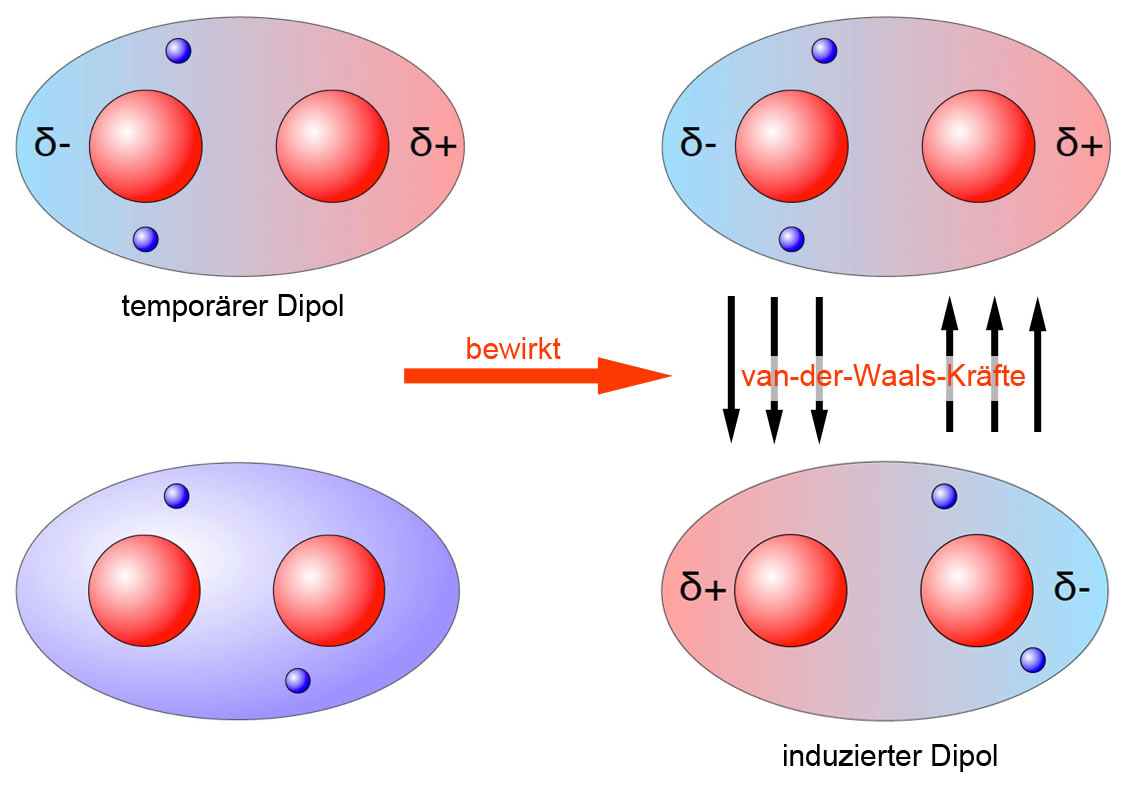
London-Dispersionskräfte sind die schwächsten der Van-der-Waals-Kräfte und treten zwischen allen Atomen und Molekülen auf, sowohl polaren als auch unpolaren. Sie entstehen durch momentane, fluktuierende Dipole, die durch die zufällige Bewegung von Elektronen erzeugt werden. Obwohl diese Dipole nur kurzlebig sind, können sie in benachbarten Atomen oder Molekülen Dipole induzieren, was zu einer schwachen Anziehungskraft führt. Die Stärke der London-Dispersionskräfte hängt von der Anzahl der Elektronen im Molekül und seiner Oberfläche ab. Größere Moleküle mit mehr Elektronen und größeren Oberflächen haben stärkere Dispersionskräfte.
Beispiel: Edelgase wie Helium (He) und Neon (Ne) existieren als einzelne Atome und haben keine permanente Polarität. Die einzigen intermolekularen Kräfte, die zwischen ihnen wirken, sind London-Dispersionskräfte. Diese Kräfte sind jedoch stark genug, um diese Gase bei sehr niedrigen Temperaturen zu verflüssigen.
Alkane und Van-der-Waals-Kräfte
Alkane sind gesättigte Kohlenwasserstoffe, die aus Kohlenstoff- und Wasserstoffatomen bestehen, die durch Einfachbindungen miteinander verbunden sind. Sie haben die allgemeine Formel CnH2n+2, wobei 'n' die Anzahl der Kohlenstoffatome ist. Beispiele für Alkane sind Methan (CH₄), Ethan (C₂H₆), Propan (C₃H₈) und Butan (C₄H₁₀).
Alkane sind im Allgemeinen unpolare Moleküle, da die Elektronegativitätsdifferenz zwischen Kohlenstoff und Wasserstoff gering ist. Folglich sind die London-Dispersionskräfte die dominierenden intermolekularen Kräfte, die zwischen Alkanen wirken. Dies bedeutet, dass die physikalischen Eigenschaften von Alkanen, wie z.B. Siedepunkte und Schmelzpunkte, stark von der Stärke der London-Dispersionskräfte beeinflusst werden.
Hier sind einige wichtige Punkte zu beachten:
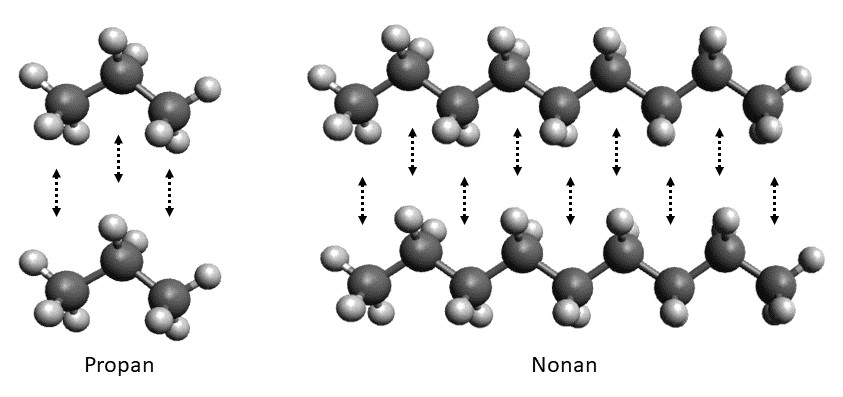
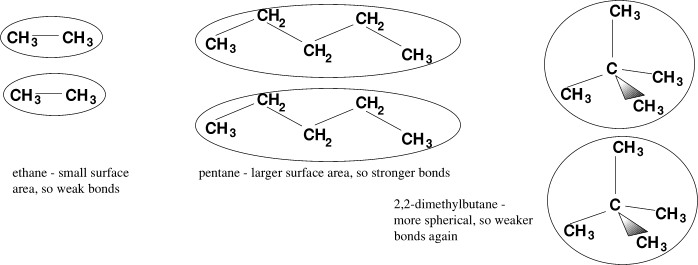
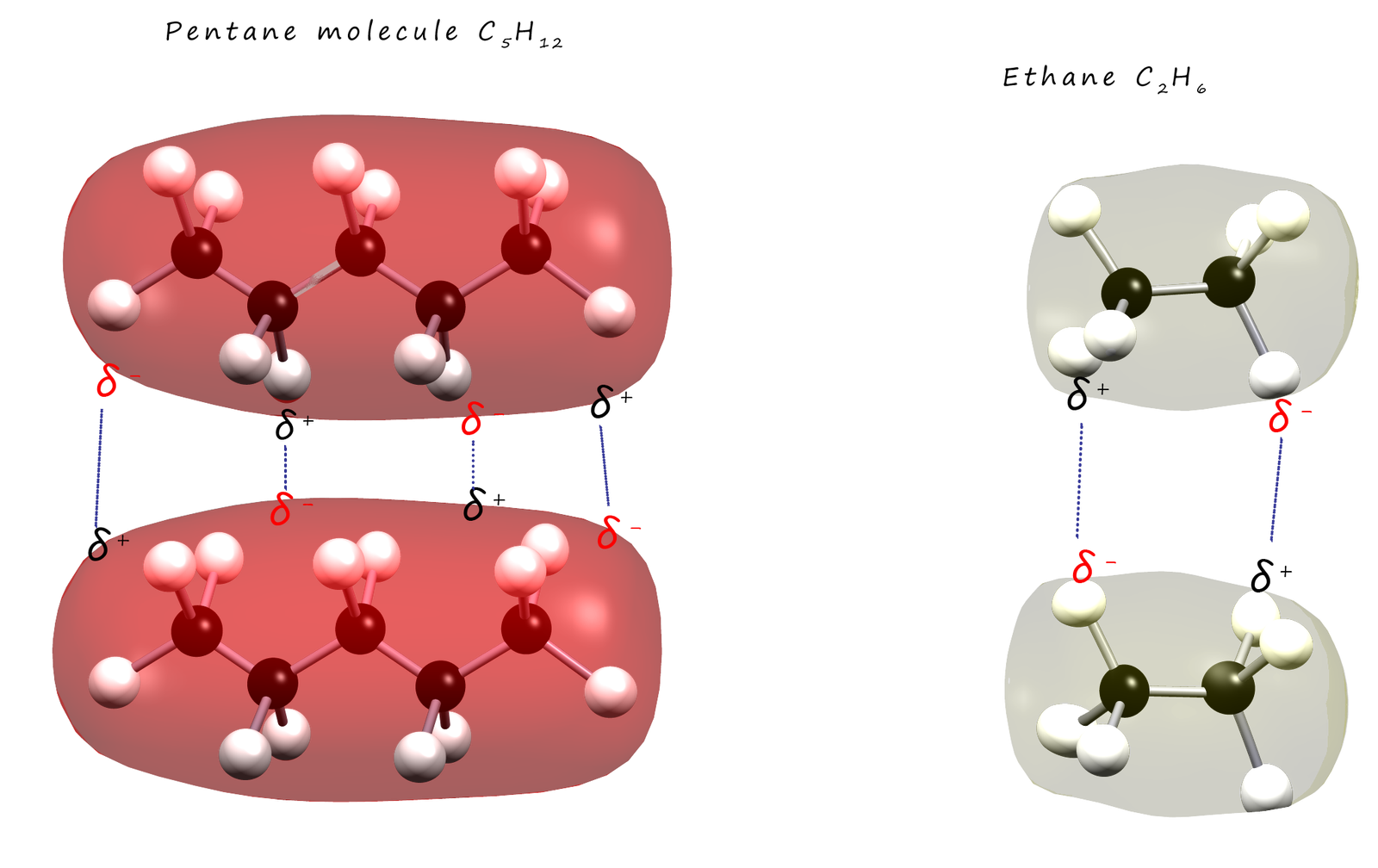
- Zunehmende Molekülgröße: Mit zunehmender Anzahl der Kohlenstoffatome in einem Alkan nimmt auch seine Molekülmasse und seine Oberfläche zu. Dies führt zu einer Zunahme der London-Dispersionskräfte. Daher haben Alkane mit längeren Ketten im Allgemeinen höhere Siedepunkte und Schmelzpunkte als Alkane mit kürzeren Ketten. Beispielsweise hat Butan (C₄H₁₀) einen höheren Siedepunkt als Ethan (C₂H₆).
- Verzweigung: Die Struktur von Alkanen beeinflusst ebenfalls die Stärke der London-Dispersionskräfte. Verzweigte Alkane haben kleinere Oberflächen als lineare Alkane mit der gleichen Anzahl an Kohlenstoffatomen. Dies führt zu schwächeren Dispersionskräften und niedrigeren Siedepunkten. Beispielsweise hat n-Butan (lineares Butan) einen höheren Siedepunkt als Isobutan (verzweigtes Butan).
- Aggregatzustand: Kurzkettige Alkane (z.B. Methan, Ethan, Propan und Butan) sind bei Raumtemperatur Gase, da die Dispersionskräfte relativ schwach sind. Alkane mit mittleren Kettenlängen (z.B. Pentan, Hexan, Heptan und Octan) sind Flüssigkeiten, während langkettige Alkane (z.B. Eicosan) bei Raumtemperatur Feststoffe sind.
Bedeutung der Van-der-Waals-Kräfte bei Alkanen
Das Verständnis der Van-der-Waals-Kräfte bei Alkanen ist aus mehreren Gründen wichtig:
- Erdölraffinerie: Die Trennung von Erdölkomponenten basiert auf Unterschieden in ihren Siedepunkten, die direkt mit der Stärke der London-Dispersionskräfte zusammenhängen. Alkane mit unterschiedlichen Kettenlängen werden durch fraktionierte Destillation getrennt.
- Kunststoffe: Viele Kunststoffe sind aus Polymeren aufgebaut, die aus langen Kohlenwasserstoffketten bestehen. Die Van-der-Waals-Kräfte zwischen diesen Ketten beeinflussen die Festigkeit, Flexibilität und Schmelztemperatur des Kunststoffs.
- Biologie: Van-der-Waals-Kräfte spielen eine wichtige Rolle bei der Faltung von Proteinen und der Wechselwirkung von Enzymen mit Substraten. Obwohl Alkane in lebenden Organismen nicht so häufig vorkommen wie andere Moleküle, tragen die gleichen Prinzipien der intermolekularen Wechselwirkungen zur Struktur und Funktion biologischer Moleküle bei.
- Lösungsmittel: Alkane werden oft als unpolare Lösungsmittel verwendet. Ihre Fähigkeit, andere unpolare Substanzen zu lösen, beruht auf den London-Dispersionskräften, die zwischen den Alkanmolekülen und den gelösten Substanzen wirken.
Zusammenfassung
Van-der-Waals-Kräfte sind schwache, aber wichtige intermolekulare Anziehungskräfte, die die physikalischen Eigenschaften von Stoffen beeinflussen. Bei Alkanen sind die London-Dispersionskräfte die dominierenden Van-der-Waals-Kräfte. Die Stärke dieser Kräfte hängt von der Größe und Form des Moleküls ab. Das Verständnis dieser Kräfte ist entscheidend für viele Anwendungen in Chemie, Ingenieurwesen und Biologie.
Ich hoffe, dieser Artikel hat Ihnen ein besseres Verständnis der Van-der-Waals-Kräfte im Zusammenhang mit Alkanen vermittelt. Wenn Sie weitere Fragen haben, zögern Sie bitte nicht, diese zu stellen. Willkommen in Deutschland und viel Erfolg beim Erlernen neuer Dinge!
Weitere Ressourcen
Wenn Sie Ihr Wissen weiter vertiefen möchten, finden Sie hier einige empfohlene Ressourcen:
- Chemie-Lehrbücher: Suchen Sie in Bibliotheken oder Buchhandlungen nach Chemie-Lehrbüchern für die Sekundarstufe oder das Studium.
- Online-Kurse: Plattformen wie Coursera, edX und Khan Academy bieten Chemie-Kurse an, die auch die Van-der-Waals-Kräfte behandeln.
- Wissenschaftliche Artikel: Wenn Sie ein tiefergehendes Verständnis suchen, können Sie wissenschaftliche Artikel in Fachzeitschriften wie der "Journal of Chemical Physics" oder "Angewandte Chemie" finden (Zugang über Universitätsbibliotheken).
- Deutschkurse mit wissenschaftlichem Schwerpunkt: Einige Sprachschulen bieten Deutschkurse an, die speziell auf die Bedürfnisse von Wissenschaftlern und Ingenieuren zugeschnitten sind.