Van Der Waals Kräfte Definition
Herzlich willkommen! Vielleicht stolpern Sie gerade über den Begriff "Van-der-Waals-Kräfte" und denken: "Chemieunterricht in meinem Urlaub? Wirklich?" Keine Sorge, wir machen es unterhaltsam und relevant für Ihren Aufenthalt! Auch wenn es sich nach einer komplizierten wissenschaftlichen Angelegenheit anhört, spielen diese Kräfte eine unsichtbare, aber wichtige Rolle in der Welt um uns herum – und sogar in einigen Dingen, die Sie während Ihrer Reise erleben werden.
Was sind Van-der-Waals-Kräfte überhaupt?
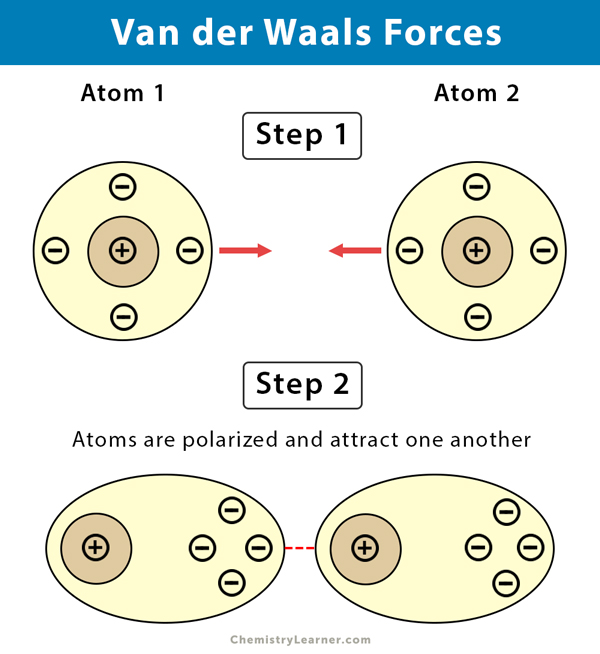
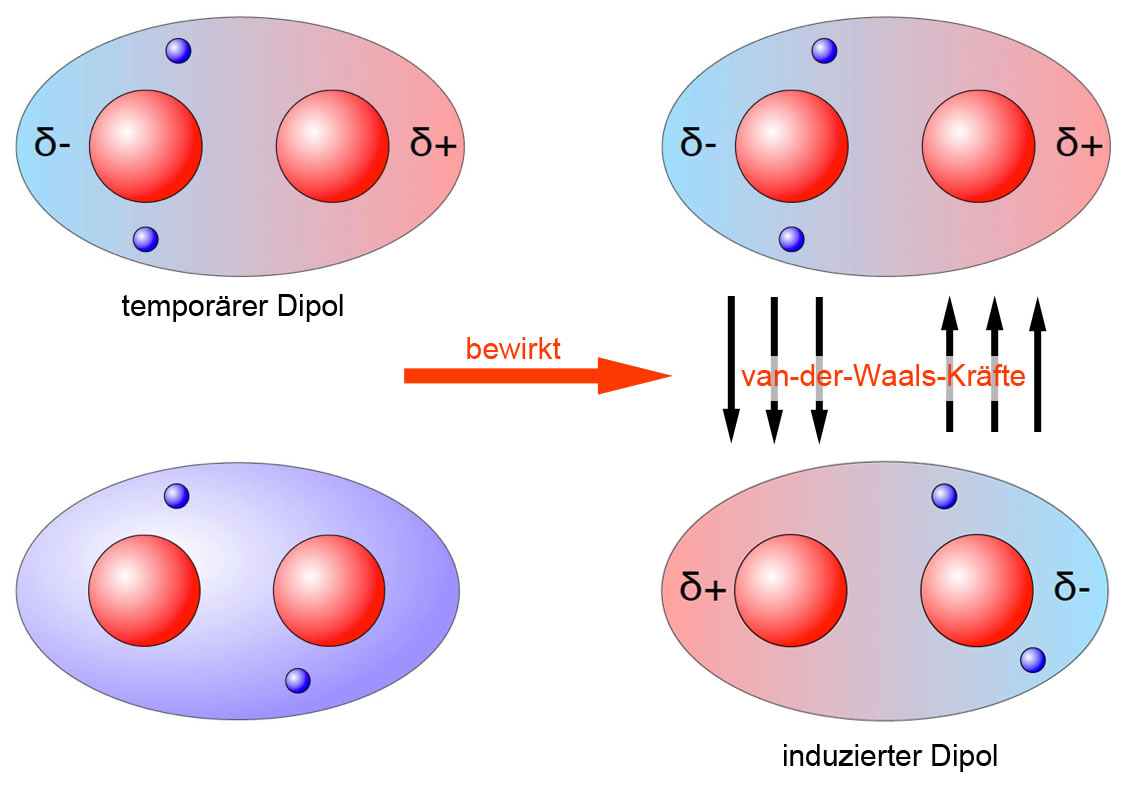
Stellen Sie sich vor, Atome und Moleküle sind wie kleine, ständig in Bewegung befindliche Teilchen. Diese Teilchen haben normalerweise keine elektrische Ladung. Aber durch ihre Bewegung können sich winzige, temporäre Ungleichgewichte in der Ladungsverteilung bilden. Das bedeutet, dass ein Teil des Moleküls für einen winzigen Moment etwas positiver und ein anderer Teil etwas negativer wird. Diese temporären, winzigen Ladungsunterschiede sind die Ursache für Van-der-Waals-Kräfte.
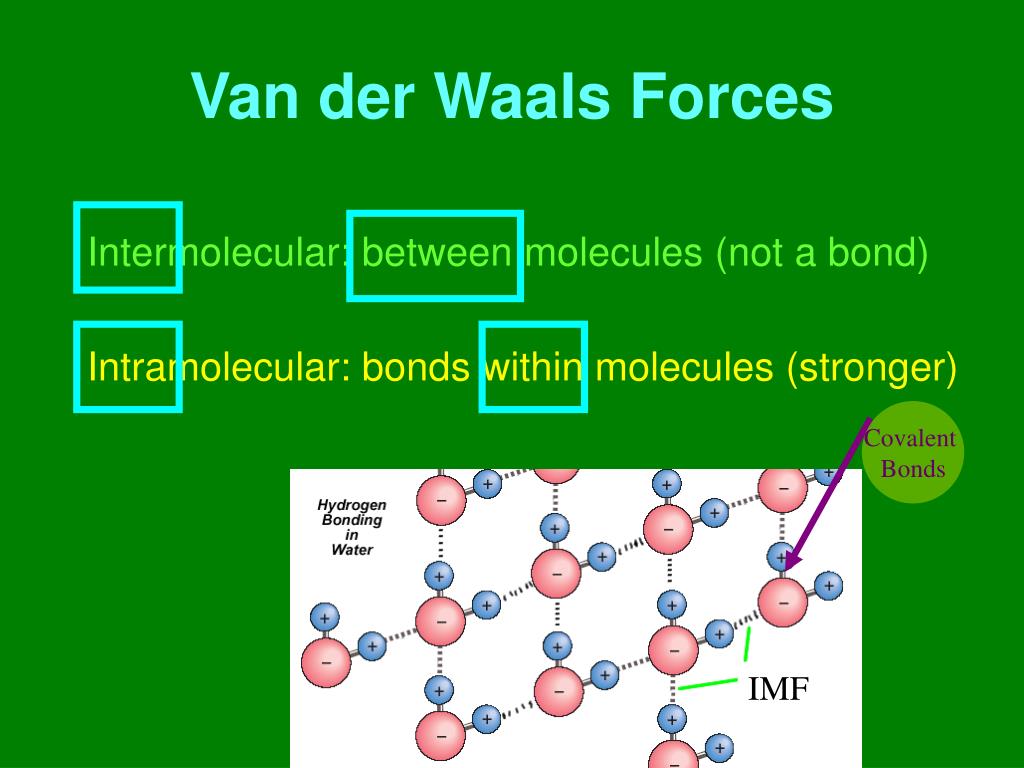
Im Wesentlichen handelt es sich um schwache, anziehende Kräfte zwischen Atomen oder Molekülen. Sie sind nicht so stark wie chemische Bindungen, die Atome *dauerhaft* verbinden, aber sie sind stark genug, um einen spürbaren Einfluss auf das Verhalten von Stoffen zu haben.
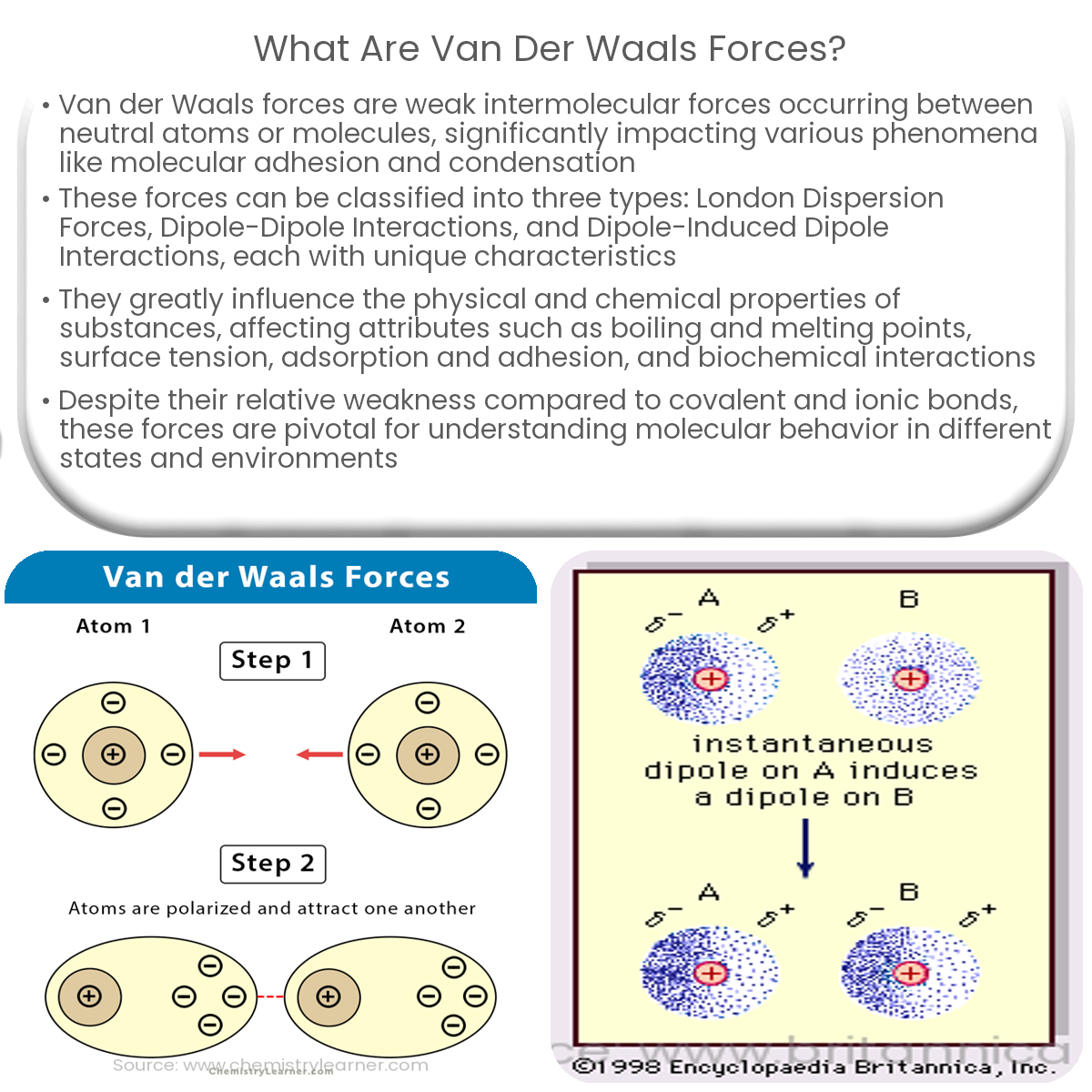
Es gibt verschiedene Arten von Van-der-Waals-Kräften, die alle auf demselben Prinzip beruhen: temporäre Ladungsverschiebungen. Die wichtigsten sind:
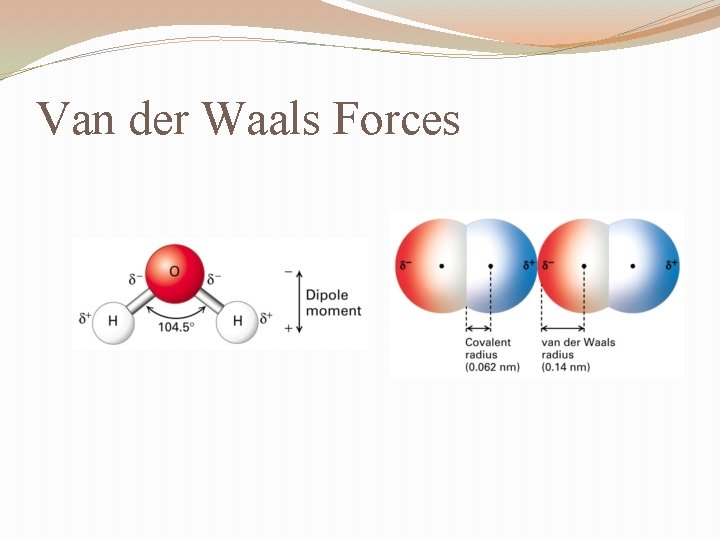
Dipol-Dipol-Wechselwirkungen
Einige Moleküle haben eine permanente, ungleiche Ladungsverteilung. Das bedeutet, dass ein Teil des Moleküls immer leicht positiv und ein anderer Teil immer leicht negativ ist. Solche Moleküle nennt man Dipole. Dipol-Dipol-Wechselwirkungen entstehen, wenn sich das positive Ende eines Dipolmoleküls zum negativen Ende eines anderen Dipolmoleküls ausrichtet und eine anziehende Kraft entsteht. Denken Sie daran wie an kleine Magnete, die sich anziehen.
Dipol-induzierte Dipol-Wechselwirkungen
Ein Dipolmolekül kann auch ein nicht-polares Molekül, also eines ohne permanente Ladungsverteilung, beeinflussen. Das Dipolmolekül "induziert" eine temporäre Ladungsverschiebung im nicht-polaren Molekül, sodass dieses auch zu einem temporären Dipol wird. Dadurch entsteht eine anziehende Kraft zwischen den beiden Molekülen.
London-Dispersionskräfte (auch London-Kräfte genannt)
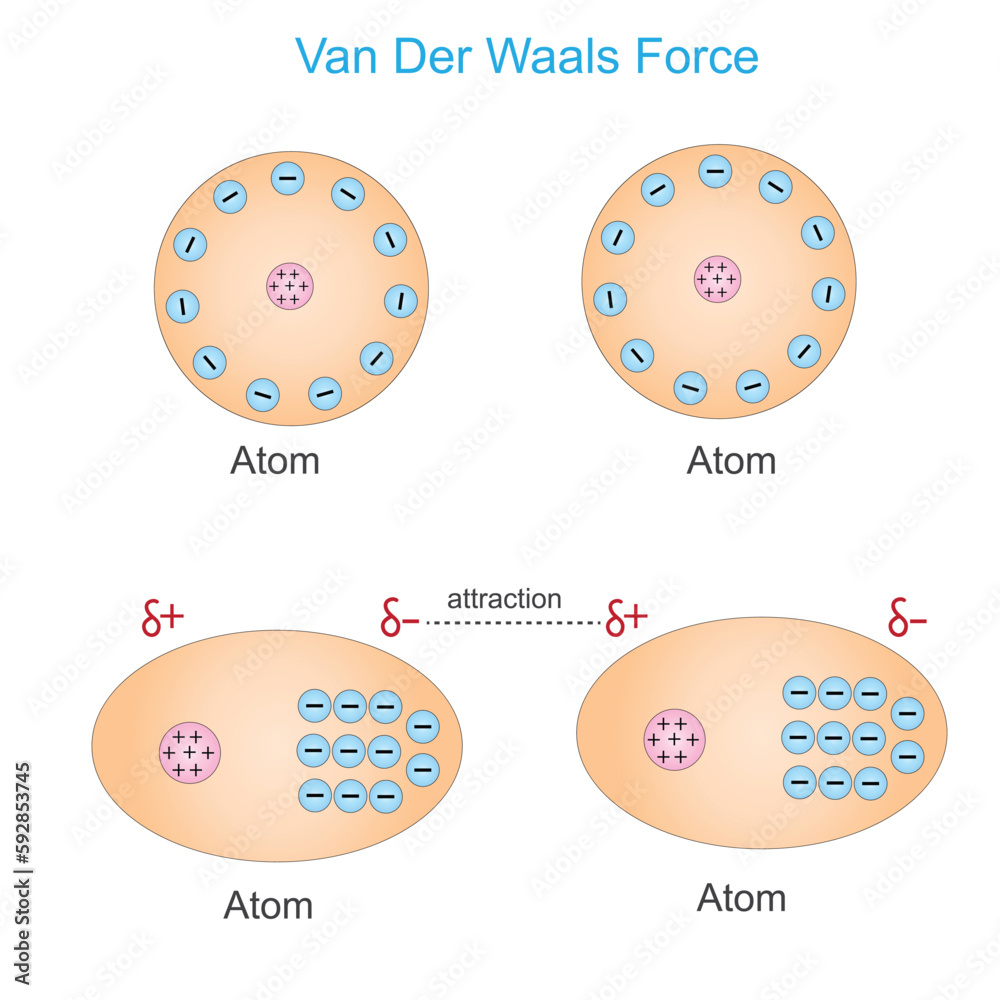
Diese sind die wichtigsten Van-der-Waals-Kräfte und treten zwischen *allen* Atomen und Molekülen auf, egal ob polar oder unpolar. Sie entstehen durch die zufällige Bewegung von Elektronen innerhalb des Moleküls. Diese Bewegung erzeugt momentane, temporäre Dipole, die dann andere Moleküle beeinflussen und anziehen. Je größer das Molekül und je mehr Elektronen es hat, desto stärker sind die London-Dispersionskräfte.
Warum sind Van-der-Waals-Kräfte wichtig für Reisende?
Auch wenn Sie die wissenschaftliche Definition vielleicht nicht auswendig lernen müssen, spielen Van-der-Waals-Kräfte eine Rolle in vielen Dingen, die Sie während Ihrer Reise erleben werden. Hier sind ein paar Beispiele:
- Geckos an Wänden: Haben Sie sich jemals gefragt, wie Geckos an glatten Oberflächen wie Wänden laufen können? Es liegt an den Millionen winziger Härchen an ihren Füßen. Diese Härchen maximieren die Kontaktfläche und ermöglichen es den Van-der-Waals-Kräften zwischen den Härchen und der Oberfläche, stark genug zu werden, um das Gewicht des Geckos zu tragen.
- Oberflächenspannung von Wasser: Wenn Sie eine Tasse Tee trinken, beobachten Sie die Oberflächenspannung des Wassers. Van-der-Waals-Kräfte zwischen den Wassermolekülen halten sie zusammen und bilden eine Art "Haut" an der Oberfläche. Deshalb können manche Insekten auf dem Wasser laufen.
- Kochen in höheren Lagen: Wenn Sie in den Bergen kochen, stellen Sie fest, dass Wasser schneller kocht. Das liegt daran, dass der Luftdruck geringer ist. Die Wassermoleküle benötigen weniger Energie, um die anziehenden Van-der-Waals-Kräfte zu überwinden und in den gasförmigen Zustand überzugehen.
- Kleidung und Textilien: Die Weichheit und der Tragekomfort Ihrer Kleidung hängen auch mit Van-der-Waals-Kräften zusammen. Die Fasern in Stoffen werden durch diese Kräfte zusammengehalten. Je schwächer die Kräfte, desto weicher fühlt sich der Stoff an.
- Die Eigenschaften von Flüssigkeiten und Feststoffen: Ob etwas eine Flüssigkeit, ein Feststoff oder ein Gas ist, hängt von der Stärke der Van-der-Waals-Kräfte zwischen den Molekülen ab. Stärkere Kräfte bedeuten höhere Schmelz- und Siedepunkte.
Van-der-Waals-Kräfte und Ihr kulinarisches Erlebnis
Auch beim Essen spielen diese Kräfte eine Rolle. Die Textur, der Geschmack und sogar die Aromen, die Sie wahrnehmen, werden von der Interaktion der Moleküle in Ihren Lebensmitteln beeinflusst.
- Schokolade: Die cremige Textur von Schokolade wird durch die Anordnung der Fettmoleküle ermöglicht, die durch Van-der-Waals-Kräfte zusammengehalten werden.
- Käse: Die verschiedenen Käsesorten haben unterschiedliche Texturen und Schmelzeigenschaften, die von den unterschiedlichen Arten von Proteinen und Fetten und der Art und Weise, wie sie durch Van-der-Waals-Kräfte interagieren, abhängen.
- Aromen: Die Duftstoffe, die Sie riechen, sind Moleküle, die sich in der Luft befinden. Die Van-der-Waals-Kräfte zwischen diesen Duftmolekülen und den Rezeptoren in Ihrer Nase bestimmen, welche Aromen Sie wahrnehmen.
Van-der-Waals-Kräfte im Alltag: Praktische Beispiele
Hier sind einige weitere alltägliche Beispiele, in denen Van-der-Waals-Kräfte eine Rolle spielen:
- Haftung von Klebstoffen: Klebstoffe funktionieren, weil sie starke Van-der-Waals-Kräfte mit den Oberflächen bilden, die sie verbinden.
- Kondensation von Gasen: Wenn ein Gas abgekühlt wird, verlangsamen sich die Moleküle und die Van-der-Waals-Kräfte werden stärker, was dazu führt, dass das Gas kondensiert und eine Flüssigkeit bildet.
- Kapillarwirkung: Die Kapillarwirkung, die das Aufsteigen von Wasser in einem dünnen Röhrchen (wie in Pflanzen) ermöglicht, wird durch die Van-der-Waals-Kräfte zwischen den Wassermolekülen und der Röhrchenwand verursacht.
- Adsorption: Die Adsorption, bei der sich Moleküle an der Oberfläche eines Materials anlagern, wird ebenfalls durch Van-der-Waals-Kräfte angetrieben. Dies wird beispielsweise in Aktivkohlefiltern verwendet, um Verunreinigungen aus Wasser oder Luft zu entfernen.
Fazit: Die unsichtbare Welt um uns herum
Van-der-Waals-Kräfte sind ein faszinierendes Beispiel dafür, wie winzige, unsichtbare Kräfte einen großen Einfluss auf die Welt um uns herum haben. Auch wenn Sie kein Wissenschaftler sein müssen, um Ihren Urlaub zu genießen, kann es Ihnen eine neue Wertschätzung für die Naturwissenschaften geben, wenn Sie sich bewusst machen, wie diese Kräfte unseren Alltag beeinflussen. Denken Sie also beim nächsten Spaziergang an den Geckos, beim Kochen an den Bergen oder beim Genießen einer lokalen Spezialität an die Van-der-Waals-Kräfte, die im Hintergrund wirken! Sie werden feststellen, dass die Welt viel spannender ist, als Sie vielleicht denken!


![Van Der Waals Kräfte Definition Van-der-Waals-Kräfte · Entstehung & Beispiel · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2019/08/Van-der-Waals-Kräfte_1-1-1024x576.jpg)