Warum Ist Wasser Ein Dipol
Eine unsichtbare Kraft, eine subtile Anziehung, die das Leben, wie wir es kennen, überhaupt erst ermöglicht: Die Rede ist vom Dipolcharakter des Wassers. In Museen und Wissenschaftszentren weltweit wird dieses faszinierende Phänomen oft anhand von interaktiven Ausstellungen und anschaulichen Modellen erklärt. Doch was steckt wirklich dahinter, und warum ist Wasser ein Dipol?
Die molekulare Grundlage: Sauerstoff und Wasserstoff
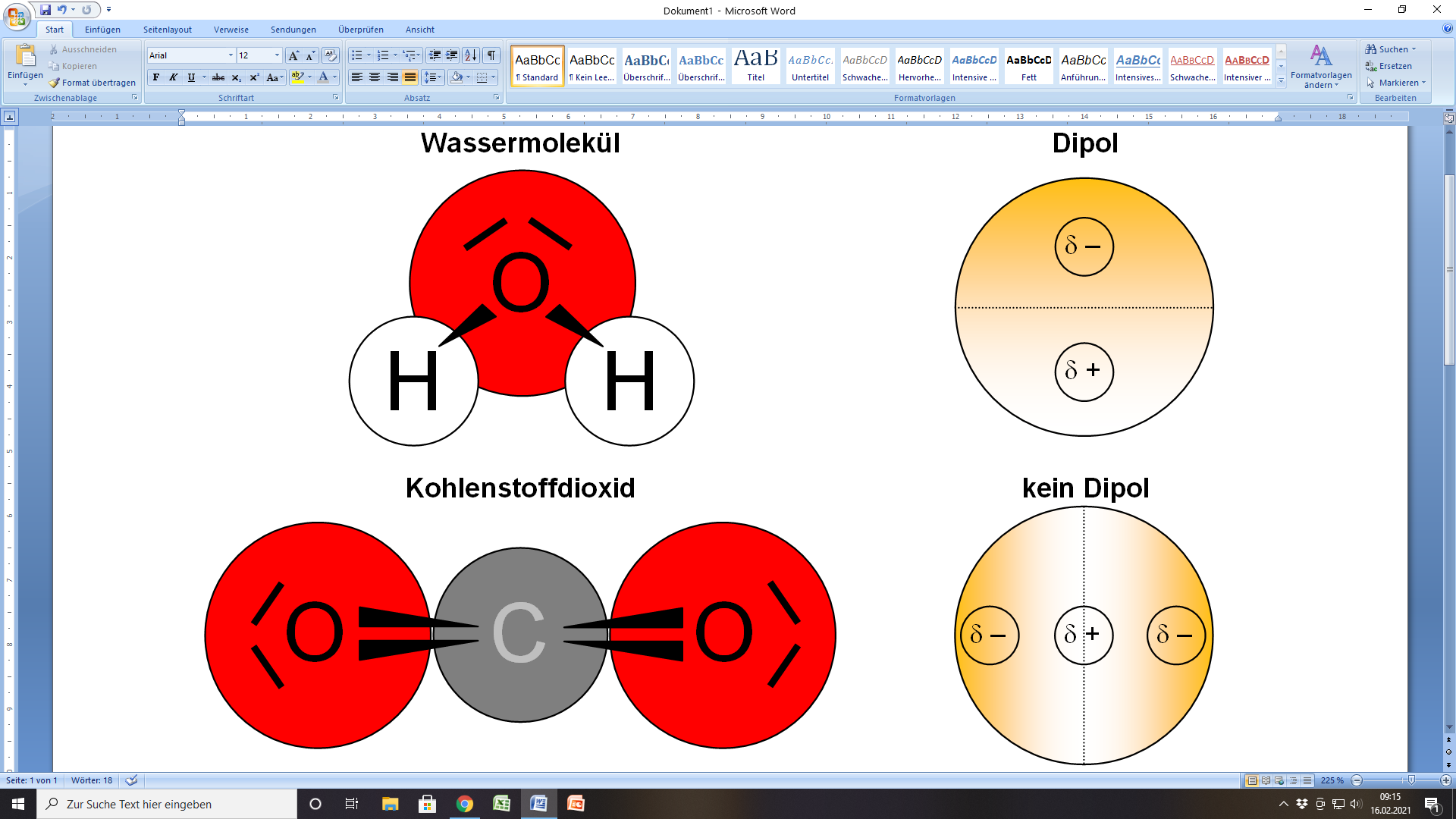
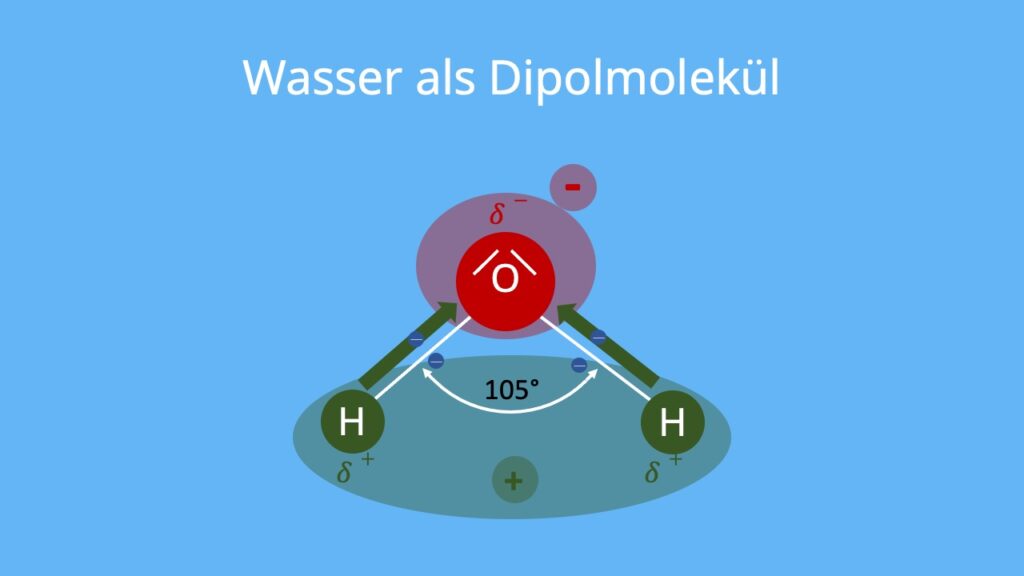
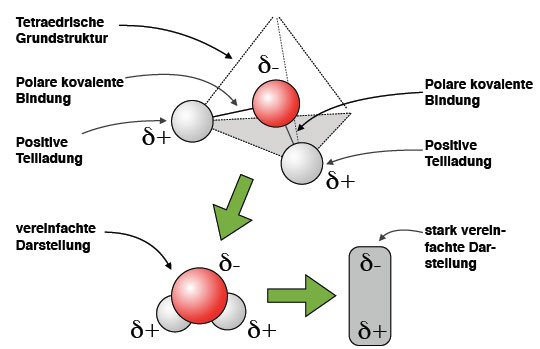
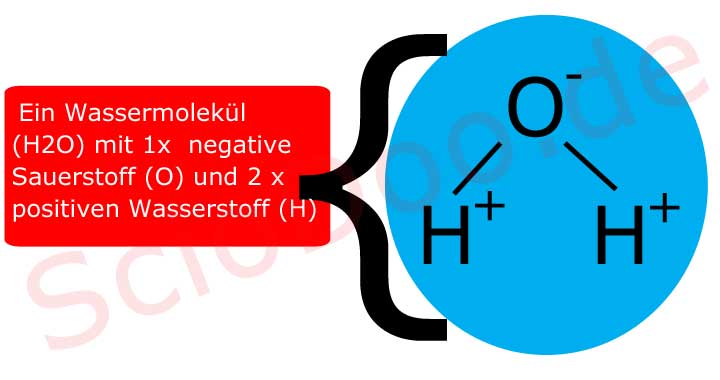
Um den Dipolcharakter des Wassers zu verstehen, müssen wir uns zunächst seine molekulare Struktur vor Augen führen. Ein Wassermolekül (H2O) besteht aus einem Sauerstoffatom (O) und zwei Wasserstoffatomen (H). Diese Atome sind nicht linear angeordnet, sondern bilden einen Winkel von etwa 104,5 Grad. Diese ungewöhnliche Geometrie ist entscheidend für die Entstehung des Dipols.
Das Sauerstoffatom ist wesentlich elektronegativer als die beiden Wasserstoffatome. Elektronegativität ist ein Maß für die Fähigkeit eines Atoms, Elektronen in einer chemischen Bindung an sich zu ziehen. Da Sauerstoff eine höhere Elektronegativität besitzt, zieht es die Elektronenpaare, die es mit den Wasserstoffatomen teilt, stärker an sich. Das Ergebnis ist eine ungleiche Verteilung der Elektronendichte innerhalb des Moleküls.
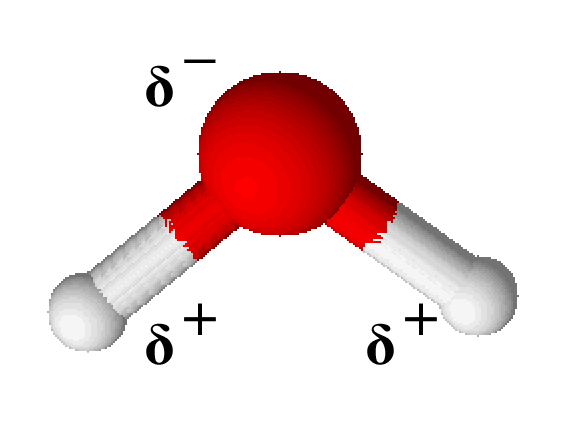
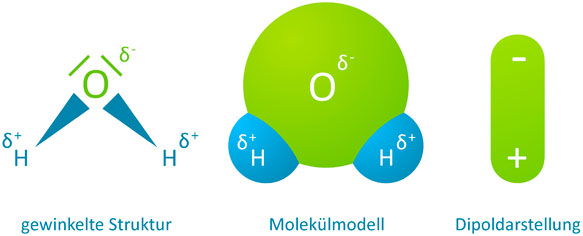
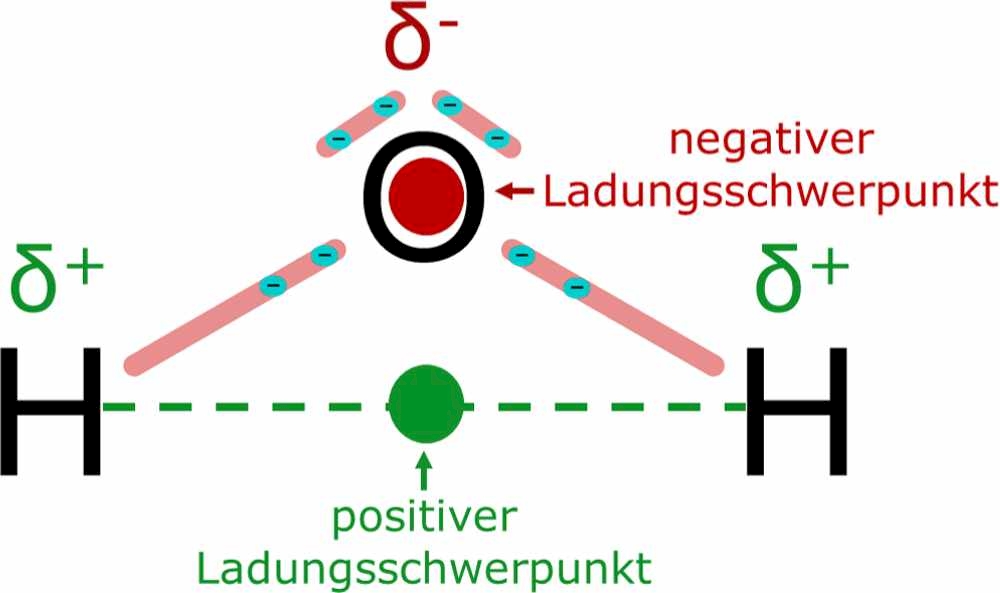
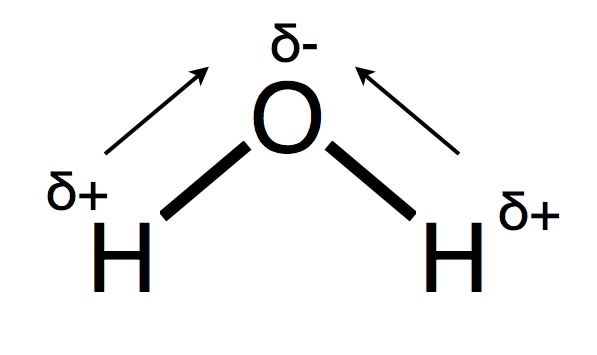
Genauer gesagt, die Elektronen verbringen mehr Zeit in der Nähe des Sauerstoffatoms, wodurch dieses eine partielle negative Ladung (δ-) erhält. Im Gegenzug verlieren die Wasserstoffatome Elektronenanteile und bekommen somit eine partielle positive Ladung (δ+). Diese partiellen Ladungen sind nicht gleichzusetzen mit vollständigen Ionenladungen, aber sie erzeugen dennoch ein deutliches Ungleichgewicht innerhalb des Moleküls. Dieses Ungleichgewicht ist es, was Wasser zu einem Dipol macht.
Der Dipolmoment: Ein Vektor der Anziehung
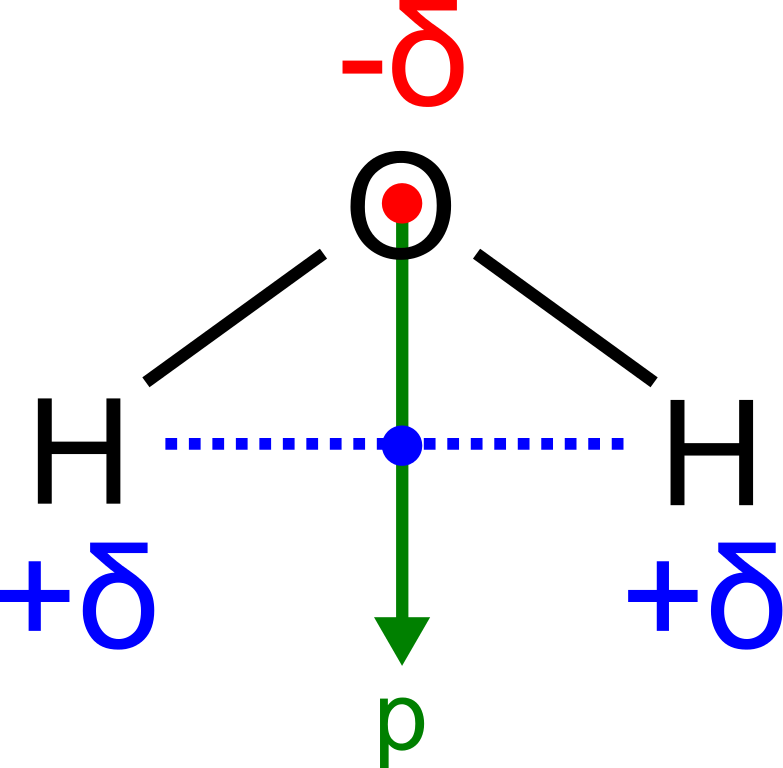
Ein Dipolmoment ist ein Vektor, der die Größe und Richtung der Ladungstrennung in einem Molekül beschreibt. Im Falle des Wassers zeigt der Dipolmoment vom Mittelpunkt zwischen den beiden Wasserstoffatomen zum Sauerstoffatom. Die Stärke des Dipolmoments hängt von der Differenz der Elektronegativitäten zwischen den Atomen und der Geometrie des Moleküls ab.
In Ausstellungen zum Thema Wasserchemie wird oft ein interaktives Modell verwendet, bei dem Besucher die Winkel zwischen den Atomen verändern können. Sie können dann beobachten, wie sich die Stärke des Dipolmoments verändert. So wird auf spielerische Weise veranschaulicht, wie wichtig die molekulare Geometrie für die Entstehung des Dipols ist. Ein lineares Molekül, wie beispielsweise Kohlendioxid (CO2), besitzt trotz polarer Bindungen kein Dipolmoment, da sich die Dipolmomente der einzelnen Bindungen aufheben.
Die Konsequenzen des Dipolcharakters: Wasser als Lösungsmittel
Der Dipolcharakter des Wassers hat weitreichende Konsequenzen für seine physikalischen und chemischen Eigenschaften. Eine der wichtigsten ist seine Fähigkeit, als universelles Lösungsmittel zu fungieren.
Polare Stoffe, wie beispielsweise Salze, bestehen aus Ionen mit positiven und negativen Ladungen. Wenn ein Salz in Wasser gegeben wird, umgeben die Wassermoleküle die Ionen. Die partiell negativen Sauerstoffatome ziehen die positiven Ionen an, während die partiell positiven Wasserstoffatome die negativen Ionen anziehen. Diese Anziehungskräfte sind stark genug, um die Ionen aus dem Kristallgitter des Salzes zu lösen und sie im Wasser zu verteilen. Dieser Vorgang wird als Solvatation bezeichnet.
Nicht-polare Stoffe, wie beispielsweise Öle, lösen sich hingegen schlecht in Wasser. Dies liegt daran, dass sie keine Ladungen besitzen, die von den Wassermolekülen angezogen werden könnten. Stattdessen stoßen sich die nicht-polaren Moleküle gegenseitig ab und bilden separate Phasen.
In Ausstellungen wird dieser Effekt oft mit einer Demonstration gezeigt, bei der Öl und Wasser in einem Becherglas gemischt werden. Die Besucher können dann beobachten, wie sich die beiden Flüssigkeiten trennen und wie die Wassermoleküle versuchen, sich voneinander fernzuhalten. Diese einfache Demonstration verdeutlicht auf anschauliche Weise die Bedeutung des Dipolcharakters für die Löslichkeit von Stoffen.
Wasserstoffbrücken: Die Stärke der Gemeinschaft
Eine weitere wichtige Konsequenz des Dipolcharakters des Wassers ist die Bildung von Wasserstoffbrücken. Eine Wasserstoffbrücke ist eine schwache Anziehungskraft zwischen einem partiell positiv geladenen Wasserstoffatom eines Wassermoleküls und einem partiell negativ geladenen Sauerstoffatom eines anderen Wassermoleküls.
Obwohl jede einzelne Wasserstoffbrücke relativ schwach ist, führen die zahlreichen Wasserstoffbrücken in flüssigem Wasser zu einer starken Kohäsion zwischen den Molekülen. Diese Kohäsion verleiht dem Wasser seine hohe Oberflächenspannung, die es ermöglicht, dass Insekten auf der Wasseroberfläche laufen können. Sie ist auch verantwortlich für die hohe spezifische Wärmekapazität des Wassers, was bedeutet, dass es viel Energie benötigt, um seine Temperatur zu erhöhen. Diese Eigenschaft ist essentiell für die Klimaregulierung.
In einigen Museen werden Modelle von Wasserstoffbrücken verwendet, um die dreidimensionale Struktur von Wasser zu veranschaulichen. Die Besucher können dann erkennen, wie die Wassermoleküle miteinander vernetzt sind und wie diese Vernetzung zu den ungewöhnlichen Eigenschaften des Wassers beiträgt.
Die Bedeutung für das Leben: Mehr als nur ein Lösungsmittel
Der Dipolcharakter des Wassers ist nicht nur für seine physikalischen und chemischen Eigenschaften von Bedeutung, sondern auch für das Leben selbst. Wasser ist das Lebenselixier. Es ist das wichtigste Lösungsmittel in lebenden Organismen und spielt eine entscheidende Rolle bei vielen biochemischen Reaktionen.
Die polare Natur des Wassers ermöglicht es, dass viele wichtige Biomoleküle, wie beispielsweise Proteine und Nukleinsäuren, in Wasser gelöst und transportiert werden können. Wasser ist auch an vielen chemischen Reaktionen beteiligt, wie beispielsweise der Photosynthese und der Zellatmung.
Darüber hinaus trägt die hohe spezifische Wärmekapazität des Wassers dazu bei, die Temperatur in lebenden Organismen zu regulieren. Dies ist besonders wichtig für Tiere, die in kalten Umgebungen leben, da es ihnen ermöglicht, ihre Körpertemperatur konstant zu halten.
Die Tatsache, dass Wasser ein Dipol ist, ist kein Zufall, sondern ein Ergebnis der fundamentalen Gesetze der Physik und Chemie. Ohne den Dipolcharakter des Wassers gäbe es kein Leben, wie wir es kennen.
Besucher, die sich mit den fundamentalen Eigenschaften von Wasser auseinandersetzen, können sich oft der Fragilität und Einzigartigkeit des Lebens auf unserem Planeten besser bewusst werden. Ausstellungen über den Dipolcharakter des Wassers sind daher nicht nur lehrreich, sondern auch ein Beitrag zur Umweltbildung.
Die Zukunft der Forschung: Ein tieferes Verständnis
Obwohl wir bereits viel über den Dipolcharakter des Wassers wissen, gibt es noch viele offene Fragen. Forscher untersuchen beispielsweise, wie sich der Dipolcharakter des Wassers unter extremen Bedingungen verändert, wie beispielsweise bei hohen Drücken oder Temperaturen. Sie erforschen auch, wie der Dipolcharakter des Wassers die Wechselwirkungen zwischen Biomolekülen beeinflusst.
Durch ein tieferes Verständnis des Dipolcharakters des Wassers können wir möglicherweise neue Technologien entwickeln, beispielsweise zur Wasseraufbereitung oder zur Entwicklung neuer Medikamente. Die Erforschung des Wassers, dieser vermeintlich einfachen Substanz, ist also auch in Zukunft von großer Bedeutung.
Der Dipolcharakter des Wassers, vermittelt durch informative Ausstellungen und anschauliche Modelle, ist ein Schlüssel zum Verständnis der Welt, in der wir leben. Es ist eine unsichtbare Kraft, die das Leben ermöglicht und die uns daran erinnert, wie eng wir mit der Natur verbunden sind. Der Besuch einer Ausstellung zu diesem Thema ist daher nicht nur eine wissenschaftliche Erfahrung, sondern auch eine Möglichkeit, die Schönheit und Komplexität der Welt um uns herum neu zu entdecken.
![Warum Ist Wasser Ein Dipol Wassermolekül • Aufbau und Eigenschaften · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2021/12/02_Aufbau-eines-Wassermoleküls-1024x576.jpg)
![Warum Ist Wasser Ein Dipol Wassermolekül • Aufbau und Eigenschaften · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2021/12/03_Wassermolekül-als-Dipol-1024x576.jpg)


/wasser_ein_dipolmolekuel.png)



![Warum Ist Wasser Ein Dipol Wassermolekül • Aufbau und Eigenschaften · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2021/12/01_Das-Wassermolekül-1024x576.jpg)