Was Ist Die Ionisierungsenergie
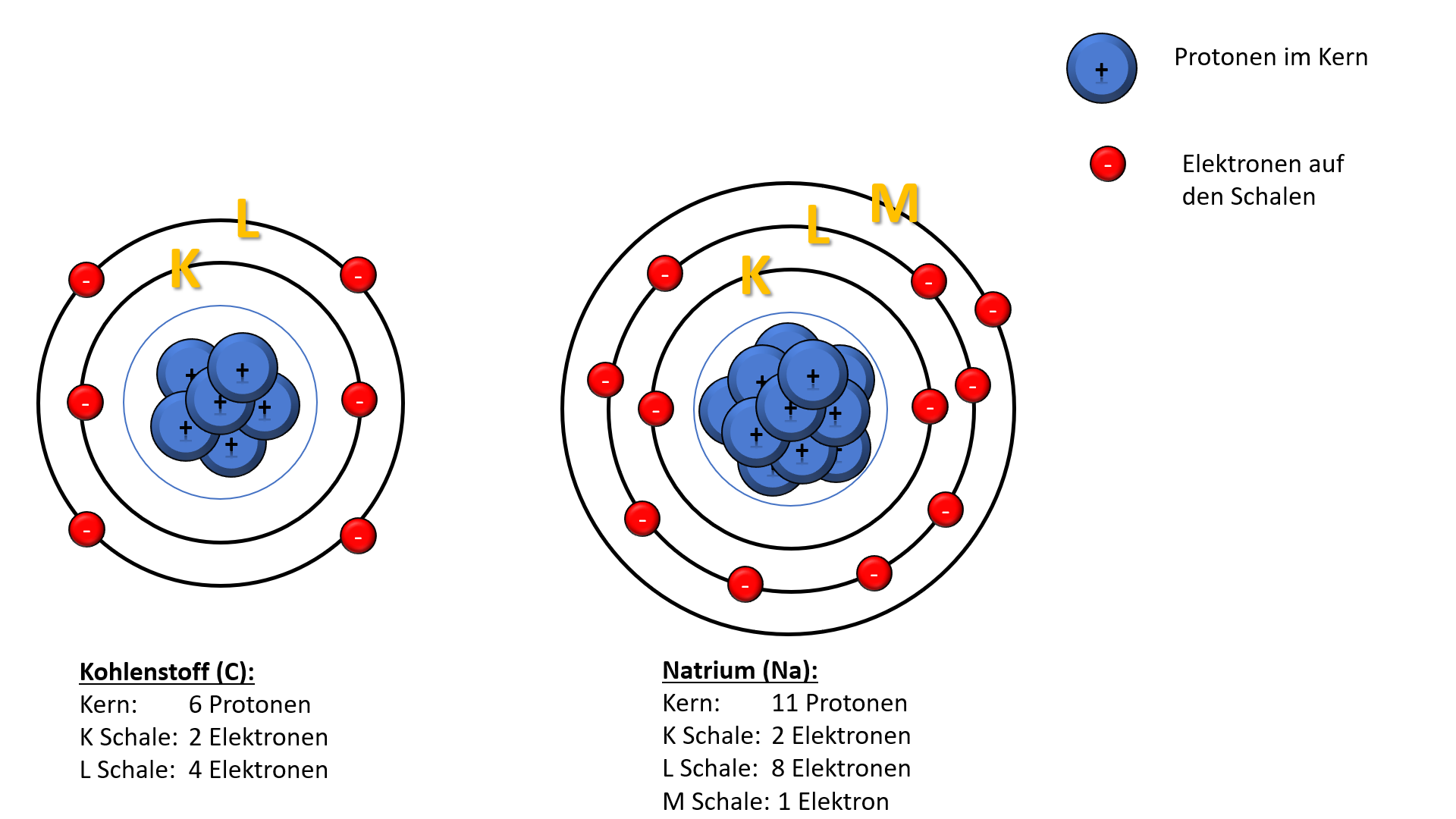
Stell dir vor, Atome sind wie kleine, super-behütete Stars. Jedes Atom hat seine eigenen Elektronen, die wie treue Bodyguards um den Kern herumschwirren. Und diese Bodyguards, die Elektronen, kleben ganz schön fest an ihrem Star, dem Atom. Aber was passiert, wenn jemand versucht, eines dieser Elektronen wegzunehmen? Genau da kommt die Ionisierungsenergie ins Spiel!
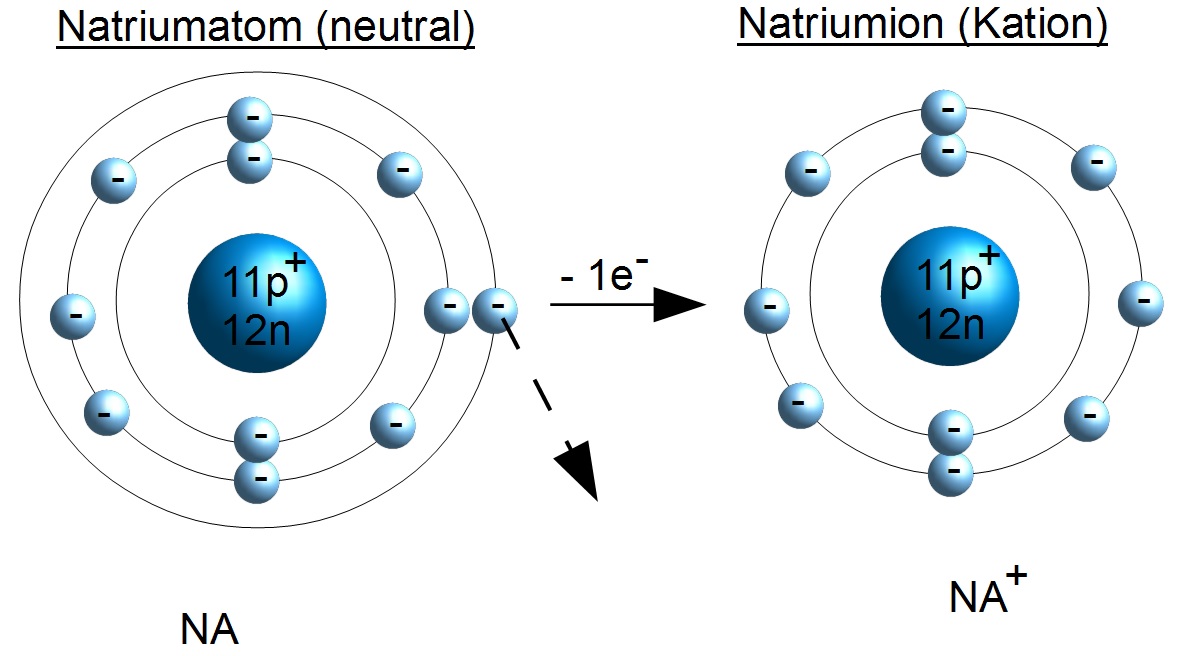
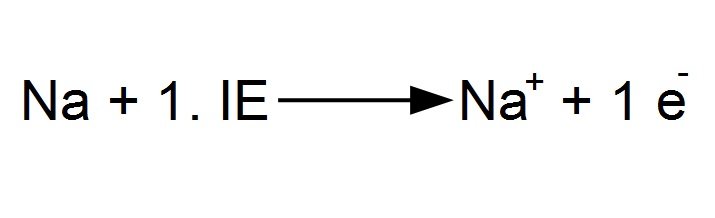
Die Ionisierungsenergie ist im Grunde die Energie, die du brauchst, um einem Atom ein Elektron zu klauen. Klingt fies, oder? Aber keine Sorge, es ist alles wissenschaftlich und passiert nur im Labor (oder in Sternen, aber dazu später mehr!). Denk an die Ionisierungsenergie wie an einen Wettbewerb. Wer die meiste Energie aufbringen kann, gewinnt das Elektron! Je stärker das Atom sein Elektron festhält, desto höher ist die Ionisierungsenergie. Es ist also eine Art Tauziehen zwischen dir und dem Atom!
Warum ist das Ganze so spannend? Weil die Ionisierungsenergie uns jede Menge über die Atome verrät. Sie ist wie ein Fenster in die Welt der chemischen Elemente. Stell dir vor, du bist ein Detektiv und die Ionisierungsenergie ist dein wichtigster Hinweis. Sie hilft dir, die Persönlichkeit der Atome zu verstehen. Sind sie eher anhänglich und halten ihre Elektronen fest? Oder sind sie großzügig und geben sie leicht her? Die Ionisierungsenergie gibt dir die Antwort!
Die Reihenfolge der Elektronenraubzüge
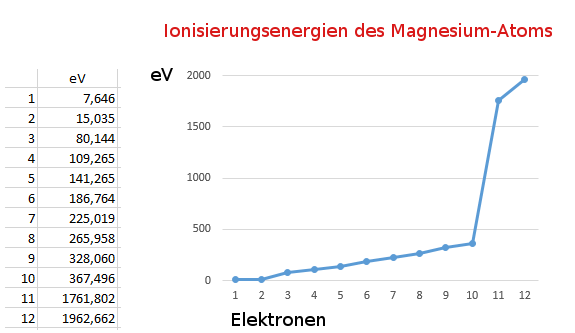
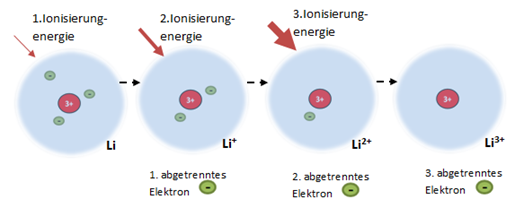
Das Tolle ist, dass du nicht nur ein Elektron klauen kannst. Du kannst es mehrmals versuchen! Die erste Ionisierungsenergie ist die Energie, die du brauchst, um das erste Elektron zu entfernen. Die zweite Ionisierungsenergie ist die Energie, die du brauchst, um das zweite Elektron zu entfernen, und so weiter. Aber Achtung: Je mehr Elektronen du klaust, desto schwieriger wird es! Das Atom wird immer wütender und hält seine verbleibenden Elektronen noch fester. Das ist wie bei einem Keksglas: Je weniger Kekse drin sind, desto besser passt man darauf auf!
Warum ist es immer schwieriger?
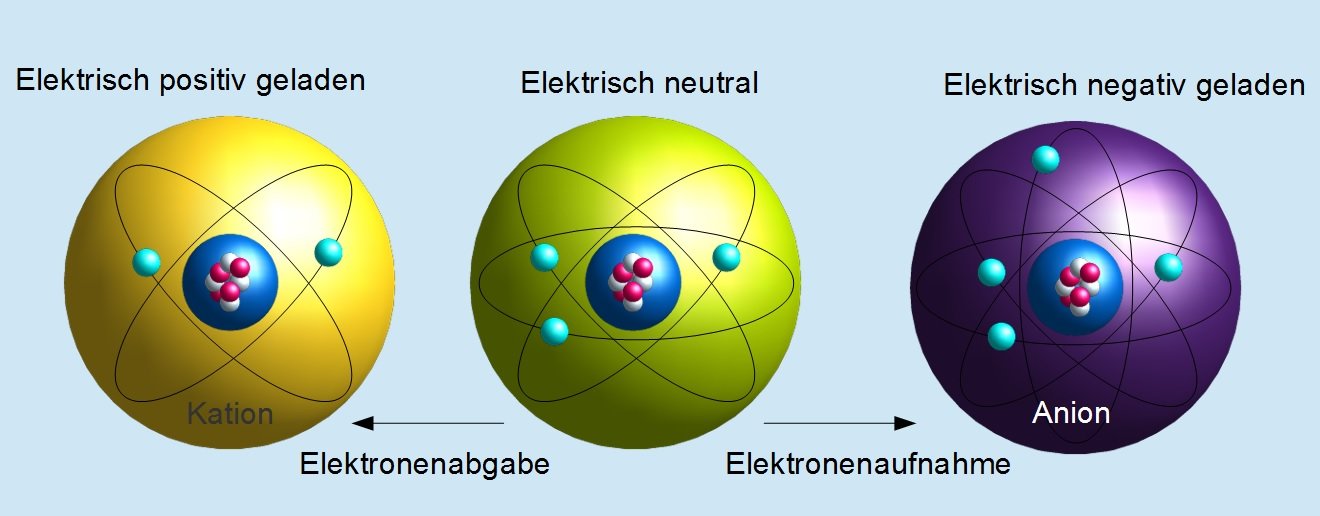
Ganz einfach: Wenn du ein Elektron entfernst, wird das Atom positiv geladen. Das bedeutet, es hat jetzt mehr positive Ladung im Kern als negative Ladung durch die Elektronen. Positive Ladungen ziehen negative Ladungen an. Deshalb ziehen die verbleibenden Elektronen noch stärker zum positiv geladenen Kern hin. Stell dir vor, du versuchst, einen Magneten von einem anderen Magneten zu trennen – je näher sie beieinander sind, desto schwieriger wird es!
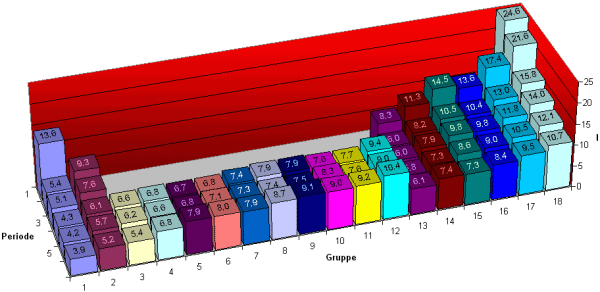
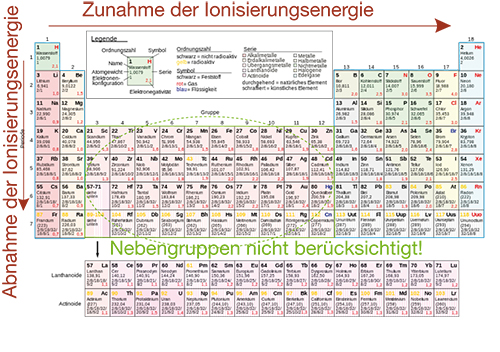
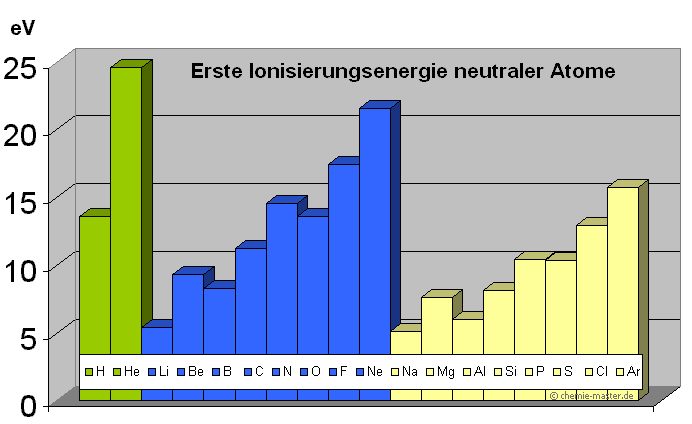
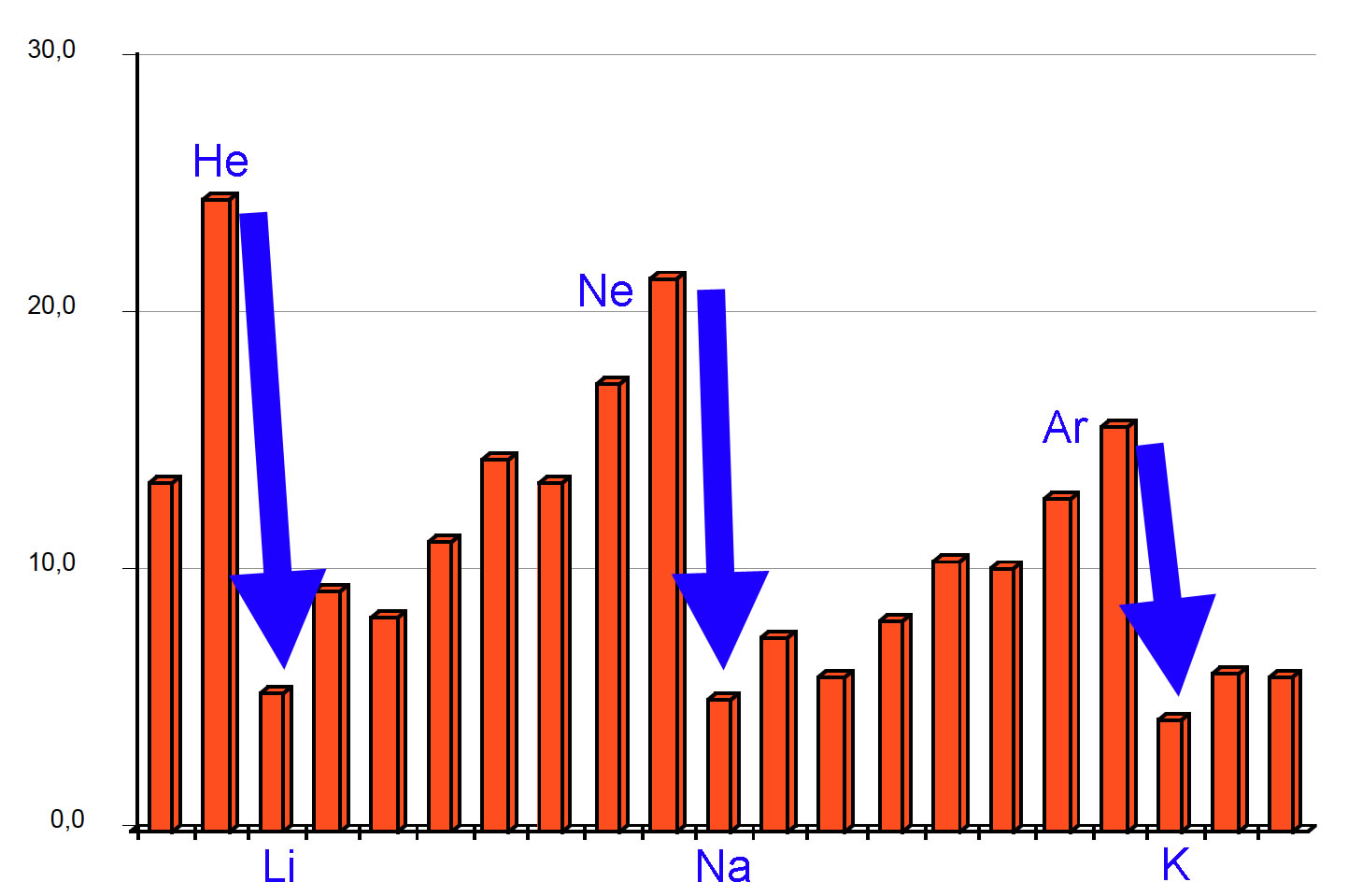
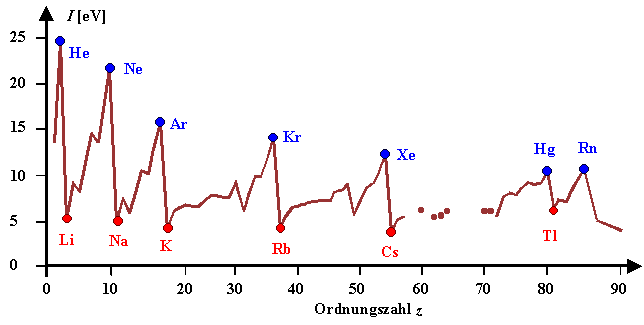
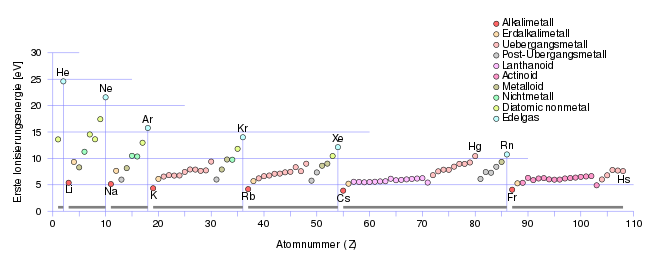
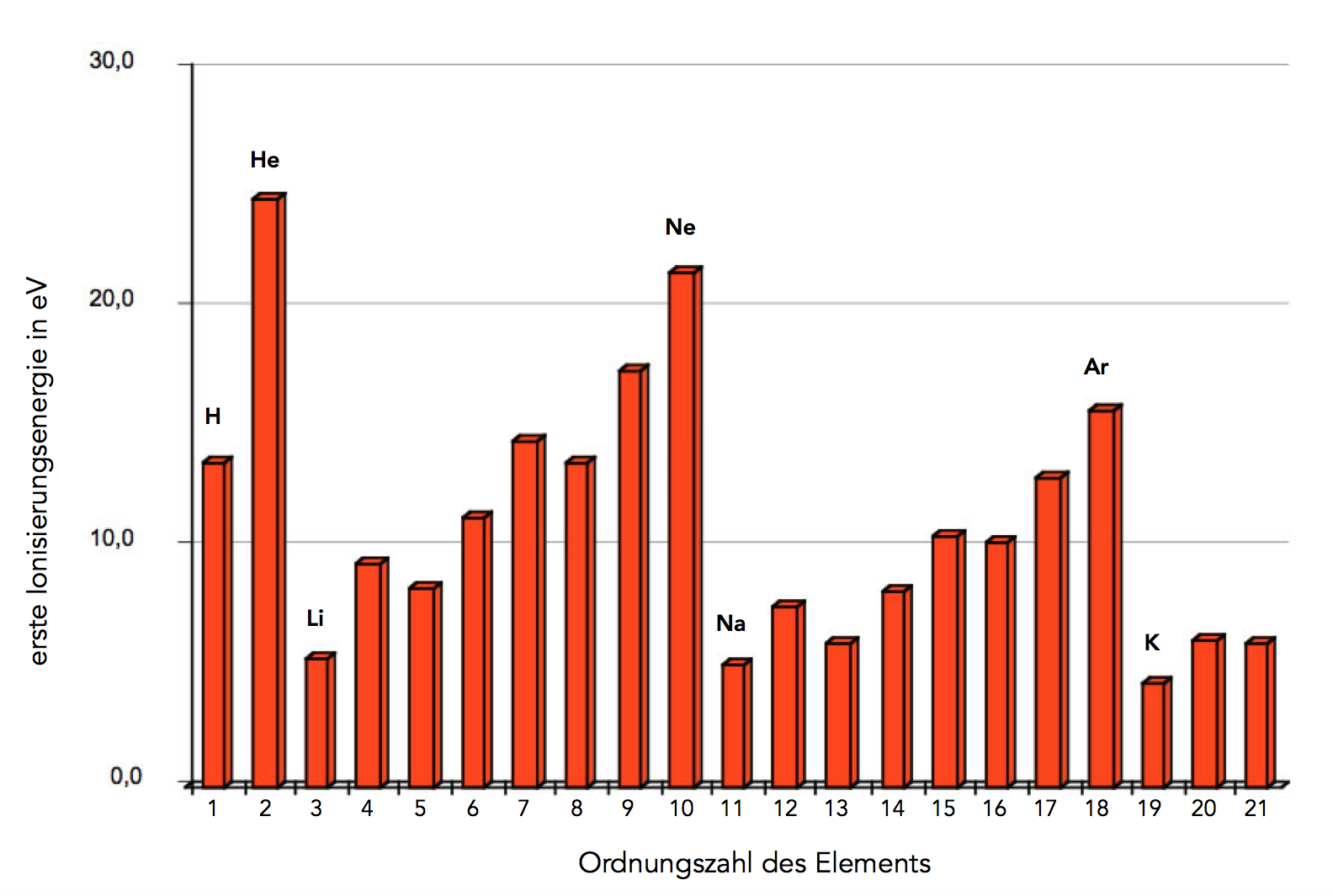
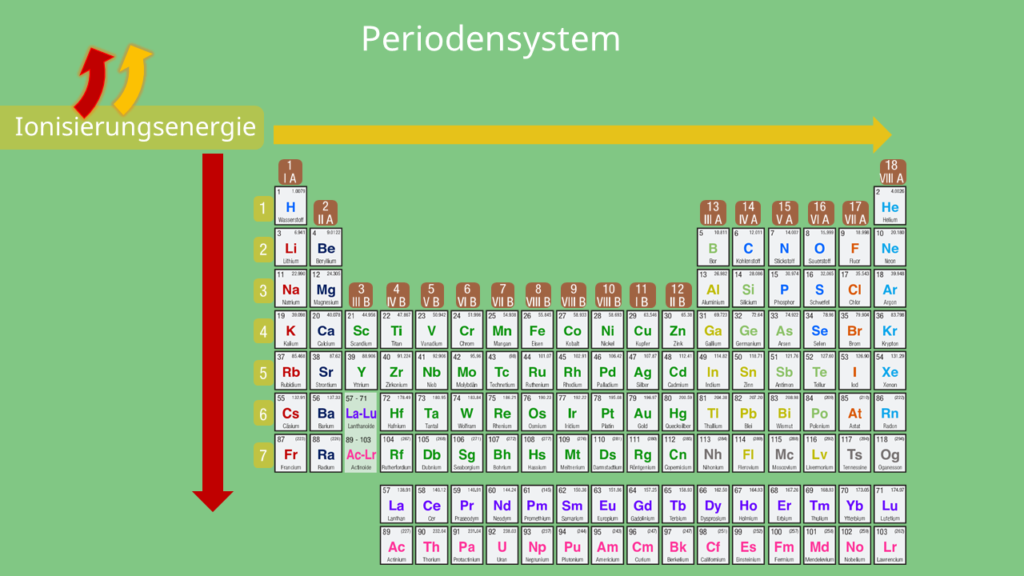
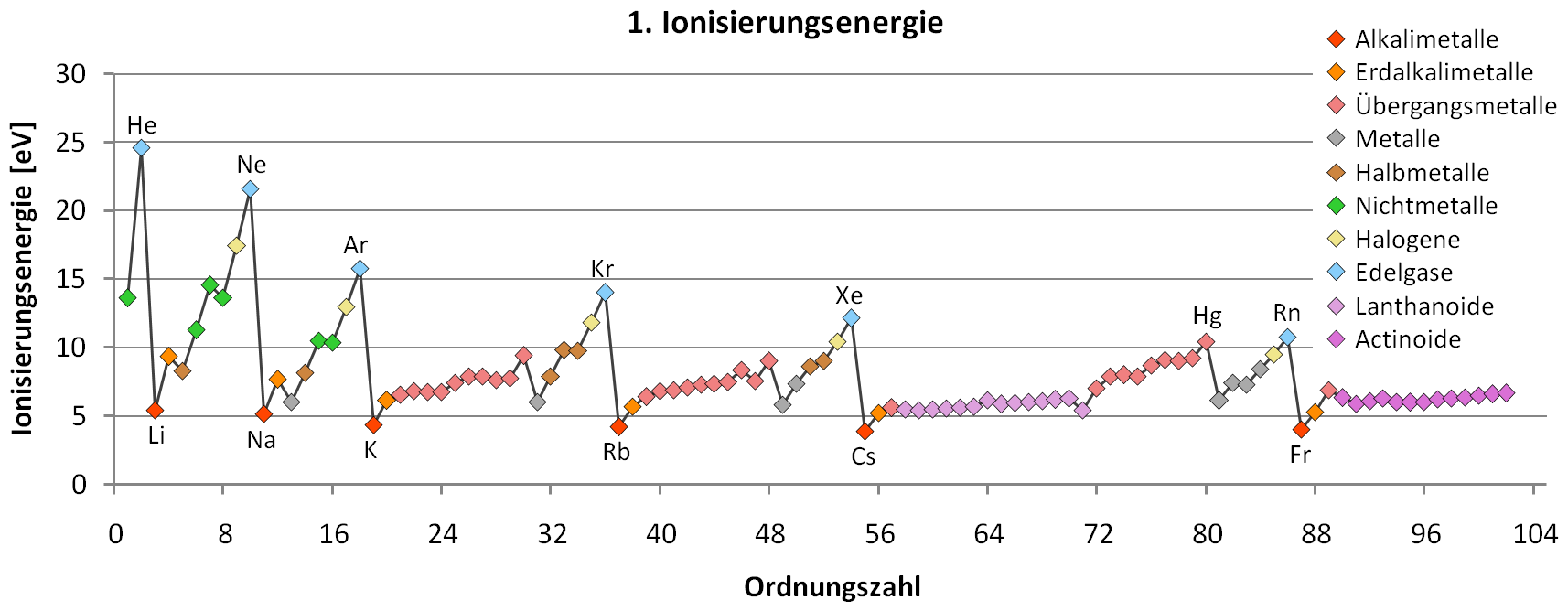
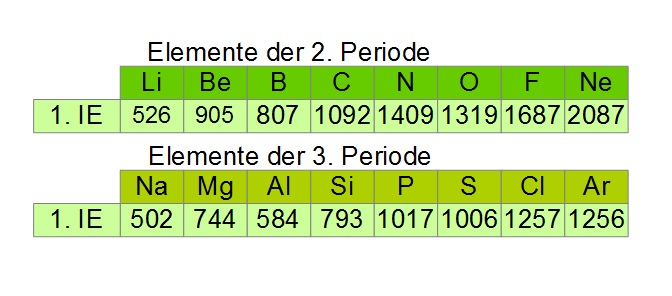
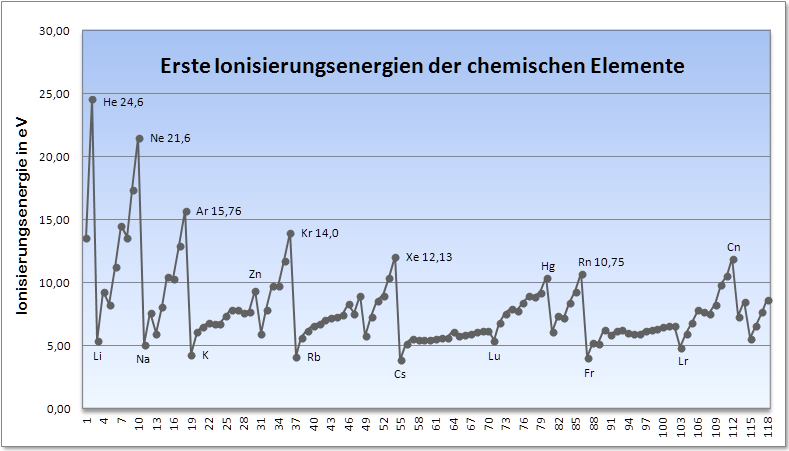
Die Ionisierungsenergie ist auch super nützlich, um das Periodensystem zu verstehen. Du weißt schon, diese große Tabelle mit all den chemischen Elementen. Die Elemente sind nach ihren Eigenschaften geordnet, und die Ionisierungsenergie spielt dabei eine wichtige Rolle. Im Allgemeinen nimmt die Ionisierungsenergie innerhalb einer Periode (einer Zeile im Periodensystem) von links nach rechts zu. Das liegt daran, dass die Atome immer kleiner werden und ihre Elektronen stärker festhalten. Innerhalb einer Gruppe (einer Spalte im Periodensystem) nimmt die Ionisierungsenergie von oben nach unten ab. Das liegt daran, dass die Elektronen weiter vom Kern entfernt sind und leichter entfernt werden können.
Also, die Ionisierungsenergie ist nicht nur eine trockene wissenschaftliche Definition. Sie ist ein Schlüssel zum Verständnis der Welt der Atome. Sie verrät uns, wie stark Atome ihre Elektronen festhalten, wie sie miteinander reagieren und wie das Periodensystem aufgebaut ist. Und das ist doch ziemlich cool, oder?
Denk mal darüber nach: Auch in Sternen spielt die Ionisierungsenergie eine große Rolle. In den extrem heißen Bedingungen im Inneren eines Sterns werden Atome ständig ionisiert, verlieren also ihre Elektronen. Das beeinflusst die Art und Weise, wie der Stern Energie erzeugt und abstrahlt. Die Farben der Sterne, die wir am Nachthimmel sehen, hängen sogar mit den Ionisierungsprozessen in ihrem Inneren zusammen! Die Ionisierungsenergie ist also nicht nur etwas für Labore, sondern auch etwas für Sternengucker!
Also, das nächste Mal, wenn du etwas über Atome und Chemie liest, denk an die Ionisierungsenergie. Denk an den Wettbewerb um die Elektronen, an die Detektivarbeit und an die Sterne. Vielleicht entdeckst du ja deine eigene Begeisterung für diese faszinierende Größe! Wer weiß, vielleicht wirst du ja der nächste Elektronen-Entdecker!
![Was Ist Die Ionisierungsenergie Ionisierungsenergie • Formel, Tabelle, Trends im PSE · [mit Video]](https://d3f6gjnauy613m.cloudfront.net/system/production/videos/001/841/c270baef7a2a1bcd25c7dd1c88b7b172c0336e9e/Ioniesierungsenergie_Thumbnail.png?1729777257)