Was Ist Ein Dipol Molekül
Herzlich willkommen in der faszinierenden Welt der Chemie, liebe Reisende und Neu-Deutschlandentdecker! Vielleicht hast du schon einmal von dem Begriff "Dipolmolekül" gehört und dich gefragt, was das eigentlich bedeutet. Keine Sorge, es ist viel einfacher zu verstehen, als es vielleicht klingt. Stell dir vor, du bist auf Entdeckungstour durch Deutschland und findest ein besonderes Souvenir – etwas, das zwei unterschiedliche Seiten hat und genau das macht ein Dipolmolekül aus!
Was ist ein Dipolmolekül überhaupt?
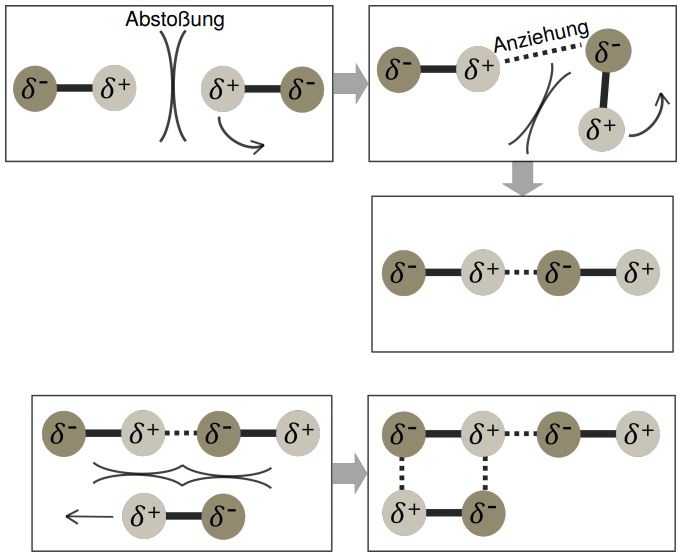
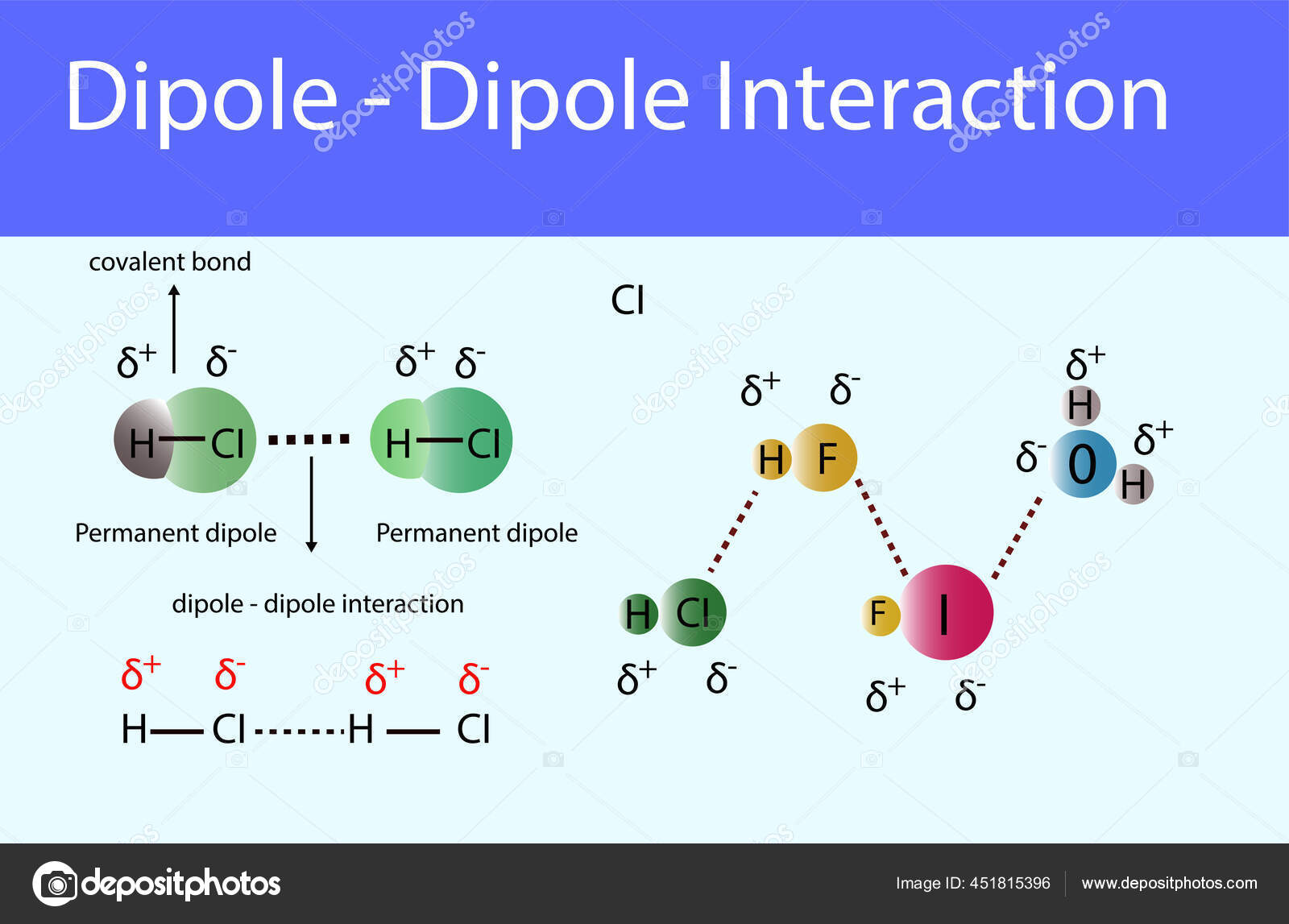
Im Grunde genommen ist ein Dipolmolekül ein Molekül, bei dem die elektrische Ladung nicht gleichmäßig verteilt ist. Das bedeutet, dass eine Seite des Moleküls eine leicht positive Ladung (δ+) trägt, während die andere Seite eine leicht negative Ladung (δ-) aufweist. Diese ungleiche Verteilung der Ladung erzeugt ein sogenanntes Dipolmoment – stell dir das wie einen kleinen Pfeil vor, der von der positiven zur negativen Seite des Moleküls zeigt.
Um das besser zu verstehen, müssen wir uns die Bausteine eines Moleküls anschauen: die Atome. Jedes Atom hat einen Kern mit positiv geladenen Protonen und eine Hülle mit negativ geladenen Elektronen. Diese Elektronen sind nicht statisch, sondern bewegen sich um den Kern herum. Wenn zwei Atome sich zu einem Molekül verbinden, teilen sie sich Elektronen, um eine stabile chemische Bindung einzugehen.
Der Clou dabei ist: Nicht alle Atome ziehen gleich stark an Elektronen. Diese Anziehungskraft wird als Elektronegativität bezeichnet. Sauerstoff (O) ist beispielsweise viel elektronegativer als Wasserstoff (H). Das bedeutet, dass Sauerstoff die Elektronen in einer Bindung stärker zu sich zieht als Wasserstoff.
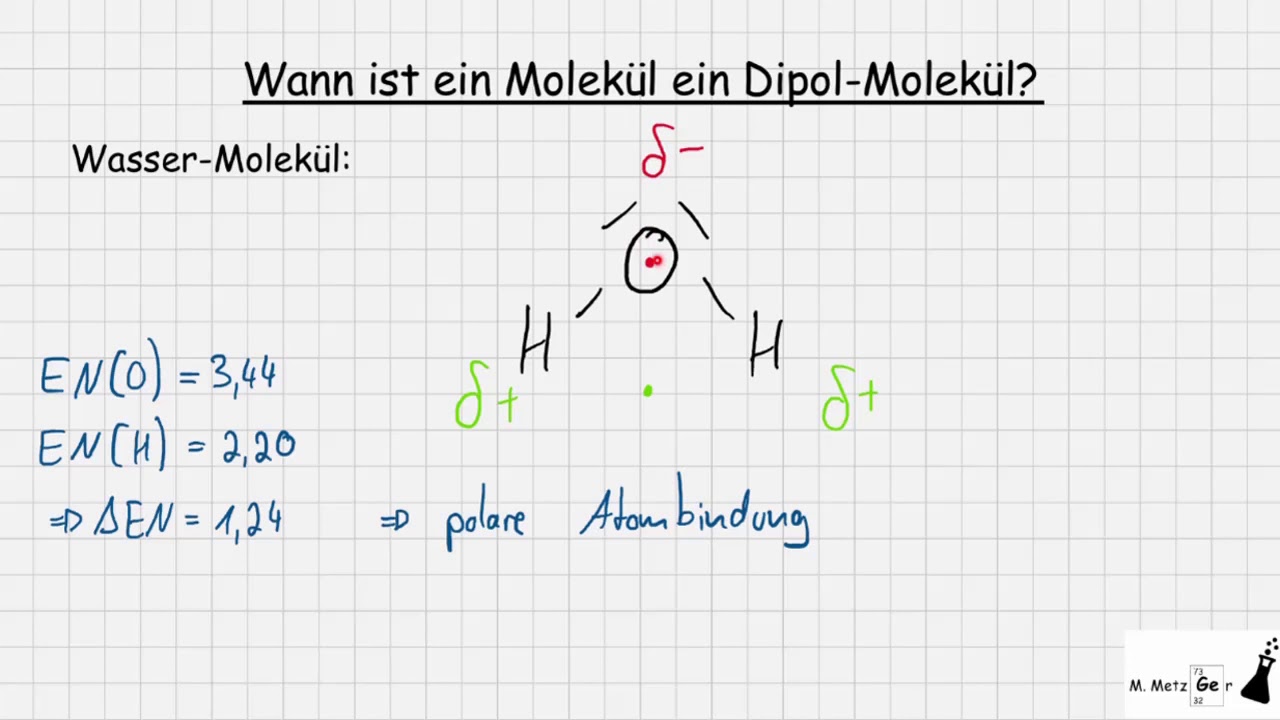
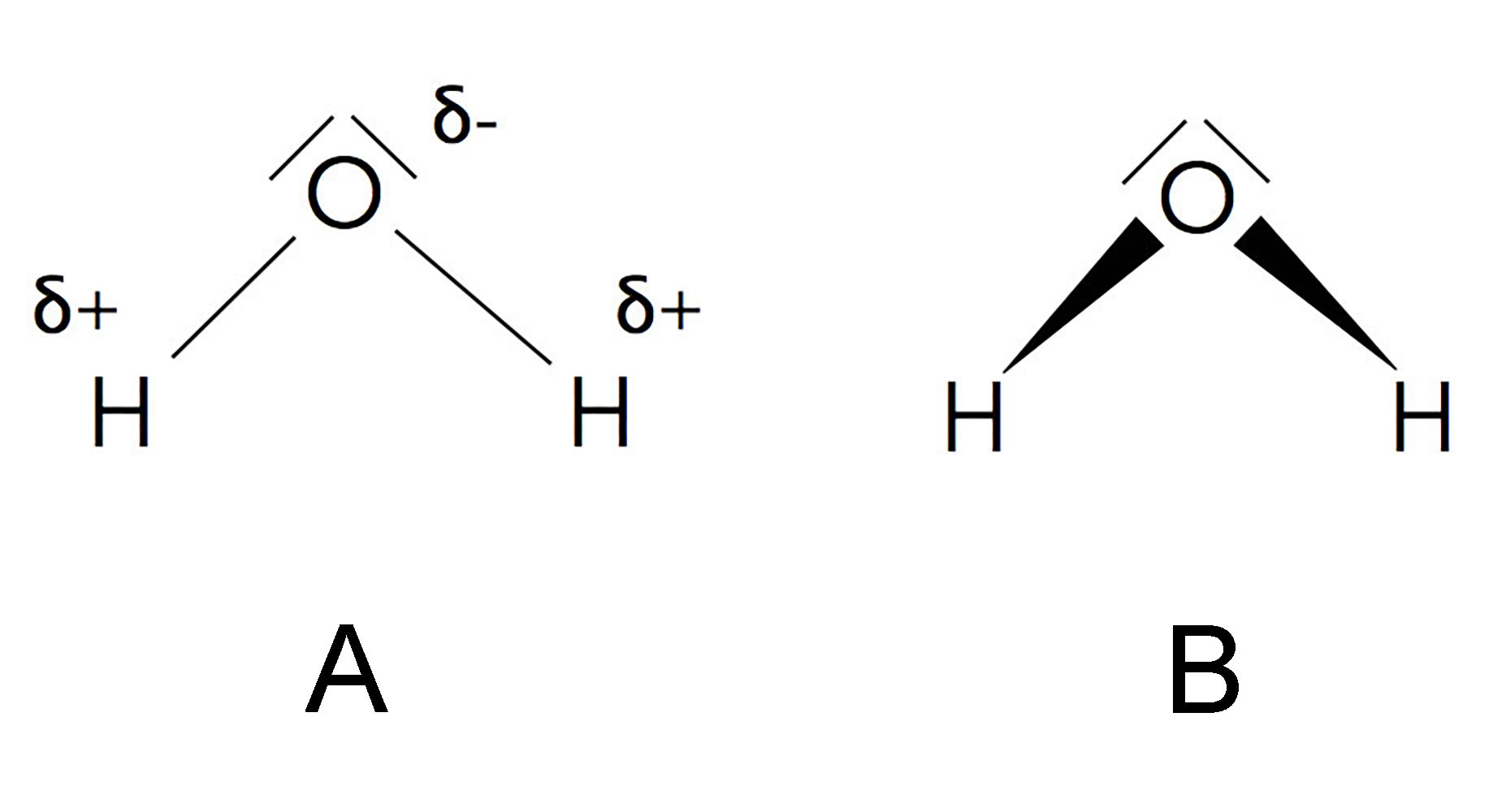
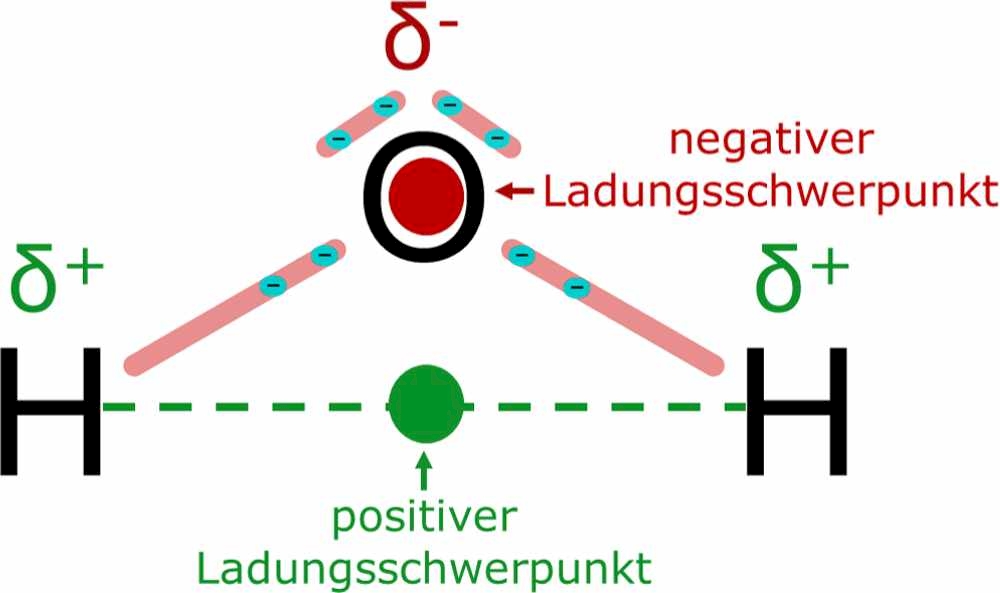
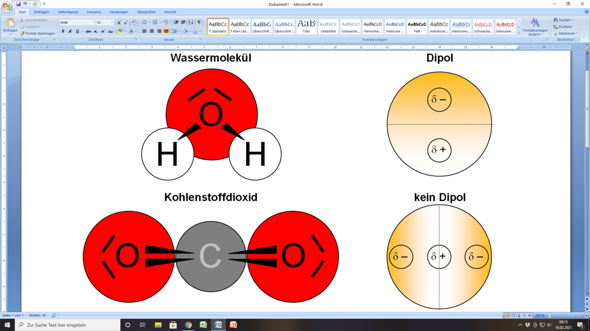
Nehmen wir als Beispiel das wohl bekannteste Dipolmolekül: Wasser (H2O). Sauerstoff ist deutlich elektronegativer als Wasserstoff. Dadurch zieht der Sauerstoff in einem Wassermolekül die Elektronen stärker an sich. Das führt dazu, dass der Sauerstoffpartial eine leicht negative Ladung (δ-) bekommt, während die beiden Wasserstoffatome jeweils eine leicht positive Ladung (δ+) erhalten. Dadurch entsteht ein Dipolmoment, das von den Wasserstoffatomen zum Sauerstoffatom zeigt. Es ist fast so, als würden die Wasserstoffatome dem Sauerstoffatom einen kleinen Elektroschub geben.
Merke dir: Ein Molekül ist ein Dipol, wenn es eine ungleiche Ladungsverteilung und somit ein Dipolmoment besitzt.
Warum sind Dipolmoleküle wichtig?
Dipolmoleküle sind nicht nur ein faszinierendes chemisches Konzept, sondern sie spielen auch eine entscheidende Rolle in vielen Bereichen unseres Lebens und der Natur. Ihre besonderen Eigenschaften beeinflussen die physikalischen und chemischen Eigenschaften von Stoffen auf vielfältige Weise:
1. Lösungsverhalten
Einer der wichtigsten Effekte von Dipolmolekülen ist ihr Einfluss auf die Löslichkeit von Stoffen. Die Regel "Ähnliches löst sich in Ähnlichem" besagt, dass polare Stoffe sich gut in polaren Lösungsmitteln lösen, während unpolare Stoffe sich gut in unpolaren Lösungsmitteln lösen. Wasser ist ein ausgezeichnetes polares Lösungsmittel, weil es selbst ein Dipolmolekül ist. Das bedeutet, dass sich viele polare Stoffe, wie zum Beispiel Zucker oder Salz, gut in Wasser lösen. Die positiven und negativen Enden der Wassermoleküle interagieren mit den geladenen Teilchen der gelösten Substanz und halten sie in Lösung. Öl hingegen ist ein unpolarer Stoff und löst sich nicht in Wasser, da es keine starken Wechselwirkungen mit den Wassermolekülen eingehen kann. Wenn du also in Deutschland bist und dir ein Glas Wasser mit Zucker bestellst, kannst du dich daran erinnern, dass die Dipole des Wassers und des Zuckers fleißig zusammenarbeiten, um eine homogene Lösung zu erzeugen!
2. Oberflächenspannung
Die Oberflächenspannung von Wasser ist ebenfalls eine Folge seiner Dipoleigenschaft. Wassermoleküle ziehen sich gegenseitig an, insbesondere an der Wasseroberfläche. Diese Anziehungskraft erzeugt eine Art "Haut" auf der Wasseroberfläche, die es kleinen Insekten ermöglicht, darauf zu laufen oder kleine Gegenstände zu tragen. Stell dir vor, du siehst einen Wasserläufer auf einem Teich in einem deutschen Park – das ist Physik in Aktion!
3. Siedepunkt
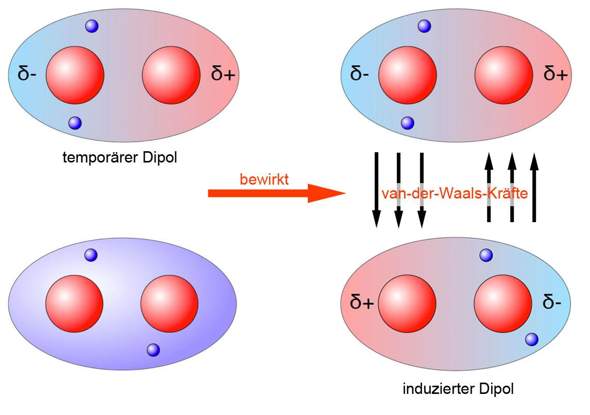
Dipolmoleküle haben in der Regel höhere Siedepunkte als unpolare Moleküle mit ähnlicher Molekülmasse. Das liegt daran, dass die Anziehungskräfte zwischen den Dipolmolekülen (Dipol-Dipol-Wechselwirkungen) stärker sind als die schwachen Van-der-Waals-Kräfte zwischen unpolaren Molekülen. Um eine Flüssigkeit zum Sieden zu bringen, muss man genügend Energie aufwenden, um diese Anziehungskräfte zu überwinden. Deshalb benötigt Wasser beispielsweise eine relativ hohe Temperatur (100°C), um zu sieden, während unpolare Stoffe wie Methan schon bei viel niedrigeren Temperaturen sieden.
4. Biologische Prozesse
Dipolmoleküle spielen eine entscheidende Rolle in vielen biologischen Prozessen. Zum Beispiel sind Proteine und DNA komplexe Moleküle, die aus vielen polaren und unpolaren Teilen bestehen. Die Wechselwirkungen zwischen diesen Teilen und mit dem umgebenden Wasser sind entscheidend für die Struktur und Funktion dieser Moleküle. Wasser ist auch essentiell für den Transport von Nährstoffen und Abfallprodukten in lebenden Organismen. Ohne die Dipoleigenschaft des Wassers gäbe es kein Leben, wie wir es kennen.
Wie erkennt man ein Dipolmolekül?
Es gibt ein paar einfache Regeln, die dir helfen können, zu erkennen, ob ein Molekül ein Dipol ist:
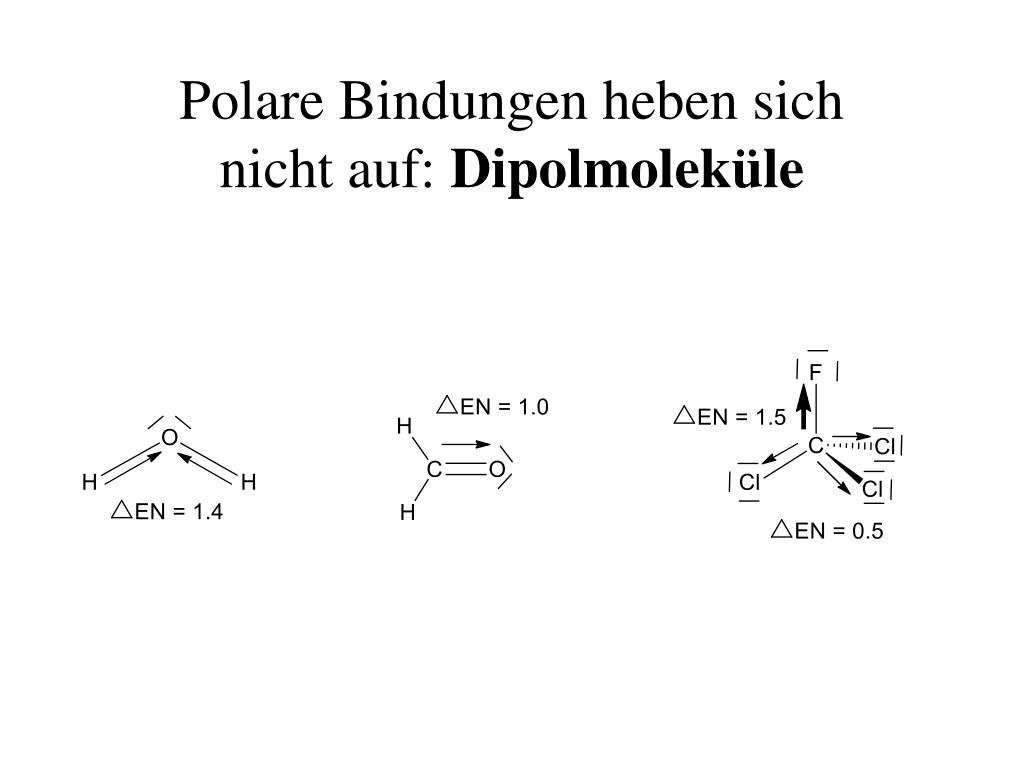
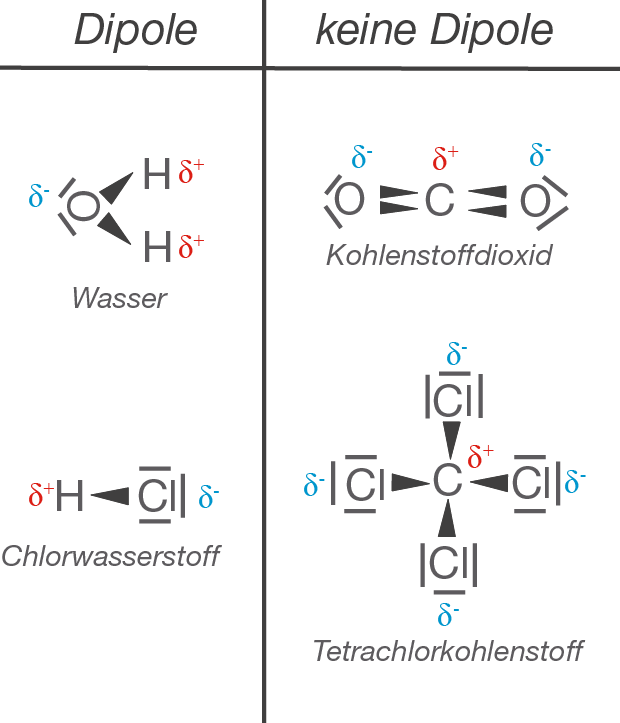
- Betrachte die Elektronegativität der Atome: Wenn die Atome, die eine Bindung eingehen, unterschiedliche Elektronegativitäten haben, ist die Bindung polar.
- Betrachte die Molekülgeometrie: Selbst wenn ein Molekül polare Bindungen enthält, kann es trotzdem unpolar sein, wenn die Bindungen symmetrisch angeordnet sind und sich die Dipolmomente gegenseitig aufheben. Beispielsweise ist Kohlenstoffdioxid (CO2) zwar polar in seinen einzelnen C=O-Bindungen, aber das Molekül ist linear und die beiden Dipolmomente zeigen in entgegengesetzte Richtungen, wodurch sie sich aufheben. Wasser hingegen ist gewinkelt und die Dipolmomente der O-H-Bindungen addieren sich zu einem resultierenden Dipolmoment.
- Experimentelle Methoden: Es gibt auch experimentelle Methoden, um das Dipolmoment eines Moleküls zu messen.
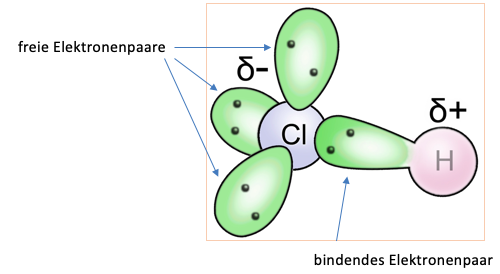
Ein Beispiel: Ammoniak (NH3) ist ein Dipolmolekül, weil Stickstoff elektronegativer als Wasserstoff ist und das Molekül eine pyramidale Geometrie hat, die verhindert, dass sich die Dipolmomente aufheben.
Dipolmoleküle im Alltag in Deutschland
Auch wenn du es vielleicht nicht merkst, begegnest du Dipolmolekülen jeden Tag, während du Deutschland erkundest. Hier sind ein paar Beispiele:
- Kochen: Wasser, das du zum Kochen von Kartoffeln oder zum Brühen von Tee verwendest, ist ein Dipolmolekül. Die Fähigkeit von Wasser, andere polare Stoffe zu lösen, ist entscheidend für die Zubereitung vieler Gerichte.
- Reinigung: Viele Reinigungsmittel enthalten polare Lösungsmittel, die helfen, Schmutz und Fett zu lösen, die oft auch polare Bestandteile enthalten.
- Kleidung: Baumwolle, ein beliebtes Material für Kleidung, besteht aus Zellulose, einem polaren Polymer. Dadurch kann Baumwolle Feuchtigkeit aufnehmen und ist angenehm zu tragen.
- Medizin: Viele Medikamente sind polare Moleküle, die sich gut in Wasser lösen und daher leicht vom Körper aufgenommen werden können.
- Bier und Wein: Alkohol (Ethanol) ist ein polares Molekül, das sowohl mit Wasser als auch mit einigen unpolaren Stoffen mischbar ist. Das trägt zum Geschmack und zur Textur von Bier und Wein bei. Und natürlich darf ein kühles Bier oder ein Glas Wein bei einem Besuch in Deutschland nicht fehlen!
Also, wenn du das nächste Mal durch die Strassen schlenderst oder ein typisch deutsches Gericht geniesst, denk daran, dass Dipolmoleküle im Hintergrund fleissig ihre Arbeit verrichten. Sie sind die unsichtbaren Helfer, die viele Prozesse in unserem Alltag ermöglichen.
Zusammenfassend lässt sich sagen: Ein Dipolmolekül ist ein Molekül mit einer ungleichen Ladungsverteilung, das ein Dipolmoment erzeugt. Diese Dipoleigenschaft beeinflusst viele physikalische und chemische Eigenschaften von Stoffen und spielt eine wichtige Rolle in unserem Leben und der Natur. Ich hoffe, diese Erklärung hat dir geholfen, das Konzept der Dipolmoleküle besser zu verstehen! Viel Spass bei deiner weiteren Entdeckungstour durch Deutschland!
Gute Reise und viel Spaß!
![Was Ist Ein Dipol Molekül Dipol • Induzierter Dipol, Dipolmoleküle, Wasser · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2023/03/WP_Wassermolekuel-als-Dipol-1024x576.jpg)
![Was Ist Ein Dipol Molekül Dipol • Induzierter Dipol, Dipolmoleküle, Wasser · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2023/03/WP_Wasser-als-Dipolmolekuel-1024x576.jpg)