Was Ist Eine Wasserstoffbrückenbindung
Hast du dich jemals gefragt, warum Wasser so seltsam ist? Es ist nicht einfach eine Flüssigkeit! Es hat einige supercoole Eigenschaften. Ein Grund dafür ist etwas namens Wasserstoffbrückenbindung. Klingt kompliziert? Keine Sorge! Es ist einfacher, als du denkst.
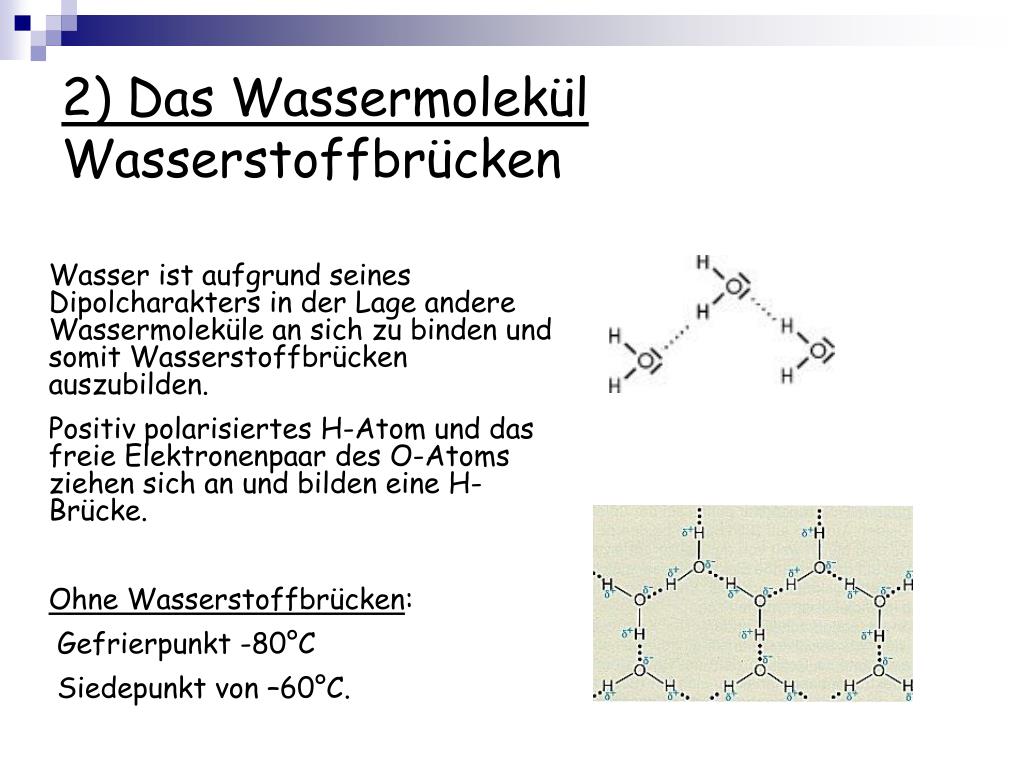
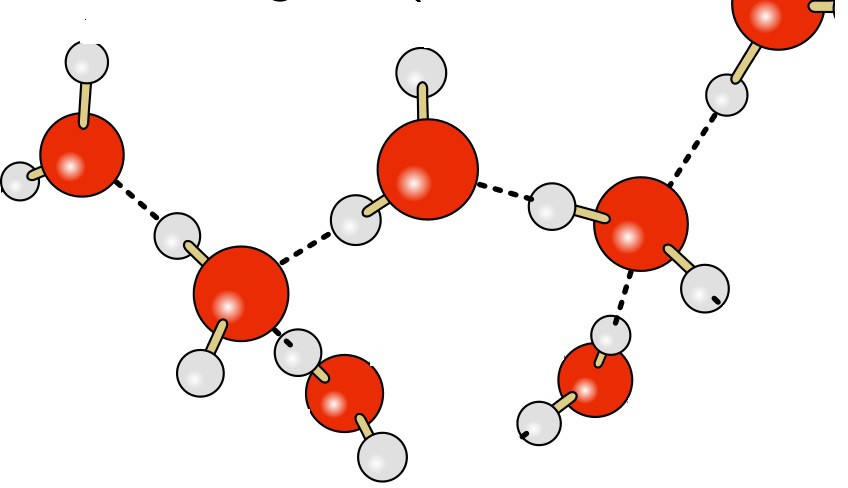
Stell dir vor, Wasser ist wie eine große Familie. Jedes Wasser-Molekül ist wie ein Familienmitglied. Und diese Familienmitglieder lieben es, Händchen zu halten. Diese "Hände" sind die Wasserstoffbrückenbindungen. Sie sind wie kleine, unsichtbare Magnete, die die Wassermoleküle zusammenhalten.
Was genau ist eine Wasserstoffbrückenbindung?
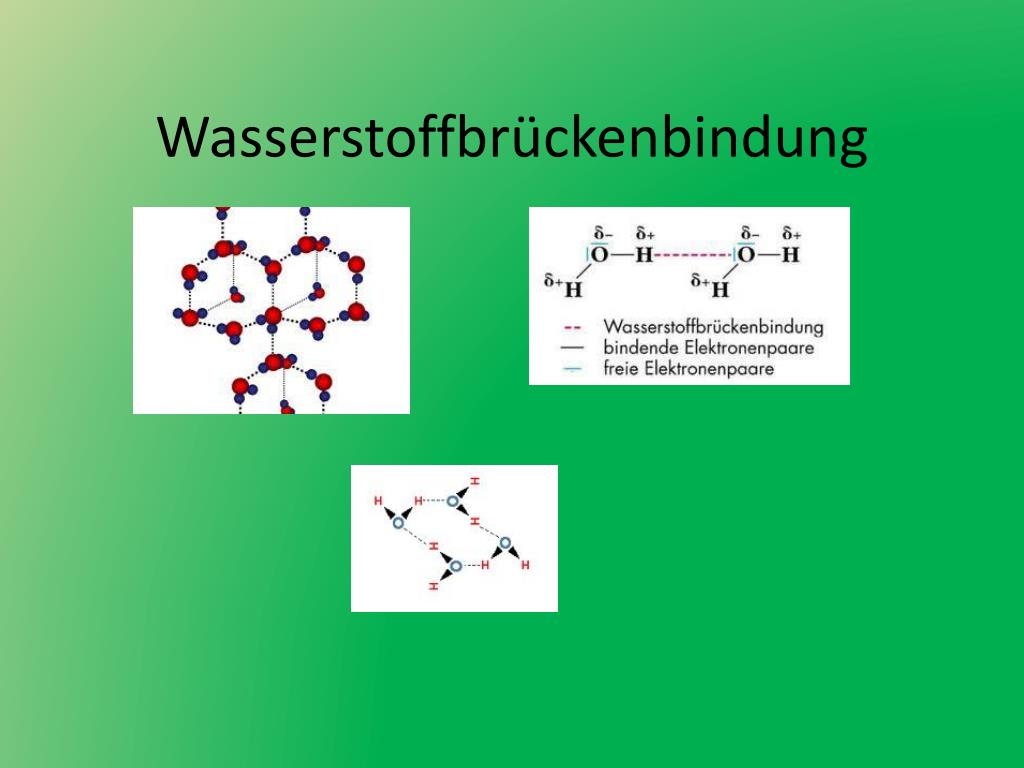
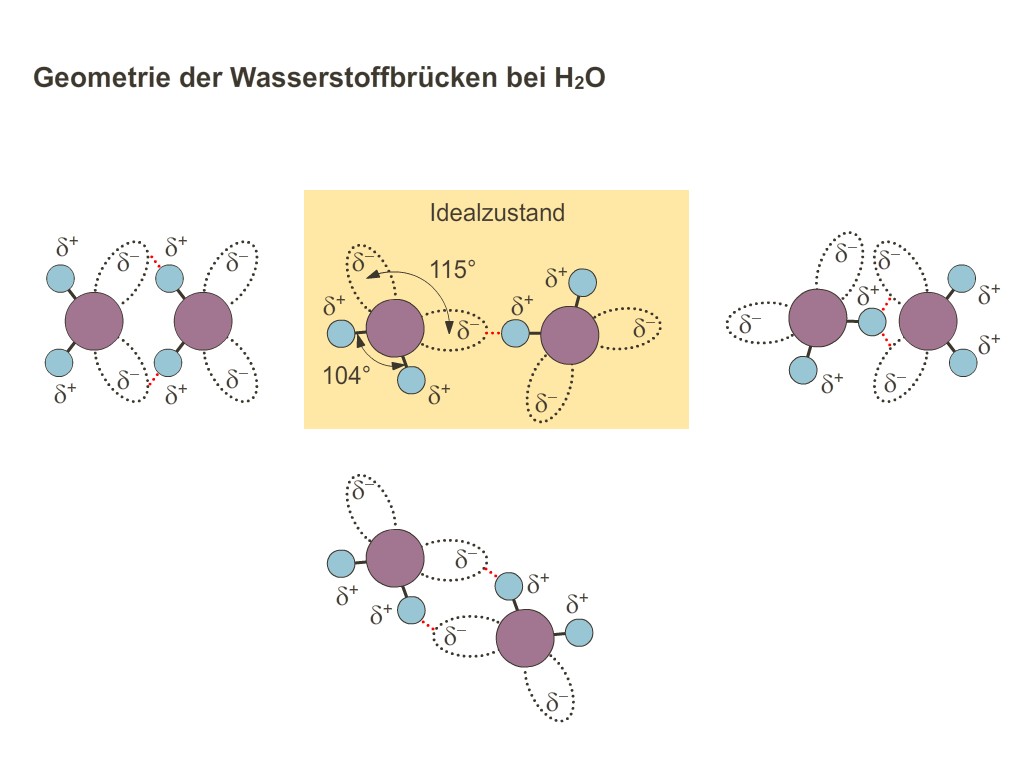
Okay, lass uns das mal runterbrechen. Ein Wassermolekül (H2O) hat ein Sauerstoffatom (O) und zwei Wasserstoffatome (H). Sauerstoff ist ein bisschen gierig nach Elektronen. Er zieht die Elektronen in der Bindung stärker zu sich als die Wasserstoffatome. Dadurch bekommt der Sauerstoff eine leicht negative Ladung (δ-), und die Wasserstoffatome bekommen eine leicht positive Ladung (δ+). Denk daran wie an winzige kleine Plus- und Minuszeichen.
Jetzt kommt der lustige Teil! Diese kleinen Ladungen sind super interessant. Der positiv geladene Wasserstoff von einem Wassermolekül fühlt sich von dem negativ geladenen Sauerstoff eines anderen Wassermoleküls angezogen. Bäm! Das ist eine Wasserstoffbrückenbindung! Es ist wie ein magnetischer Kuss zwischen den Molekülen.
Warum ist das so wichtig?
Diese Bindungen sind nicht super stark, aber es sind viele davon da! Und das macht einen riesigen Unterschied. Stell dir vor, du versuchst, ein Haus aus Legosteinen zu bauen. Ein einzelner Legostein ist nicht sehr stabil. Aber wenn du viele Legosteine zusammensteckst, bekommst du etwas Stabiles und Starkes. So ähnlich ist es mit den Wasserstoffbrückenbindungen.
Dank dieser Bindungen hat Wasser einige wirklich bemerkenswerte Eigenschaften:
- Hohe Oberflächenspannung: Das ist, warum Wasserläufer auf dem Wasser laufen können. Die Wassermoleküle an der Oberfläche halten sich so stark fest, dass sie eine Art "Haut" bilden. Super cool, oder?
- Hoher Siedepunkt: Wasser braucht viel Energie zum Kochen. Das liegt daran, dass du erst die Wasserstoffbrückenbindungen aufbrechen musst, bevor die Wassermoleküle in Dampf übergehen können.
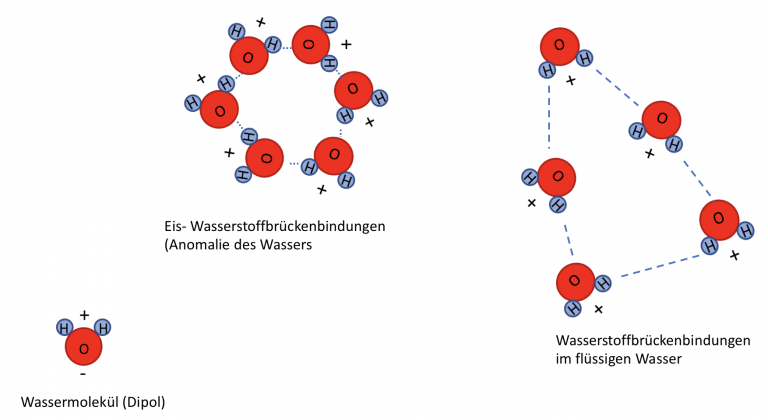
- Dichteanomalie: Eis ist leichter als Wasser. Das ist mega wichtig für das Leben im Wasser. Stell dir vor, Seen würden von unten nach oben gefrieren! Fische hätten es dann ziemlich schwer.
Wasserstoffbrückenbindungen überall!
Wasser ist nicht der einzige Ort, wo diese Bindungen eine Rolle spielen. Sie sind überall in der Natur! Zum Beispiel:
- DNA: Die Doppelhelix unserer DNA wird durch Wasserstoffbrückenbindungen zusammengehalten. Sie verbinden die beiden Stränge wie eine Leiter. Stell dir vor, diese Bindungen wären nicht da! Dann würde sich unsere DNA einfach auflösen.
- Proteine: Proteine falten sich in komplexe Strukturen. Diese Strukturen werden oft durch Wasserstoffbrückenbindungen stabilisiert. Das ist wichtig, damit Proteine ihre Arbeit richtig machen können.
Und es wird noch besser! Denk mal an deine Jeans. Baumwolle, aus der sie gemacht ist, ist ein großes Polysaccharid, eine lange Kette. Und rat mal, was die vielen Stränge in dieser Kette zusammenhält? Genau: Wasserstoffbrückenbindungen! Also, auch wenn du nicht darüber nachdenkst, wenn du deine Lieblingsjeans trägst, sind Wasserstoffbrücken am Werk!
Okay, zugegeben, Wasserstoffbrückenbindungen sind keine Liebesgeschichte im eigentlichen Sinne. Es ist eher wie eine starke, aber nicht immer dauerhafte Anziehungskraft. Aber das macht sie ja so interessant. Es ist wie ein Tanz zwischen Molekülen, der das Leben, wie wir es kennen, erst möglich macht.
Die Chemie der Wasserstoffbrückenbindungen ist also nicht nur ein trockener Fakt, den man in der Schule lernt. Sie ist überall um uns herum, beeinflusst unser Leben und die Welt, in der wir leben. Und, ganz ehrlich, ist das nicht unglaublich faszinierend?
Also, das nächste Mal, wenn du ein Glas Wasser trinkst oder einen Eiswürfel in dein Getränk gibst, denk an die kleinen Wasserstoffbrückenbindungen. Sie sind die unbesungenen Helden der Chemie!
„Ich glaube, dass die Wissenschaft die Grundlage für das Verständnis der Welt ist und dass es wichtig ist, dass die Menschen ein grundlegendes Verständnis für sie haben.“ - Linus Pauling
Und wer weiß? Vielleicht inspiriert dich dieses kleine Abenteuer in die Welt der Moleküle ja dazu, selbst tiefer in die Geheimnisse der Chemie einzutauchen. Es gibt noch so viel zu entdecken!
![Was Ist Eine Wasserstoffbrückenbindung Wasserstoffbrückenbindung • einfach erklärt · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2019/12/Wasserstoffbrückenbindung_WP_1-1024x576.jpg)


![Was Ist Eine Wasserstoffbrückenbindung Wasserstoffbrückenbindung: Chemische Bindung, Struktur · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2019/12/Wasserstoffbrückenbindung_WP_4_struktur-1024x576.jpg)


![Was Ist Eine Wasserstoffbrückenbindung Wasserstoffbrückenbindung: Chemische Bindung, Struktur · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2019/12/Wasserstoffbrückenbindung_WP_3_dna-1024x576.jpg)
![Was Ist Eine Wasserstoffbrückenbindung Wasserstoffbrückenbindung: Chemische Bindung, Struktur · [mit Video]](https://d3f6gjnauy613m.cloudfront.net/system/production/videos/001/668/b12b7511b7402ae54fa6fbcbe435928e5aab8b16/Wasserstoffbrückenbindung_Thumbnail.png?1639048257)



![Was Ist Eine Wasserstoffbrückenbindung Wasserstoffbrückenbindung • einfach erklärt · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2019/12/Wasserstoffbrückenbindung_WP_2_kohäsion-1024x576.jpg)