Was Sind Säuren Und Basen

Wenn Sie neu in Deutschland sind oder einfach nur Ihr Wissen über grundlegende wissenschaftliche Konzepte auffrischen möchten, ist es wichtig, ein Verständnis von Säuren und Basen zu haben. Diese Substanzen sind allgegenwärtig in unserem Alltag, von Lebensmitteln, die wir essen, bis hin zu Reinigungsmitteln, die wir verwenden. Dieser Artikel bietet eine klare und prägnante Erklärung von Säuren und Basen, ihre Eigenschaften und ihre Bedeutung.
Was sind Säuren?
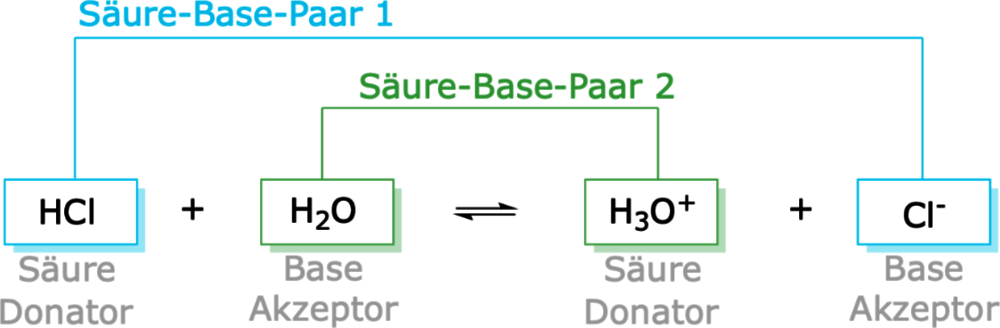
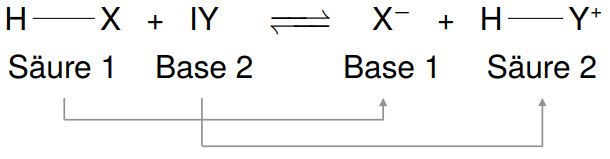
Eine Säure ist eine Substanz, die in der Lage ist, ein Proton (H+ Ion) abzugeben oder ein Elektronenpaar zu akzeptieren. Einfacher ausgedrückt: Säuren erhöhen die Konzentration von Wasserstoffionen (H+) in einer wässrigen Lösung. Die Stärke einer Säure wird durch ihren pH-Wert gemessen. Ein pH-Wert kleiner als 7 kennzeichnet eine saure Lösung. Je niedriger der pH-Wert, desto stärker die Säure.
Eigenschaften von Säuren
- Saurer Geschmack: Viele Säuren haben einen sauren Geschmack (obwohl es niemals sicher ist, Chemikalien zu schmecken, um sie zu identifizieren!). Denken Sie an den Geschmack von Zitronensaft (Zitronensäure) oder Essig (Essigsäure).
- Reaktion mit Metallen: Säuren reagieren mit einigen Metallen und setzen dabei Wasserstoffgas (H2) frei. Diese Reaktion kann zu Korrosion führen.
- Ätzend: Starke Säuren sind ätzend und können Haut, Gewebe und viele Materialien beschädigen oder zerstören.
- Leitfähig: Säuren lösen sich in Wasser und bilden Ionen, wodurch sie elektrische Leitfähigkeit ermöglichen.
- Färben Indikatoren rot: Säuren färben bestimmte chemische Indikatoren rot. Ein bekanntes Beispiel ist Lackmuspapier, das sich in Gegenwart einer Säure rot färbt.
Beispiele für Säuren
- Salzsäure (HCl): Eine starke Säure, die im Magensaft zur Verdauung von Nahrungsmitteln vorkommt und in der Industrie vielfältig eingesetzt wird.
- Schwefelsäure (H2SO4): Eine der am häufigsten verwendeten Industriechemikalien, eingesetzt in Batterien, Düngemitteln und vielen anderen Prozessen.
- Essigsäure (CH3COOH): Der Hauptbestandteil von Essig, verwendet zum Würzen von Speisen und als Konservierungsmittel.
- Zitronensäure (C6H8O7): In vielen Früchten, insbesondere Zitrusfrüchten, enthalten, verleiht sie einen sauren Geschmack und wird als Konservierungsmittel eingesetzt.
- Kohlensäure (H2CO3): Entsteht, wenn Kohlendioxid sich in Wasser löst, beispielsweise in kohlensäurehaltigen Getränken.
Was sind Basen?
Eine Base ist eine Substanz, die in der Lage ist, ein Proton (H+ Ion) aufzunehmen oder ein Hydroxidion (OH-) freizusetzen. Basen verringern die Konzentration von Wasserstoffionen (H+) in einer wässrigen Lösung. Die Stärke einer Base wird ebenfalls durch den pH-Wert gemessen. Ein pH-Wert größer als 7 kennzeichnet eine basische (oder alkalische) Lösung. Je höher der pH-Wert, desto stärker die Base.
Eigenschaften von Basen
- Bitterer Geschmack: Viele Basen haben einen bitteren Geschmack (auch hier gilt: niemals Chemikalien schmecken!).
- Seifiges Gefühl: Basen fühlen sich oft seifig oder schlüpfrig an.
- Ätzend: Starke Basen sind ebenfalls ätzend und können Haut, Gewebe und viele Materialien beschädigen oder zerstören.
- Leitfähig: Wie Säuren lösen sich Basen in Wasser und bilden Ionen, wodurch sie elektrische Leitfähigkeit ermöglichen.
- Färben Indikatoren blau: Basen färben bestimmte chemische Indikatoren blau. Lackmuspapier färbt sich in Gegenwart einer Base blau.
Beispiele für Basen
- Natriumhydroxid (NaOH): Auch bekannt als Ätznatron, wird in der Seifenherstellung, Papierherstellung und vielen anderen industriellen Prozessen verwendet.
- Kaliumhydroxid (KOH): Auch bekannt als Ätzkali, wird in der Herstellung von Flüssigseifen und Batterien verwendet.
- Ammoniak (NH3): Ein Gas mit stechendem Geruch, das in Reinigungsmitteln und Düngemitteln verwendet wird. In Wasser gelöst bildet es eine schwache Base.
- Calciumhydroxid (Ca(OH)2): Auch bekannt als gelöschter Kalk, wird im Bauwesen (z.B. als Bestandteil von Mörtel) und in der Landwirtschaft zur Bodenverbesserung verwendet.
- Magnesiumhydroxid (Mg(OH)2): In Antazida enthalten, um Magensäure zu neutralisieren.
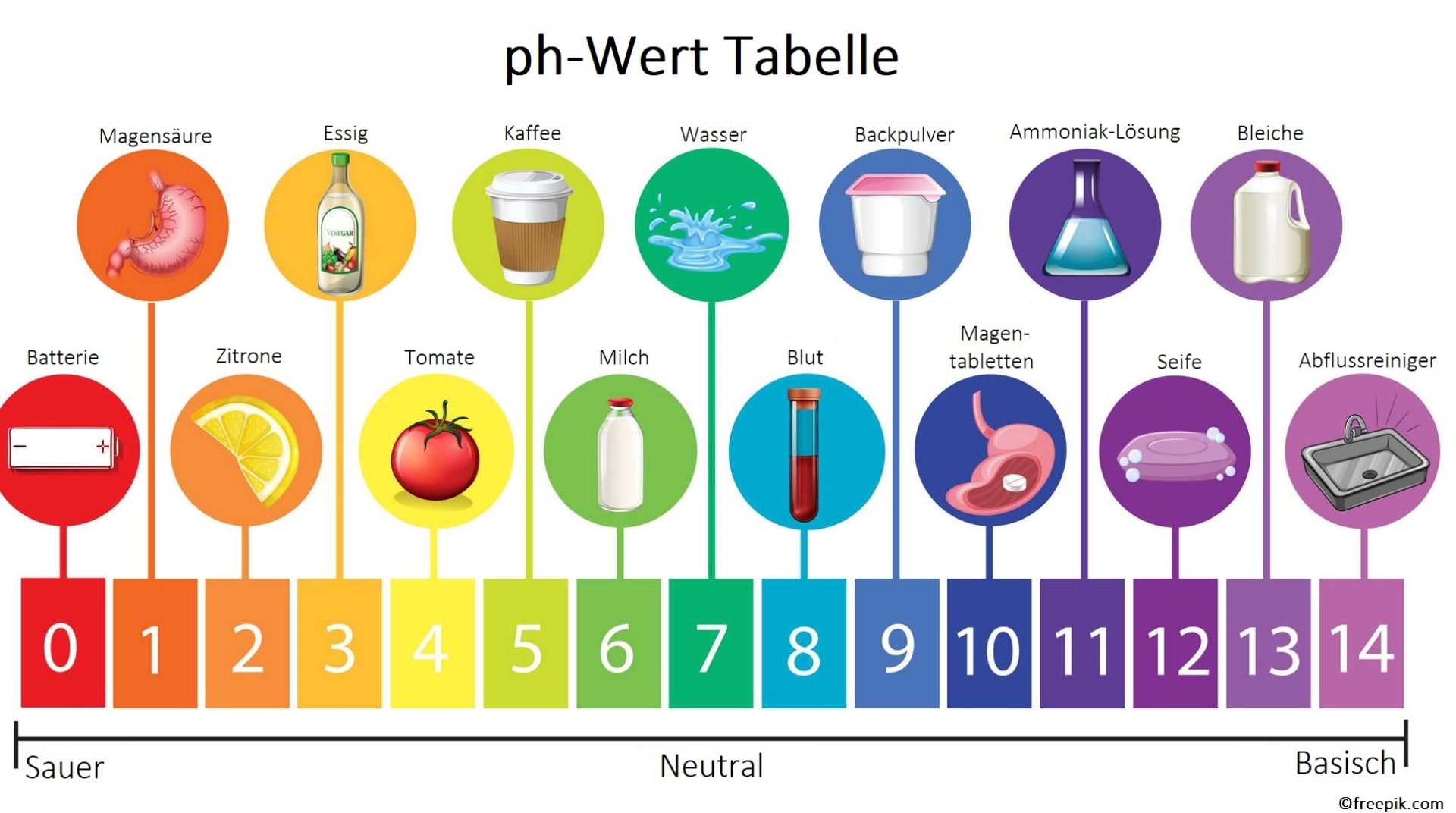
Der pH-Wert
Der pH-Wert ist eine Maßeinheit für die Acidität oder Alkalinität einer Lösung. Er reicht von 0 bis 14. Ein pH-Wert von 7 ist neutral (weder sauer noch basisch), beispielsweise reines Wasser. Werte unter 7 sind sauer, Werte über 7 sind basisch.
Wichtig: Der pH-Wert ist logarithmisch. Das bedeutet, dass eine Lösung mit einem pH-Wert von 3 zehnmal saurer ist als eine Lösung mit einem pH-Wert von 4 und hundertmal saurer als eine Lösung mit einem pH-Wert von 5.
Der pH-Wert kann mit verschiedenen Methoden gemessen werden, darunter pH-Papier (Indikatorpapier), pH-Meter und Indikatorlösungen. In Deutschland finden Sie pH-Papier und einfache pH-Meter in Apotheken (Apotheken) und Baumärkten (Baumärkten).
Neutralisation
Die Reaktion zwischen einer Säure und einer Base wird als Neutralisation bezeichnet. Bei dieser Reaktion reagieren die H+-Ionen der Säure mit den OH--Ionen der Base, um Wasser (H2O) und ein Salz zu bilden. Ein Salz ist eine ionische Verbindung, die aus der Reaktion einer Säure mit einer Base entsteht. Ein Beispiel ist die Reaktion von Salzsäure (HCl) mit Natriumhydroxid (NaOH), die Natriumchlorid (NaCl), also Kochsalz, und Wasser erzeugt:
HCl + NaOH → NaCl + H2O
Die Neutralisation ist ein wichtiger Prozess in vielen Anwendungen, wie z. B. die Behandlung von Abwasser, die Regulierung des pH-Werts im Boden und die Neutralisierung von Magensäure mit Antazida.
Sicherheitsvorkehrungen im Umgang mit Säuren und Basen
Sowohl Säuren als auch Basen können gefährlich sein, insbesondere in konzentrierter Form. Es ist wichtig, beim Umgang mit diesen Substanzen Vorsicht walten zu lassen und geeignete Sicherheitsmaßnahmen zu treffen:
- Schutzkleidung: Tragen Sie immer eine Schutzbrille und Handschuhe, um Haut- und Augenkontakt zu vermeiden.
- Belüftung: Arbeiten Sie in einem gut belüfteten Bereich, um das Einatmen von Dämpfen zu vermeiden.
- Verdünnung: Verdünnen Sie Säuren und Basen immer langsam und vorsichtig, indem Sie die Säure oder Base in das Wasser gießen (niemals umgekehrt!). Dies verhindert, dass die Lösung spritzt und gefährliche Wärme erzeugt.
- Lagerung: Lagern Sie Säuren und Basen getrennt voneinander und von anderen Chemikalien. Verwenden Sie geeignete Behälter und kennzeichnen Sie diese deutlich.
- Notfallmaßnahmen: Im Falle eines Unfalls spülen Sie die betroffene Stelle sofort mit viel Wasser. Suchen Sie bei Bedarf ärztliche Hilfe auf. Die Notrufnummer in Deutschland ist 112.
Das Verständnis von Säuren und Basen ist nicht nur für naturwissenschaftliche Disziplinen von Bedeutung, sondern auch für den Alltag. Von der Zubereitung von Speisen über die Reinigung des Haushalts bis hin zur Wartung Ihres Autos - Kenntnisse über diese Substanzen können Ihnen helfen, fundierte Entscheidungen zu treffen und sicher mit Chemikalien umzugehen. Wenn Sie weitere Fragen haben, zögern Sie nicht, sich an Experten in Apotheken oder Fachgeschäften zu wenden.

![Was Sind Säuren Und Basen Basen • Definition und Erklärung · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2023/04/WP_BasenUe_Basen-als-Protonenakzeptoren-1024x576.png)

![Was Sind Säuren Und Basen Basen • Definition und Erklärung · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2023/04/WP_BasenUe_Lewis-Base-1024x576.png)