Wie Stellt Man Reaktionsgleichungen Auf
Die Chemie, oft als die Wissenschaft der Stoffe und ihrer Veränderungen bezeichnet, bedient sich einer präzisen Sprache, um diese Veränderungen zu beschreiben: die Reaktionsgleichung. Sie ist weit mehr als nur eine formale Notation; sie ist ein Fenster in die Welt der Moleküle, eine Landkarte, die uns durch die Landschaft der chemischen Umwandlungen führt. Das Aufstellen von Reaktionsgleichungen ist eine grundlegende Fähigkeit für jeden, der sich mit Chemie beschäftigt, sei es im Labor, im Klassenzimmer oder im Alltag. Es erfordert ein Verständnis der beteiligten Stoffe, ihrer Eigenschaften und der Art und Weise, wie sie miteinander reagieren.
Warum Reaktionsgleichungen wichtig sind
Reaktionsgleichungen dienen mehreren wichtigen Zwecken:
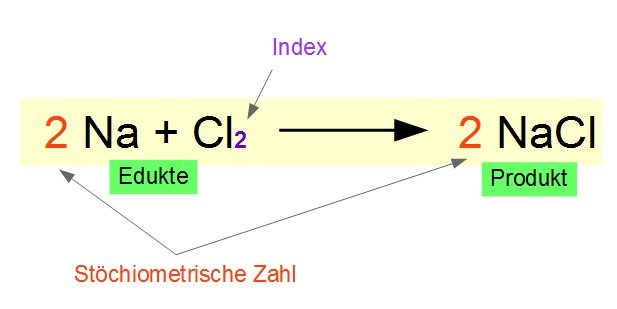
- Qualitative Beschreibung: Sie zeigen uns, welche Stoffe miteinander reagieren (Edukte oder Reaktanten) und welche Stoffe dabei entstehen (Produkte).
- Quantitative Beschreibung: Sie geben die stöchiometrischen Verhältnisse an, d.h. die Mengenverhältnisse, in denen die Stoffe miteinander reagieren. Dies ist entscheidend für Berechnungen in der Chemie, z.B. um die Ausbeute einer Reaktion vorherzusagen oder um die benötigten Mengen an Reaktanten zu bestimmen.
- Information über den Zustand: Sie können Informationen über den Aggregatzustand der Stoffe (fest, flüssig, gasförmig, gelöst) sowie über Reaktionsbedingungen (Temperatur, Druck, Katalysatoren) enthalten.
Eine korrekte Reaktionsgleichung ist somit eine vollständige und präzise Darstellung einer chemischen Reaktion. Sie ermöglicht es uns, die Reaktion zu verstehen, vorherzusagen und zu kontrollieren.
Schritt-für-Schritt-Anleitung zum Aufstellen von Reaktionsgleichungen
Der Prozess des Aufstellens einer Reaktionsgleichung lässt sich in mehrere Schritte unterteilen:
1. Identifizierung der Edukte und Produkte
Der erste Schritt besteht darin, die Edukte (Reaktanten) und die Produkte der Reaktion zu identifizieren. Diese Information kann aus einer Aufgabenstellung, einer Versuchsbeschreibung oder einer Beobachtung stammen. Es ist wichtig, die chemischen Formeln der beteiligten Stoffe korrekt zu kennen. Fehler in den Formeln führen unweigerlich zu einer falschen Reaktionsgleichung.
Beispiel: Eisen reagiert mit Sauerstoff zu Eisen(III)-oxid (Rost). Hier sind Eisen und Sauerstoff die Edukte, und Eisen(III)-oxid ist das Produkt.
2. Aufstellen der unausgeglichenen Gleichung (Skelettgleichung)
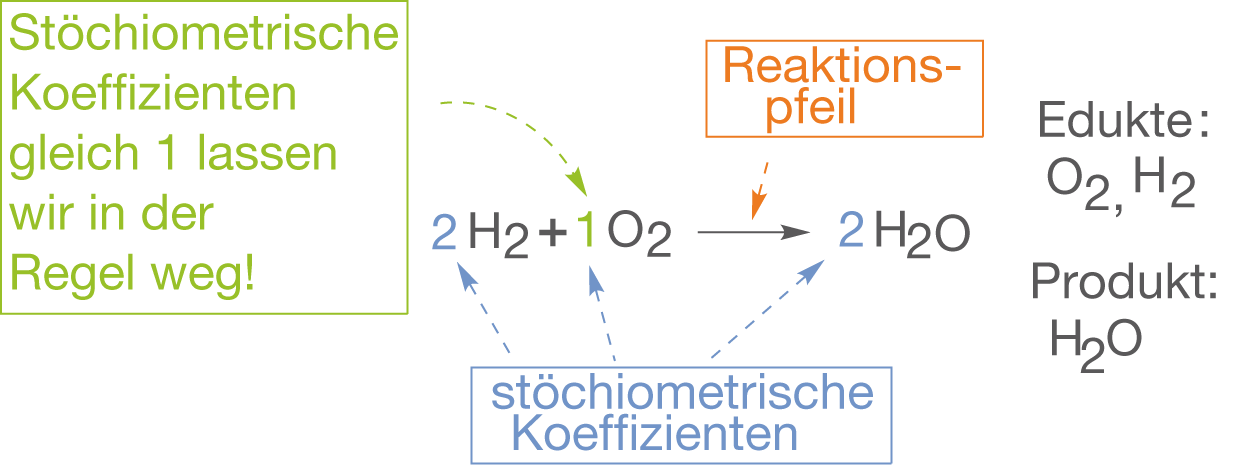
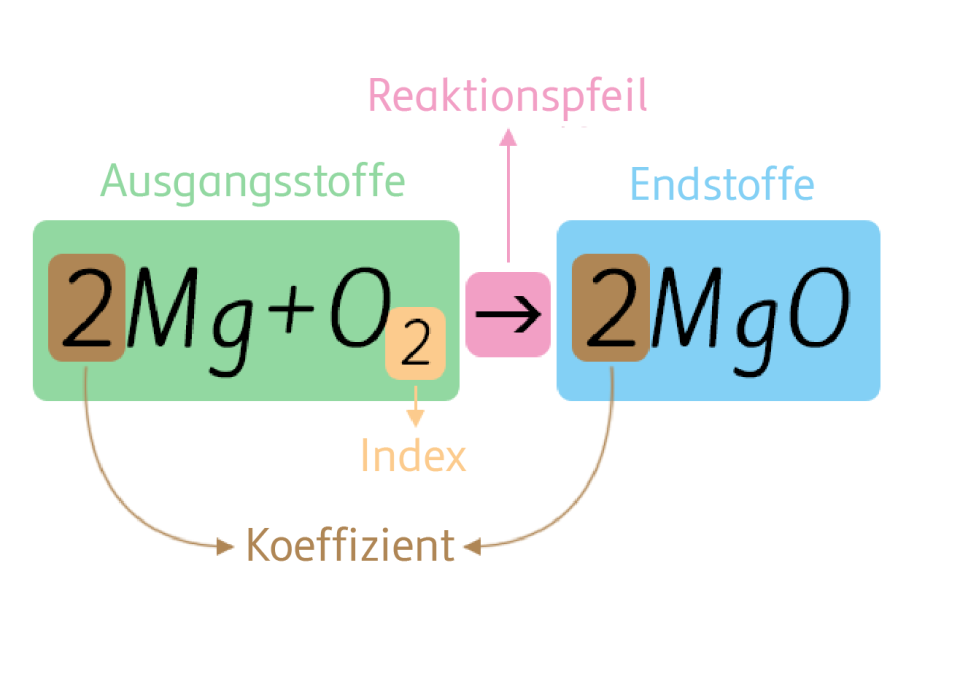
Schreiben Sie die chemischen Formeln der Edukte auf der linken Seite und die chemischen Formeln der Produkte auf der rechten Seite einer Gleichung. Verbinden Sie beide Seiten mit einem Reaktionspfeil (→). Dieser Pfeil zeigt die Richtung der Reaktion an.
Beispiel: Fe + O2 → Fe2O3
Beachten Sie, dass diese Gleichung noch unausgeglichen ist; d.h. die Anzahl der Atome jeder Sorte ist auf der linken und rechten Seite nicht gleich.
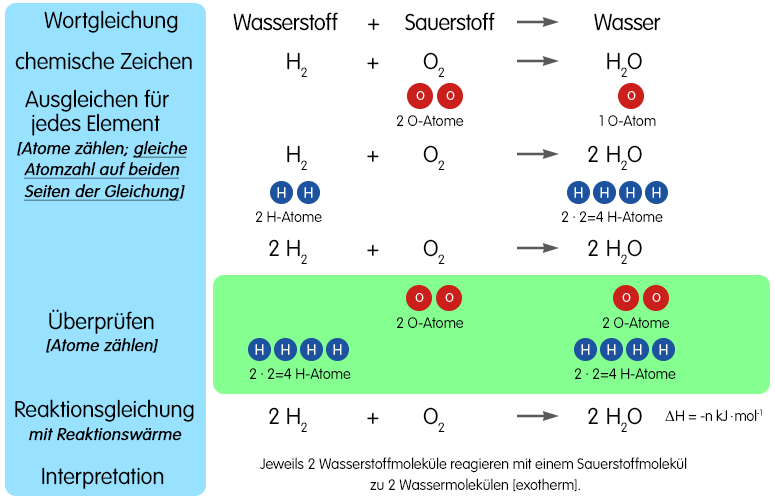
3. Ausgleichen der Gleichung
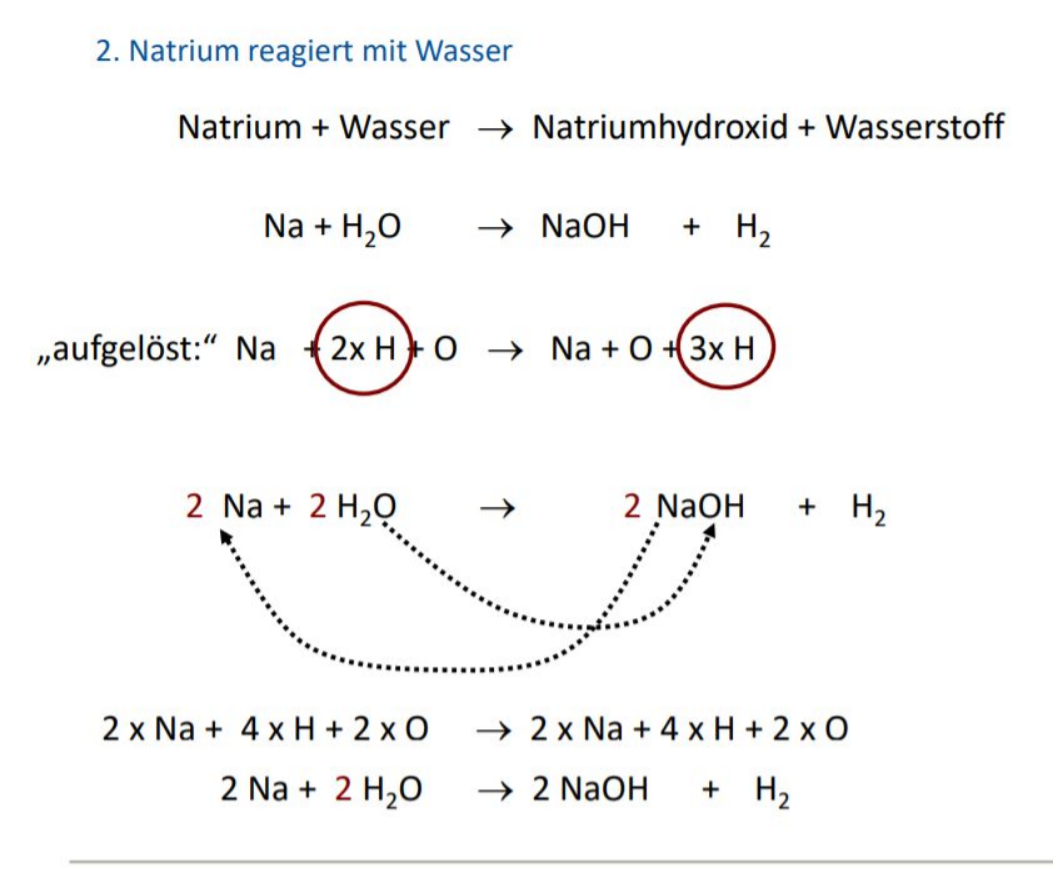
Der wichtigste Schritt ist das Ausgleichen der Gleichung. Dies bedeutet, dass die Anzahl der Atome jedes Elements auf beiden Seiten der Gleichung gleich sein muss. Dies wird durch das Hinzufügen von stöchiometrischen Koeffizienten vor die chemischen Formeln erreicht. Wichtig: Man ändert niemals die chemischen Formeln selbst, um die Gleichung auszugleichen. Dies würde die Identität der Stoffe verändern!
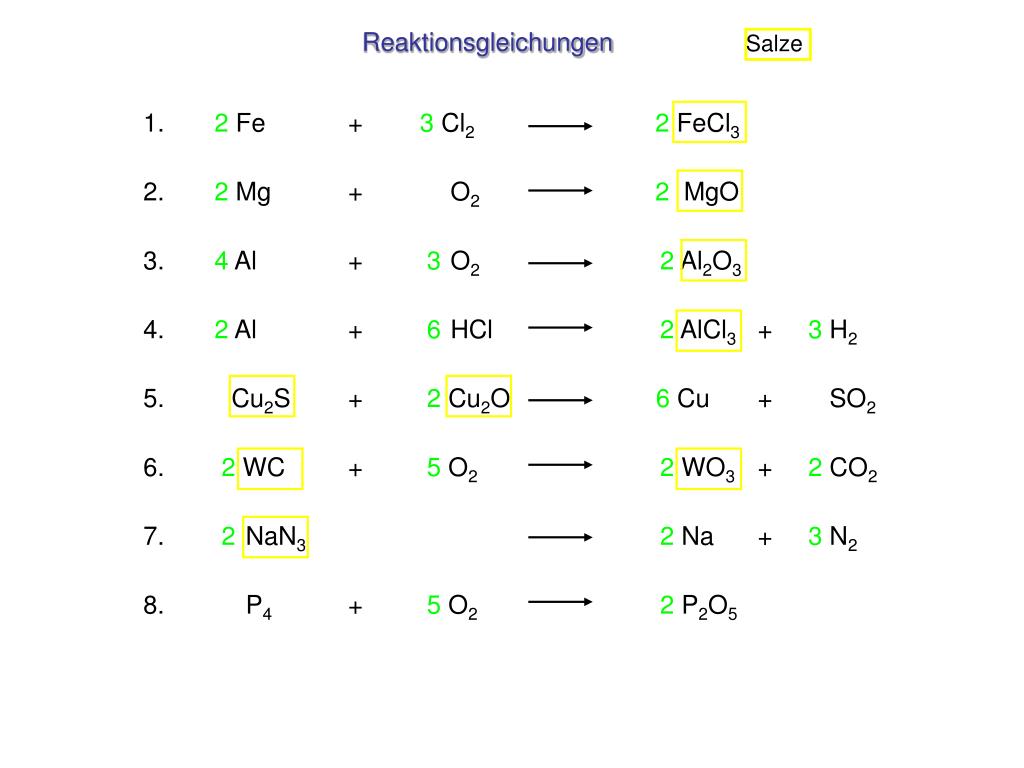
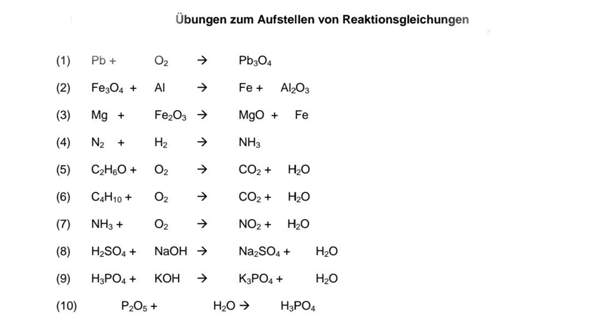
Das Ausgleichen kann durch systematisches Probieren und Anpassen der Koeffizienten erfolgen. Es gibt jedoch auch systematische Methoden, die in komplexeren Fällen hilfreich sind.
Beispiel (Eisen und Sauerstoff):
- Beginnen Sie mit einem Element, das nur in einer Formel auf jeder Seite vorkommt (hier Eisen oder Sauerstoff). Nehmen wir Eisen. Auf der linken Seite haben wir 1 Eisenatom, auf der rechten Seite 2. Um dies auszugleichen, setzen wir den Koeffizienten 2 vor das Eisen auf der linken Seite: 2 Fe + O2 → Fe2O3
- Nun betrachten wir den Sauerstoff. Auf der linken Seite haben wir 2 Sauerstoffatome, auf der rechten Seite 3. Das kleinste gemeinsame Vielfache von 2 und 3 ist 6. Um 6 Sauerstoffatome auf der linken Seite zu erhalten, setzen wir den Koeffizienten 3 vor das Sauerstoffmolekül: 2 Fe + 3 O2 → Fe2O3
- Jetzt haben wir 6 Sauerstoffatome auf beiden Seiten. Um 6 Sauerstoffatome auf der rechten Seite zu erhalten, muss der Koeffizient vor Fe2O3 verändert werden (er ist eigentlich schon richtig, da 1 Fe2O3 Molekül bereits 3 O2 beinhaltet, was multipliziert mit 2 sechs ergibt). Aber, jetzt ist das Eisen nicht mehr ausgeglichen. Um dies zu korrigieren, muss der Koeffizient vor dem Eisen (Fe) geändert werden. Da wir auf der rechten Seite 2 Eisenatome haben, benötigen wir auch 2 auf der linken Seite: 4 Fe + 3 O2 → 2 Fe2O3
Die ausgeglichene Reaktionsgleichung lautet somit:
4 Fe + 3 O2 → 2 Fe2O3
Dies bedeutet, dass 4 Atome Eisen mit 3 Molekülen Sauerstoff zu 2 Formeleinheiten Eisen(III)-oxid reagieren.
4. Angabe des Aggregatzustands (optional)
Es ist oft hilfreich, den Aggregatzustand der Stoffe in der Reaktionsgleichung anzugeben. Dies geschieht durch Hinzufügen von Indizes in Klammern hinter der chemischen Formel:
- (s) für fest (solid)
- (l) für flüssig (liquid)
- (g) für gasförmig (gaseous)
- (aq) für in Wasser gelöst (aqueous)
Beispiel: 4 Fe(s) + 3 O2(g) → 2 Fe2O3(s)
5. Angabe von Reaktionsbedingungen (optional)
Zusätzlich können Reaktionsbedingungen wie Temperatur, Druck oder die Anwesenheit eines Katalysators über oder unter dem Reaktionspfeil angegeben werden.
Beispiel: CH3CH2OH (g) →Al2O3, 350°C CH2=CH2(g) + H2O(g)
Diese Gleichung zeigt, dass Ethanol (CH3CH2OH) in der Gasphase bei 350°C und in Anwesenheit von Aluminiumoxid (Al2O3) als Katalysator zu Ethen (CH2=CH2) und Wasser reagiert.
Häufige Fehler beim Aufstellen von Reaktionsgleichungen
Beim Aufstellen von Reaktionsgleichungen können verschiedene Fehler auftreten. Einige der häufigsten sind:
- Falsche chemische Formeln: Dies ist der häufigste Fehler. Stellen Sie sicher, dass Sie die korrekten chemischen Formeln aller beteiligten Stoffe kennen.
- Verändern der chemischen Formeln beim Ausgleichen: Ändern Sie niemals die chemischen Formeln, um die Gleichung auszugleichen! Verwenden Sie nur stöchiometrische Koeffizienten.
- Ignorieren des Erhaltungssatzes der Masse: Die Anzahl der Atome jedes Elements muss auf beiden Seiten der Gleichung gleich sein.
- Vergessen der Aggregatzustände: Auch wenn sie nicht immer erforderlich sind, können die Aggregatzustände wertvolle Informationen liefern.
Komplexere Reaktionen
Das Ausgleichen von Redoxreaktionen (Reaktionen, bei denen Elektronen übertragen werden) kann besonders herausfordernd sein. Hierfür gibt es spezielle Methoden, wie die Halbzellenmethode oder die Oxidationszahlmethode. Diese Methoden basieren auf der Betrachtung der Teilreaktionen, bei denen Oxidation bzw. Reduktion stattfinden, und dem anschließenden Ausgleichen der Elektronenübertragung.
Das Verständnis der Reaktionsgleichung ist der Schlüssel zum Verständnis der Chemie selbst. Übung macht den Meister – je mehr Reaktionsgleichungen Sie aufstellen, desto sicherer werden Sie darin.
Zusammenfassend lässt sich sagen, dass das Aufstellen von Reaktionsgleichungen eine grundlegende Fähigkeit in der Chemie ist. Es erfordert sorgfältige Beobachtung, das Wissen um chemische Formeln und die Anwendung des Erhaltungssatzes der Masse. Mit Übung und Geduld kann jeder diese Fähigkeit erlernen und die Sprache der Chemie fließend sprechen.
![Wie Stellt Man Reaktionsgleichungen Auf Reaktionsgleichung · Reaktionsschema aufstellen · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2020/04/Reaktionsgleichung-Reaktionsschema-1-1024x576.png)