Wie Viele Elektronen Hat Helium

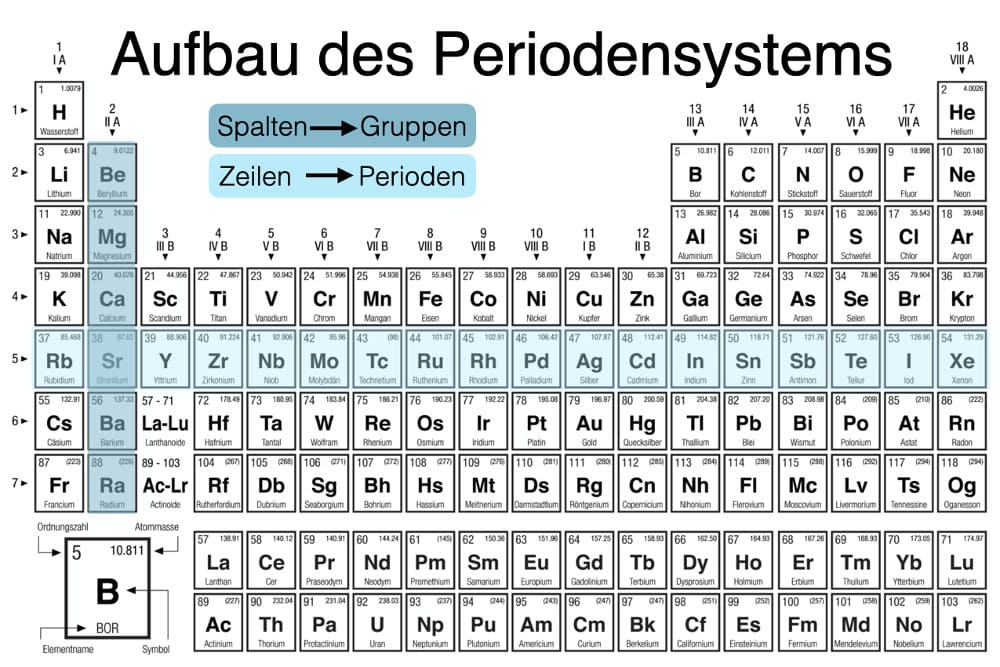
Helium ist ein chemisches Element, das im Periodensystem der Elemente mit dem Symbol He und der Ordnungszahl 2 geführt wird. Es ist ein farbloses, geruchloses, geschmackloses, inertes Edelgas. Eine der grundlegendsten Fragen, die man sich über ein Element stellen kann, ist: Wie viele Elektronen hat es? Die Antwort für Helium ist relativ einfach und eng mit seiner Position im Periodensystem verbunden.
Die Grundlage: Ordnungszahl und Elektronenanzahl
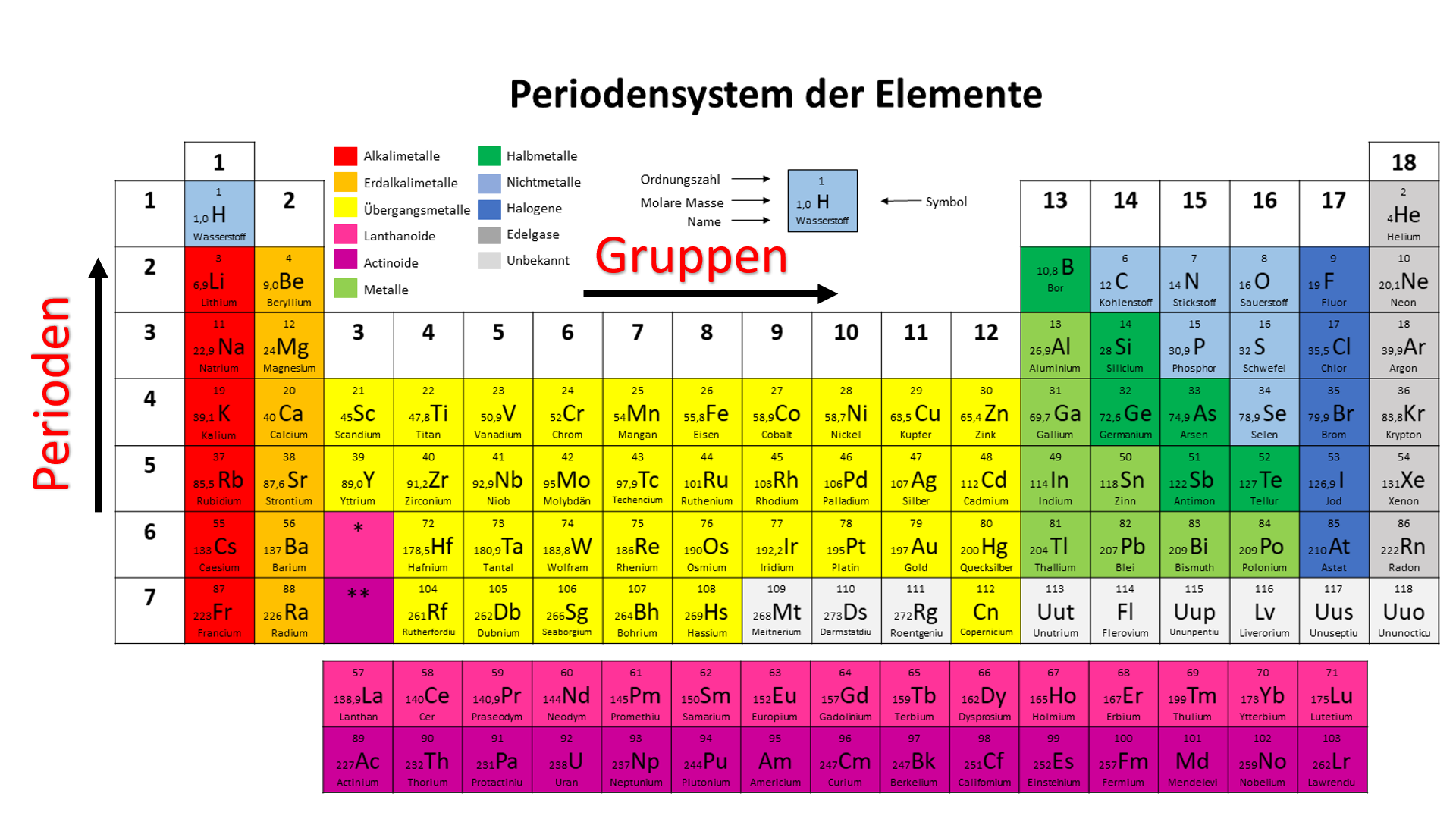
Die Ordnungszahl eines Elements ist die Anzahl der Protonen, die sich im Atomkern dieses Elements befinden. Die Ordnungszahl definiert ein Element eindeutig. So ist beispielsweise jedes Atom mit einem Proton im Kern Wasserstoff (H), und jedes Atom mit zwei Protonen im Kern ist Helium (He). Da Helium die Ordnungszahl 2 hat, bedeutet das, dass sich zwei Protonen in seinem Atomkern befinden.
Atome sind elektrisch neutral. Das bedeutet, dass sie insgesamt keine elektrische Ladung tragen. Um dies zu erreichen, muss die positive Ladung der Protonen durch eine gleiche Anzahl negativer Ladungen ausgeglichen werden. Die negativen Ladungen werden von den Elektronen getragen, die um den Atomkern kreisen. In einem neutralen Atom ist die Anzahl der Elektronen also immer gleich der Anzahl der Protonen.
Da Helium zwei Protonen hat, besitzt ein neutrales Heliumatom demzufolge auch zwei Elektronen. Diese Information ist fundamental, um die chemischen Eigenschaften von Helium zu verstehen.
Die Elektronenkonfiguration von Helium
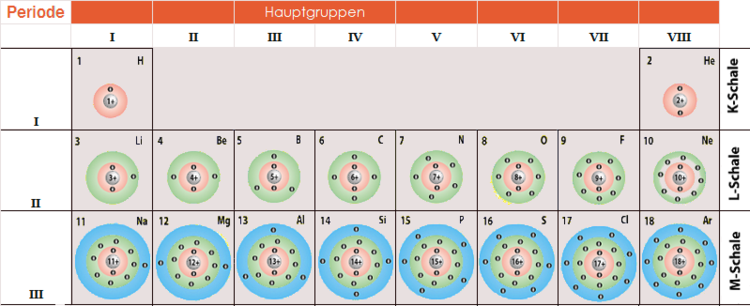
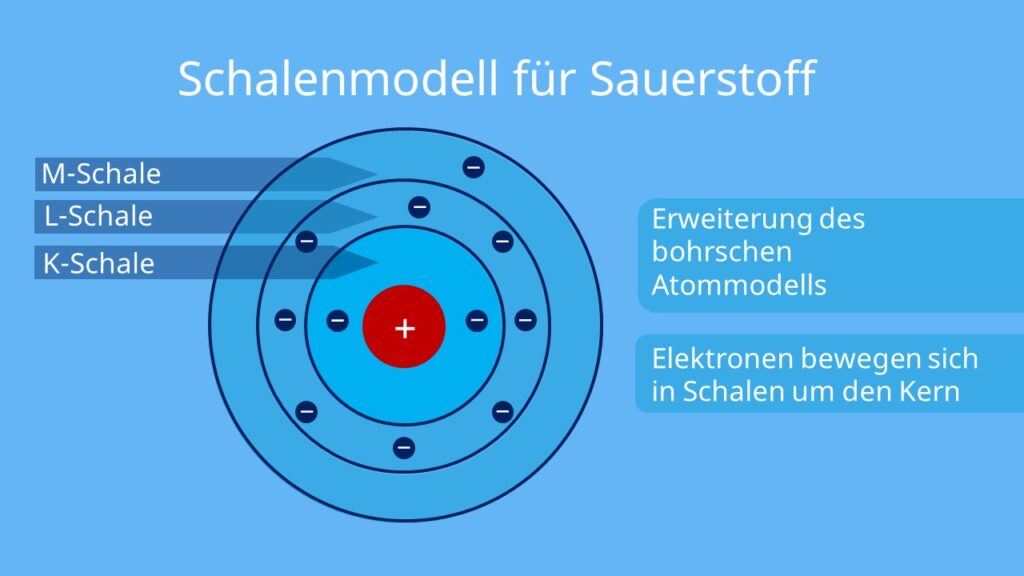
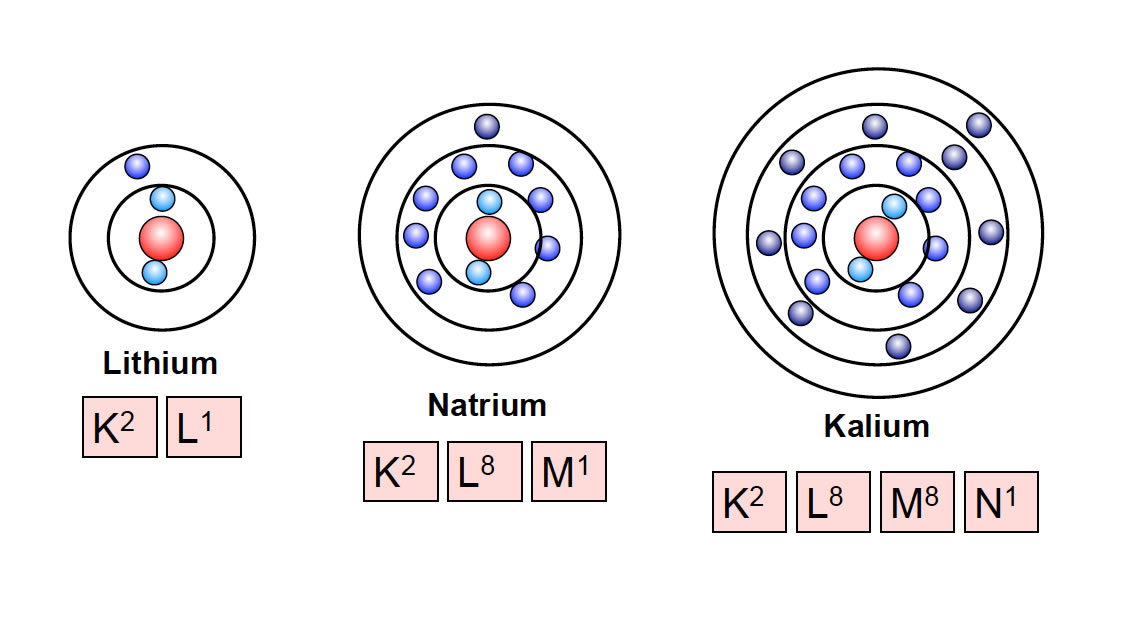
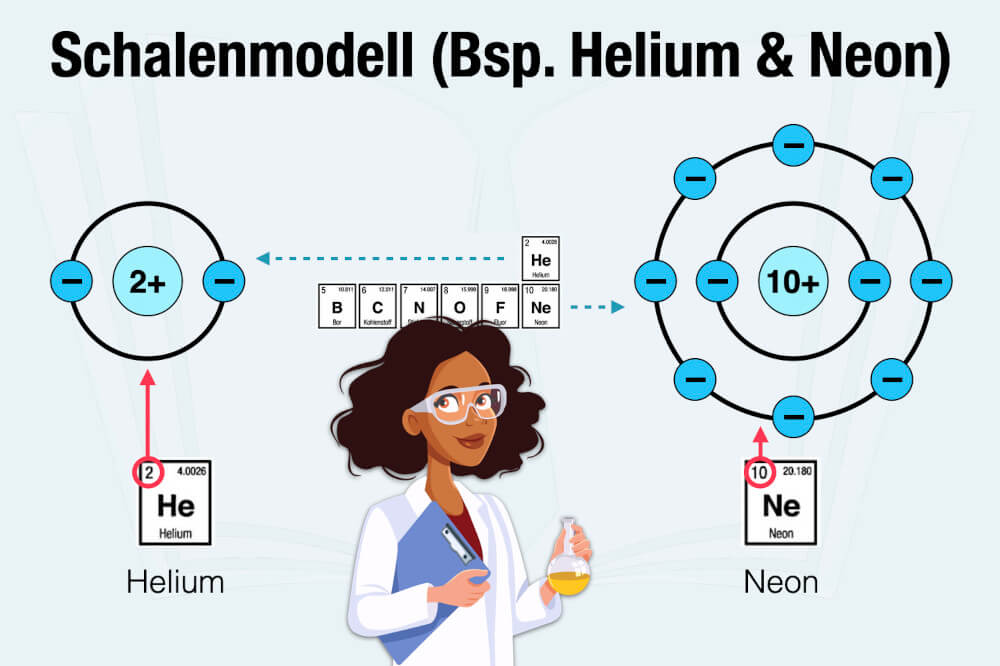
Die Elektronen eines Atoms sind nicht willkürlich um den Kern verteilt. Sie ordnen sich in spezifischen Elektronenschalen an, die unterschiedliche Energieniveaus darstellen. Die erste Elektronenschale, die dem Kern am nächsten ist, wird als K-Schale bezeichnet und kann maximal zwei Elektronen aufnehmen. Die zweite Schale, die L-Schale, kann bis zu acht Elektronen aufnehmen, und so weiter.
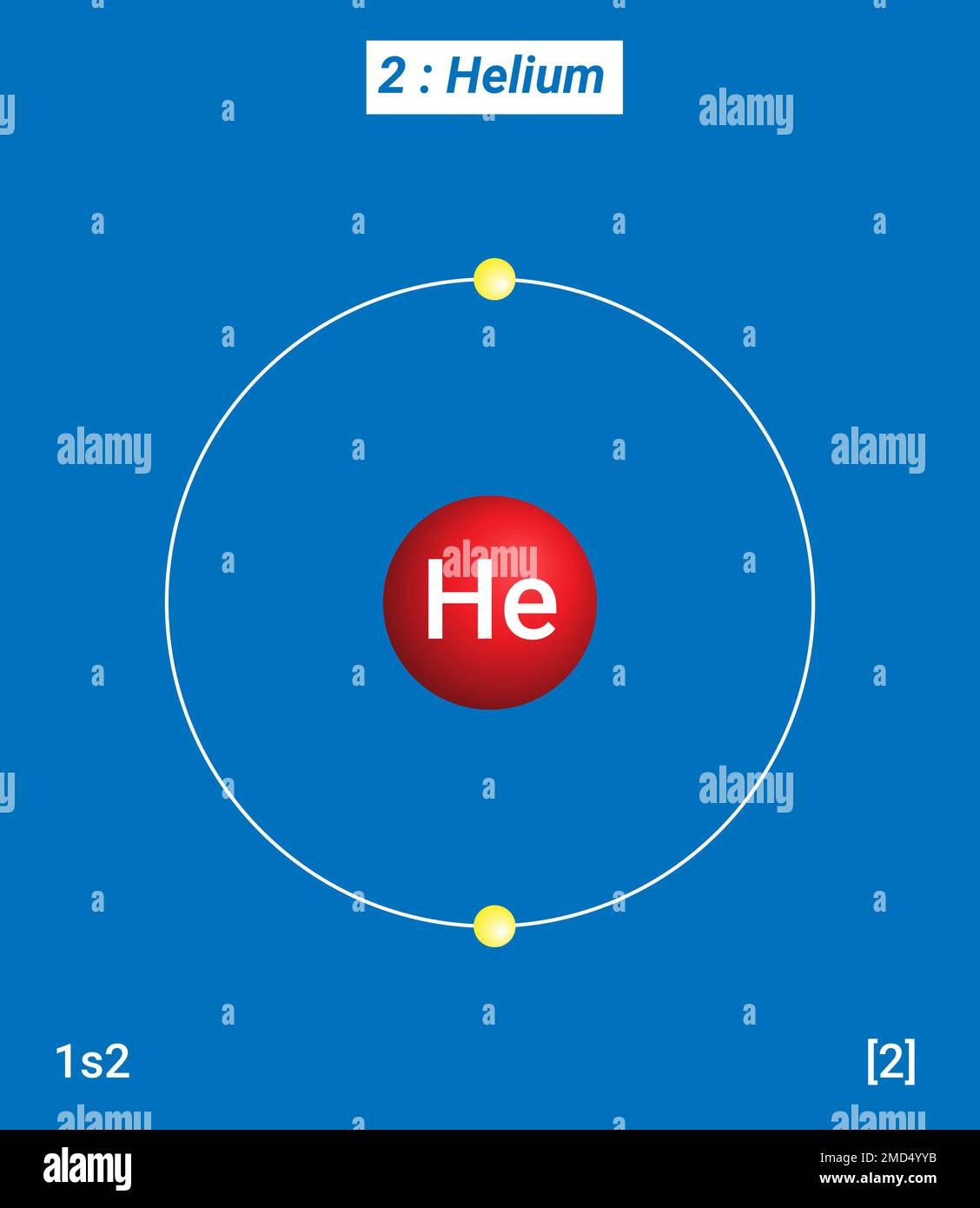
Helium hat nur zwei Elektronen, und diese beiden Elektronen befinden sich in der K-Schale. Da die K-Schale maximal zwei Elektronen aufnehmen kann, ist die Elektronenschale von Helium vollständig gefüllt. Dies wird als vollständige Valenzschale bezeichnet, und es ist diese vollständige Valenzschale, die Helium seine charakteristischen Eigenschaften als Edelgas verleiht.
Die Elektronenkonfiguration von Helium wird oft als 1s² geschrieben. Das bedeutet, dass sich zwei Elektronen (²-hochgestellt) im 1s-Orbital befinden. Das 1s-Orbital ist das Orbital mit der niedrigsten Energie und gehört zur K-Schale (n=1).
Helium als Edelgas: Die Bedeutung der Elektronenkonfiguration
Die chemische Inaktivität von Helium, seine Eigenschaft als Edelgas, rührt von seiner stabilen Elektronenkonfiguration her. Atome streben danach, eine vollständige Valenzschale zu erreichen, da dies einen Zustand niedriger Energie und hoher Stabilität darstellt. Atome können eine vollständige Valenzschale erreichen, indem sie Elektronen abgeben, aufnehmen oder teilen (durch chemische Bindungen).
Helium besitzt bereits eine vollständige Valenzschale mit seinen zwei Elektronen in der K-Schale. Daher hat es keine Tendenz, Elektronen abzugeben, aufzunehmen oder zu teilen. Dies macht es extrem reaktionsträge. Es bildet unter normalen Bedingungen keine chemischen Verbindungen mit anderen Elementen. Es gibt zwar einige sehr spezielle Verbindungen unter extremen Bedingungen, aber diese sind sehr selten und instabil.
Diese Inaktivität macht Helium in vielen Anwendungen sehr nützlich. Zum Beispiel wird es als Schutzgas beim Schweißen verwendet, um zu verhindern, dass Metalle mit Sauerstoff oder Stickstoff aus der Luft reagieren. Es wird auch zur Kühlung von Supraleitern eingesetzt, da es einen sehr niedrigen Siedepunkt hat und nicht mit den Supraleitern reagiert.
Ionen von Helium
Obwohl Helium normalerweise neutral ist und zwei Elektronen besitzt, kann es auch Ionen bilden, indem es Elektronen verliert. Das häufigste Ion von Helium ist He+, bei dem ein Elektron entfernt wurde. Dieses Ion hat eine positive Ladung, da es zwei Protonen, aber nur ein Elektron hat.
Es ist auch möglich, das zweite Elektron zu entfernen und das He2+-Ion zu erzeugen. Dieses Ion hat eine noch stärkere positive Ladung und ist sehr reaktiv, da es keine Elektronen mehr besitzt.
Die Bildung von Helium-Ionen erfordert Energie, da es der stabilen Elektronenkonfiguration entgegenwirkt. Diese Ionen sind jedoch in bestimmten Umgebungen, wie z.B. in Plasmen oder in Sternen, vorhanden.
Isotope von Helium
Neben der Anzahl der Elektronen und Protonen ist auch die Anzahl der Neutronen im Kern wichtig. Atome desselben Elements mit unterschiedlicher Anzahl von Neutronen werden als Isotope bezeichnet. Helium hat zwei stabile Isotope: Helium-4 (4He) und Helium-3 (3He).
Helium-4 ist das weitaus häufigste Isotop von Helium. Es besteht aus zwei Protonen und zwei Neutronen im Kern. Helium-3 ist ein viel selteneres Isotop und besteht aus zwei Protonen und nur einem Neutron im Kern. Obwohl sie unterschiedliche Massen haben, haben beide Isotope immer noch zwei Elektronen, da die Anzahl der Elektronen durch die Anzahl der Protonen (Ordnungszahl) bestimmt wird.
Die unterschiedlichen Isotope von Helium haben leicht unterschiedliche physikalische Eigenschaften. Zum Beispiel hat Helium-3 einen niedrigeren Siedepunkt als Helium-4. Helium-3 zeigt auch bei sehr tiefen Temperaturen ungewöhnliche suprafluide Eigenschaften.
Zusammenfassung
Zusammenfassend lässt sich sagen, dass ein neutrales Heliumatom zwei Elektronen besitzt. Diese zwei Elektronen befinden sich in der K-Schale und füllen diese vollständig aus. Diese vollständige Valenzschale verleiht Helium seine charakteristischen Eigenschaften als Edelgas: Es ist chemisch inert und bildet unter normalen Bedingungen keine chemischen Verbindungen. Die Anzahl der Elektronen wird durch die Anzahl der Protonen im Kern (Ordnungszahl) bestimmt, und diese Anzahl ist für Helium immer 2.
Das Verständnis der Elektronenkonfiguration von Helium ist entscheidend, um seine chemischen und physikalischen Eigenschaften zu verstehen und seine vielfältigen Anwendungen zu erklären.







![Wie Viele Elektronen Hat Helium Schalenmodell • Aufbau und Elektronenschalen · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2020/03/WP_Schalenmodell_Schalenmodell-Alkalimetalle-1024x576.jpg)
![Wie Viele Elektronen Hat Helium Periodensystem Erklärung • Aufbau, Perioden & Gruppen · [mit Video]](https://blog.assets.studyflix.de/wp-content/uploads/2021/12/WP-Bild_Atomaufbau-Lithium-1024x576.jpg)